
- •2. Лекарственные вещества, содержащие фенольный гидроксил
- •2.4. Реакция окисления
- •3. Лекарственные вещества, содержащие карбонильную группу (альдегидную, кетонную)
- •3.1. Реакция окисления
- •5. Лекарственные вещества, содержащие первичную ароматическую аминогруппуАминами называются производные аммиака, в которых один, два или три атома водорода заменены на углеводородные радикалы.
- •6. Лекарственные вещества, содержащие ароматическую нитрогруппу
- •7. Лекарственные вещества, содержащие вторичную аминогруппу
- •8. Лекарственные вещества, содержащие сложноэфирную группу
- •9. Лекарственные вещества, содержащие амидную группу (продолжение)
- •10. Лекарственные вещества, содержащие сульфамидную группу
- •11. Лекарственные вещества, содержащие ковалентно связанный галоген
- •12. Лекарственные вещества, содержащие азометиновую группу, ковалентно связанную серу, пиридиновый цикл, ароматический радикал, непредельную связь
- •Химические свойства
- •Реакции подлинности
2.4. Реакция окисления
Фенолы могут окисляться до различных соединений, но чаще всего до о- или п-хинонов (циклических дикетонов), окрашенных в розовый или реже в жёлтый цвет.
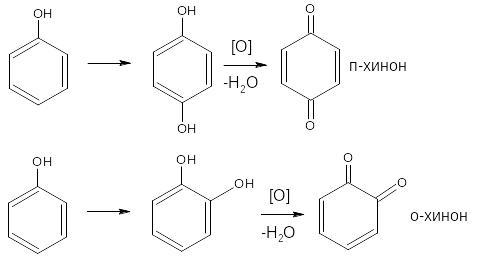
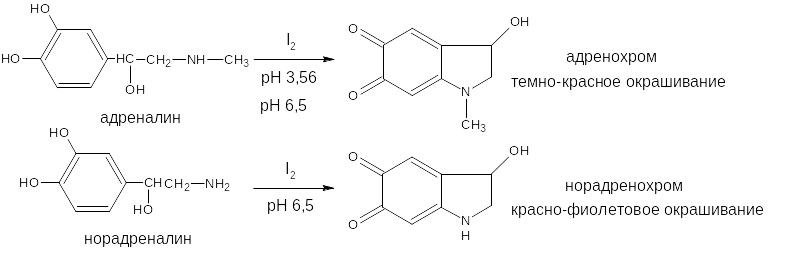
В частности, реакция окисления рекомендована ГФ для адреналина и норадреналина: в качестве окислителя используется йод при определённом значении рН среды. При этом образуются окрашенные продукты адренохром и норадренохром.
НВЕР ЧИТАЙ ТОЛЬКО ПРО НОРАДРЕНАЛИН!
2.5. Реакция образования индофенолового красителя
Основана на окислении фенолов до хинонов, которые при конденсации с аммиаком или аминопроизводным и избытком фенола образуют индофеноловый краситель, окрашенный в фиолетовый цвет.
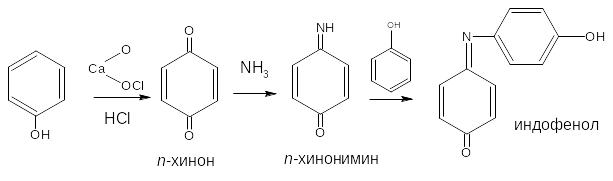
При действии нитрита натрия в кислой среде образуется п-нитрозофенол, изомеризующийся в п-хиноидоксим, который, реагируя с избытком фенола в кислой среде, образует индофенол:
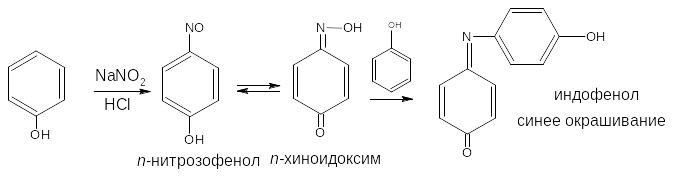
2.6. Образование нитрозосоединений
При взаимодействии с разведенной азотной кислотой фенолы могут нитроваться при комнатной температуре, образуя о- и п-нитропроизводные. Образующееся нитропроизводное содержит в п-положении подвижный атом водорода гидроксильной группы, образуется таутомерная аци-форма с хиноидной структурой, она обычно окрашена в желтый цвет. Добавление щелочи усиливает окраску, вследствие образования хорошо диссоциируемой соли:
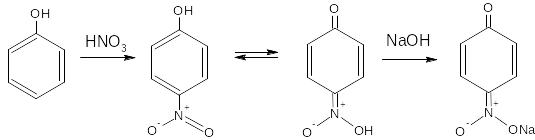
2.7. Реакция конденсации с альдегидами или ангидридами кислот
- с формальдегидом в присутствии концентрированной серной кислоты с образованием ауринового (арилметанового) красителя окрашенного в красный цвет.
Реакция является фармакопейной для кислоты салициловой. Концентрированная серная кислота на первой стадии реакции играет роль водоотнимающего средства, на второй – является окислителем.
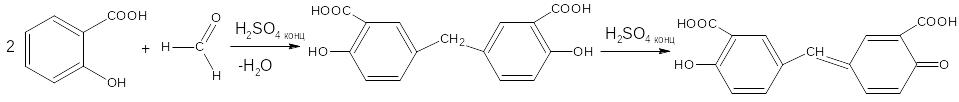
С фталевым ангидридом (сплавление и последующее растворение плава в щёлочи) рекомендована фармакопеей для идентификации фенола и резорцина.
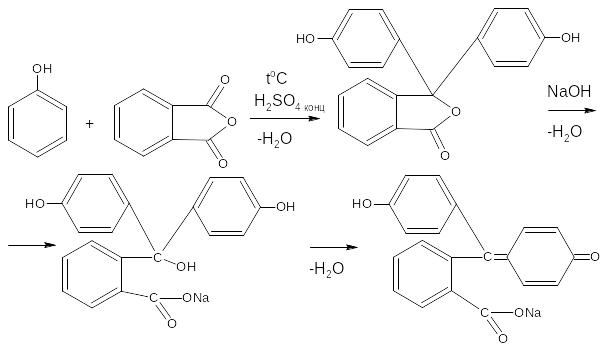
Количественное определение
2.8. Броматометрия
Метод основан на электрофильном замещении атомов водорода ароматического кольца на бром, выделенный в реакции бромата калия с бромидом калия в кислой среде.
K BrO3 + 5KBr + 6 HCl → 3Br2 + 6KCl + 3H2O
Используют способы прямого и обратного титрования. В прямом – титруют броматом калия в присутствии бромида калия с индикатором метиловым оранжевым или метиловым красным от розовой окраски до обесцвечивания. В точке эквивалентности избыточная капля бромата калия выделяет бром, который окисляет индикатор и раствор обесцвечивается. При обратном титровании вводят избыток бромата калия, добавляют калия бромид, создают кислую среду, выдерживают нужное для бромирования время и после чего избыток брома определяют йодометрически (индикатор – крахмал).
Br2 + 2KI → I2 + 2KBr
I2 + 2Na2S2O3 → Na2S4O6 + 2NaI
Способом прямого титрования определяют по ГФ Х тимол, обратного – фенол, резорцин, кислоту салициловую, синэстрол и другие ЛВ.
М.э. = ¼ М.м. (тимол)
М.э. = 1/6 М.м. (фенол, резорцин, кислота салициловая)
М.э. = 1/8 М.м. (синэстрол)
2.9. Йодометрия
Основана на электрофильном замещении атомов водорода ароматического кольца на йод.
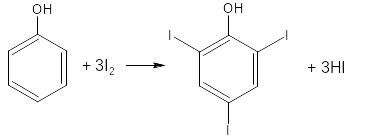
Для связывания йодоводородной кислоты, смещающей равновесие в обратную сторону, добавляют ацетат или гидрокарбонат натрия.
HI + NaHCO3 → NaI + H2O + CO2
HI + CH3COONa → NaI + CH3COOH
Используют способы прямого и обратного титрования. В последнем – избыток йода оттитровывают тиосульфатом натрия.
I2 + 2NaS2O3 → 2NaI + Na2S4O6
М.э. = 1/6 М.м. (фенол)
2.10. Йодхлорметрия
Метод основан на электрофильном замещении атомов водорода ароматического кольца на йод, входящий в состав йодмонохлорида.
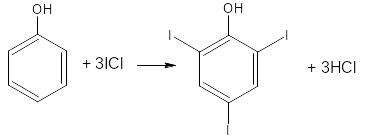
Используют способ обратного титрования – избыток йодмонохлорида определяют йодометрически.
ICl + KI → I2 + KCl
I2 + 2Na2S2O6 → 2NaI + Na2S4O6
М.э. = 1/6 М.м. (фенол)
2.11. Метод ацетилирования
Основан на свойстве ЛВ за счёт спиртовых гидроксилов ацетилироваться уксусным ангидридом с образованием нерастворимых сложных эфиров и выделением эквивалентного количества уксусной кислоты, которую оттитровывают гидроксидом натрия.
Используют по ГФ Х для количественной оценки синэстрола.
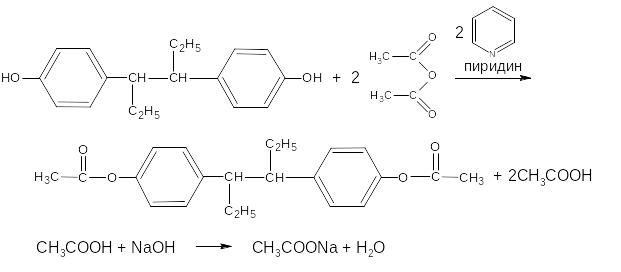
М.э. = ½ М.м.
2.12. Алкалиметрический метод нейтрализации в среде протофильного растворителя диметилформамида (ДМФА).
ЛВ группы фенолов проявляют очень слабые кислотные свойства, их определение алкалиметрическим методом нейтрализации в водных или смешанных средах невозможно, поэтому используют титрование в среде неводных растворителей, в частности, ДМФА. Метод основан на солеобразовании определяемой слабой кислоты (фенола) с титрантом (метилатом натрия) в среде протофильного растворителя, усиливающего кислотные свойства.
