
- •Введение
- •1. УЛЬТРАЗВУКОВОЙ КОНТРОЛЬ КИНЕТИКИ ТВЕРДЕНИЯ СТРОИТЕЛЬНЫХ МАТЕРИАЛОВ НА ОСНОВЕ ВЯЖУЩИХ МАТЕРИАЛОВ
- •2. УЛЬТРАЗВУКОВОЙ КОНТРОЛЬ ПРОЧНОСТИ СТРОИТЕЛЬНЫХ МАТЕРИАЛОВ
- •2.1. Назначение прибора УК-14п
- •2.2. Устройство и работа прибора УК-14п
- •2.3. Определение скорости ультразвука и прочности бетона
- •3. РЕНГЕНОВСКАЯ ДИФРАКТОМЕТРИЯ
- •3.1. Источники возбуждения спектра
- •3.2. Методы и схемы съёмки рентгенограмм
- •3.3. Качественный анализ
- •4. КАЧЕСТВЕННЫЙ РЕНТГЕНОФАЗОВЫЙ АНАЛИЗ (расшифровка рентгенограмм)
- •5.1. Получение данных ДТА и их расшифровка
- •5.2. Дериватография
- •5.3. Качественный фазовый анализ
- •5.4. Количественный фазовый анализ
- •5.5. Термовесовой метод фазового анализа
- •5.6. Фотоэлектроколориметрия
- •5.7. Аппаратура, применяемая при фотоэлектроколориметрии
- •5.9. Хроматографические методы
- •Библиографический список
При исследовании глинистых веществ целесообразно выделять фракции менее 0,001 мм, т.к. присутствие примесей затушевывает эффекты, связанные непосредственно с глинистыми материалами.
Часто бывает необходимо освободиться от примесей соответствующей обработкой образца. Например, органические примеси разрушаются 30%-ным раствором пергидроля (Н2О2), а карбонат кальция – 2,5%-ным раствором соляной кислоты. На результаты анализа влияет степень уплотнения исследуемого и эталонного веществ в тиглях. Различная степень их уплотнения приводит к различной теплопроводности, в результате чего кривая ДТА отклоняется от базисного положения. Особенно это заметно в низкотемпературной области. Одинаковой степени уплотнения препарата и эталона достигают прессованием материалов при одинаковом давлении или
путем трамбования при одинаковом числе ударов. При анализе |
|
|
И |
жидкостей в тигель насыпают эталонный материал и пропитывают его |
|
0,15–0,20 мл исследуемого вещества. |
|
Д |
|
На температуру и площадь эффектов большое влияние оказывает скорость нагревания. Для получения воспроизводимых и сопоставимых
с эталонными кривыми ДТА температура в печи должна возрастать с |
|
постоянной скоростью [14]. |
А |
|
|
б |
|
5.2. Дериватография |
|
и |
|
Дериватограф – это термоустановка, позволяющая на одном и том |
|
же листе фотобумаги одновременно автоматически получать
температурную |
д фференциальную кривые |
нагревания |
и простую |
(интегральную) и дифференциальную кривые потери веса. |
Схема де- |
||
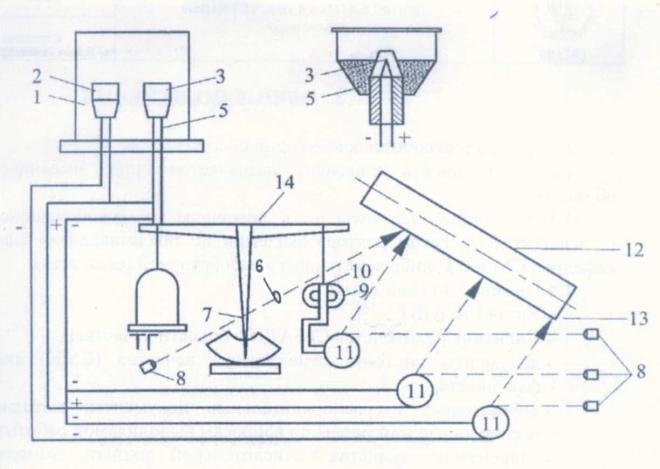
риватографа показана на рис. 16. |
|
|
|
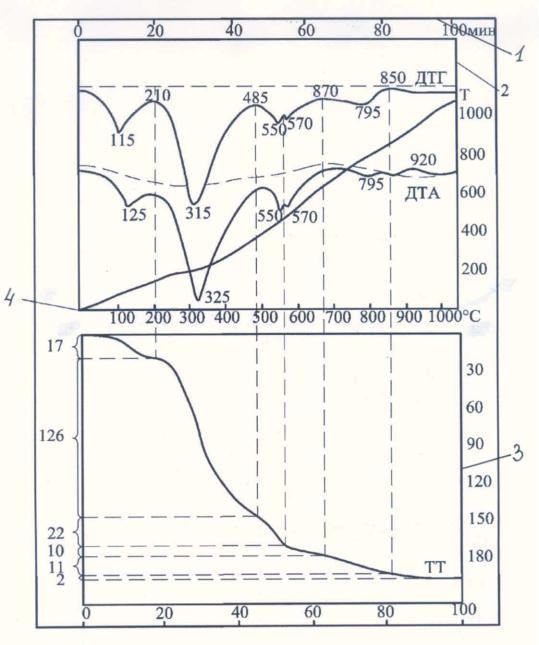
На рис. 17 изображена дериватограмма |
боксита (Н.Д. Топор): |
||
1 – шкала времениС; 2 – вертикальная шкала температур; 3 – шкала потери |
|||
веса; 4 – горизонтальная шкала температур; ДТГ – дифференциальная кривая потери веса; ДТА – дифференциальная кривая нагревания; Т – температурная кривая нагревания; ТГ – простая кривая потери веса.
Деления на шкале потери веса 3 являются равномерными, цена их выбирается с учетом чувствительности весов. Шкала времени 1 вращения барабана самописца также равномерная, а деления шкалы температур 2 неравномерные и выбираются в зависимости от предельных температур нагрева печи (150, 300, 600, 900 и 1200 °С). Все кривые на дериватограмме имеют одну координату – время.
25
|
|
А |
И |
Рис. 16. |
|
|
|
Схема дериватографа: 1 – электропечь; 2 – тигель для эталона; |
|||
|
б |
|
|
3 – тигель для пробы; 4 |
– горячийДспай термопары; 5 – фарфоровая |
||
трубка-держатель термопары и тигеля; 6 – оптическая щель; |
|||
7 |
и |
|
|
– стрелка весов; 8 – осветители; 9 – постоянный магнит; |
|||
10 – электрокатушка; 11 – зеркальные гальванометры; 12 – барабан самоп сца; 13 – шаблоны для оптического Свпечатыван я шкал; 14 – аналитические весы
Кривая ДТА на дериватограмме служит целям качественного фазового анализа, а кривые ДТГ и ТГ позволят подсчитывать количество того или иного соединения в сложном по составу материале. Совместный анализ нескольких кривых значительно увеличивает разрешающую способность метода.
5.3. Качественный фазовый анализ
Качественный фазовый анализ веществ основан на том, что температурные границы превращения веществ остаются практически неизменными, независимо от того, находится ли исследуемое соединение в чистом виде или в смеси с другими солями или минералами. Это при условии, что вещества, находящиеся в смеси, при нагревании не реагируют друг с другом. Следовательно, при нагревании смеси
26
минералов, температурные эффекты превращения которых не совпадают, эти соединения можно идентифицировать. Если минерал имеет несколько термических эффектов, то совпадение некоторых из них с эффектами других соединений может не помешать правильному качественному анализу.
|
|
|
|
И |
|
|
|
Д |
|
|
|
А |
|
|
|
б |
|
|
|
и |
|
|
|
|
С |
|
|
|
|
Рис. 17. Деривитограмма боксита
Расшифровка термограмм. По нулевым точкам проводят ось абсцисс. В точке начала записи температурной кривой проводят перпендикуляр к оси абсцисс и получают ось ординат. На оси абсцисс откладывают время в минутах. На ось ординат копируют температурную линейку. Для установления температуры того или иного эффекта на дифференциальной кривой накладывают на термограмму
27
простую линейку так, чтобы она была параллельна оси ординат, а край ее проходил через требуемую точку кривой, и проводят вертикальную линию. Место пересечения этой линии с кривой простой температурной записи является той точкой, по которой определяют температуру.
Проведя через указанную точку линию, параллельную оси абсцисс, до пересечения с ординатой, находят искомую температуру. Проводят также нулевую линию, параллельную оси абсцисс. Температуры начала, максимума и конца термоэффектов проставляют непосредственно на фотобумаге.
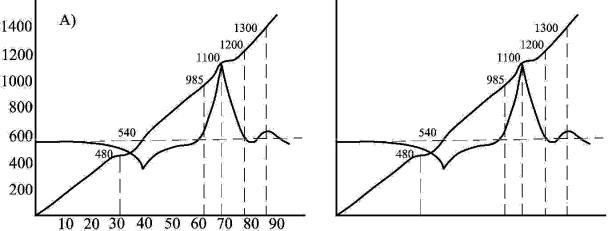
Пример такого оформления термограммы показан на рис. 18, а. При использовании температурной линейки нет необходимости градуировать ординату и абсциссу, тогда на термограмме проставляют только температуры термоэффектов (рис. 18, б).
|
|
|
|
И |
|
а |
|
|
|
|
|
|
б |
|
|
|
|
Д |
|
|
|
|
||
|
|
|
А |
|
Рис. 18. |
С |
|
||
Разл чные в дыбправильного оформления термограмм каолинита |
||||
На обратнойистороне термограммы должны быть записаны дата
опыта, название испытуемого вещества, его навеска, температура, скорость вращения барабана и вид эталона.
Термограмма должна анализироваться в том виде, как она записана прибором, поскольку отклонения кривой от нулевой линии имеют свою физико-химическую причину и являются дополнительной информацией при расшифровке. Расшифровка термограммы неизвестного вещества производится с помощью уже известных данных по температурам превращений других материалов. Термические эффекты ряда материалов, применяемых специалистами по вяжущим веществам, приведены в табл. 2, 3, 4.
Если имеющиеся справочные данные не позволяют надежно установить природу термоэффекта, то для идентификации его привлекают другие методы анализа – рентгеноскопию, электронную микроскопию, спектроскопию и т.п. [15].
28

|
|
|
|
|
|
|
Таблица 2 |
|
|
Термические эффекты некоторых минералов |
|||||
|
|
|
|
|
|
||
Минерал |
|
Формула |
Температура |
|
Природа |
||
|
минерала |
эффекта, °С |
|
|
эффекта |
||
|
|
|
|
|
|
|
|
1 |
|
|
2 |
3 |
|
|
4 |
Кальцит |
|
CaCO3 |
|
(–) 860-920 |
|
Диссоциация (44% CO2) |
|
Арагонит |
|
CaCO3 |
|
(–) 390-420 |
|
Полиморфное превращение |
|
|
|
|
|
|
|
в кальцит |
|
|
|
|
|
|
|
|
|
|
|
|
|
(–) 860-920 |
|
Диссоциация (44% CO2) |
|
Магнезит |
|
MgCO3 |
|
(–) 540-710 |
|
Диссоциация (52,2% CO2) |
|
Гидрокарбонат |
MgCO3·3H2O |
(–) 170-210 |
|
Дегидратация (потеря 2H2O) |
|||
магния |
|
|
|
(–) 400-450 |
|
Дегидратация (потеря 1H2O) |
|
|
|
|
|
|
|
И |
|
|
|
|
|
(–) 500-530 |
|
Диссоциация MgCO3 |
|
|
|
|
|
(+) 530-600 |
|
Кристаллизация аморфной |
|
|
|
|
|
|
|
MgO |
|
|
|
|
|
|
|
||
Доломит |
|
CaMg(CO3)2 |
(–) 730-790 |
|
Распад доломита на CaCO3 |
||
|
|
|
|
А |
|
и MgCO3 |
и диссоциация |
|
|
|
|
|
|
MgCO3 (23,9% CO2) |
|
|
|
|
б |
(–) 730Д |
|
|
|
Анкерит |
|
(Mg, Fe)CO3· |
Диссоциация MgCO3 |
||||
|
|
·CaCO3 |
|
(–) 810-830 |
|
Диссоциация FeCO3 и обра- |
|
|
|
и |
|
|
зование Fe2O3·CaCO3 |
||
|
|
|
|
|
|
||
|
|
|
|
(–) 900-930 |
|
Диссоциация CaCO3 |
|
|
С |
|
|
|
Диссоциация (38% CO3) |
||
Сидерит |
|
FeCO3 |
|
(–) 350-585 |
|
||
|
|
|
|
(+) 600 |
|
Окисление FeO до Fe2O3 |
|
|
|
|
|
(+) 830 |
|
|
|
Стронцианит |
SrCO3 |
|
(–) 930-1200 |
Диссоциация SrCO3 |
|||
Витерит |
|
BaCO3 |
|
(–) 835 |
|
Полиморфизм BaCO3 |
|
|
|
|
|
(–) 970-980 |
|
|
|
|
|
|
|
(–) 1200 |
|
Диссоциация BaCO3 |
|
Родохрозит |
|
MnCO3 |
|
(–) 100-350 |
|
Потеря адсорбционной воды |
|
|
|
|
|
(–) 425-600 |
|
Диссоциация MnCO3 (38,4% |
|
|
|
|
|
|
|
CO2) |
|
|
|
|
|
(+) 730-800 |
|
Окисление MnO |
|
|
|
|
|
(–) 950 |
|
Восстановление до Mn3O4 |
|
|
|
|
|
(–) 1175 |
|
Инверсионное превращение |
|
|
|
|
|
|
|
Mn3O4 |
из тетрагональной |
|
|
|
|
|
|
формы в кубическую |
|
Смитсонит |
|
ZnCO3 |
|
(–) 425-550 |
|
Диссоциация ZnCO3 |
|
29

|
|
|
|
|
|
|
|
|
Продолжение табл. 2 |
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
2 |
|
|
|
3 |
|
|
|
4 |
Брусит |
Mg(OH)2 |
|
|
(–) 405-450 |
|
|
Дегидратация (31% H2O) |
|||
Гидроокись |
Ca(OH)2 |
|
|
|
(–) 530-580 |
|
|
Дегидратация |
||
кальция (порт- |
|
|
|
|
|
|
|
|
|
|
лантид) |
|
|
|
|
|
|
|
|
|
|
Железный маг- |
(Mg, Fe)CO2 |
|
|
(–) 500-590 |
|
|
Диссоциация |
|||
незит |
|
|
|
|
(+) 755 |
|
|
Окисление FeO до Fe2O3 |
||
Гидромагнезит |
3MgCO3· |
|
|
(–) 275-375 |
|
|
Дегидратация Mg(OH)2 |
|||
|
·Mg(OH)2·3H2O |
(–) 510 |
|
|
Превращение аморфной MgO |
|||||
|
|
|
|
|
|
|
|
|
в кристаллический периклаз |
|
|
|
|
|
|
(–) 485-610 |
|
|
Диссоциация MgCO3 |
||
Диаспор |
β-AlO(OH) |
|
|
(–) 505-580 |
|
|
Дегидратация |
|||
Бёмит |
α-AlO(OH) |
|
|
(–) 460-580 |
|
|
Дегидратация |
|||
|
α-Al(OH)3 |
|
|
|
|
|
И |
|
||
Гиббсит |
|
|
(–) |
250-300 |
|
Образование белита |
||||
|
|
|
|
|
(–) 320-330 |
|
|
Превращение α→æAl2O3 |
||
|
|
|
|
|
(+) 950 |
|
|
Полиморфное превращение |
||
|
|
|
|
|
|
Д |
|
|
|
|
Байерит |
β-Al2O3·3H2O |
|
|
(–) 250-300 |
|
|
Дегидратация |
|||
Гидроаргиллит |
|
|
|
|
(–) |
310-315 |
|
егидратация |
||
|
|
|
|
|
А |
|
|
Разложение бемита |
||
|
|
|
|
|
(–) |
500-550 |
|
|||
|
|
|
|
|
(+) 800 |
|
|
Переход γ-Al2O3 → θ-Al2O3 |
||
Гётит |
FeO(OH) |
|
|
(–) 300-380 |
|
|
Дегидратация (10 % H2O) |
|||
Лимонит |
|
б |
(–) 120-140 |
|
|
Потеря |
гигроскопической |
|||
β-Fe2O3·H2O |
|
|
|
|
||||||
|
или β-FeO(OH) |
|
|
|
|
воды |
|
|||
|
и |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(–) |
250 |
|
|
Дегидратация |
|
С |
|
|
|
(–) |
300 |
|
|
|
|
|
|
|
|
(+) 450 |
|
|
Переход γ-Fe2O3 → |
||||
|
|
|
|
|
|
|
|
|
α-Fe2O3 |
|
Лепидокрокит γ-Fe2O3·H2O |
|
|
(–) 304-380 |
|
|
Дегидратация |
||||
|
или γ-FeO(OH) |
(+) 450-500 |
|
|
Переход γ-Fe2O3 → |
|||||
|
|
|
|
|
|
|
|
|
α-Fe2O3 |
|
Гелеобразные Fe2O3·nH2O |
|
|
(–) 250-300 |
|
|
Дегидратация |
||||
окислы железа |
|
|
|
|
(+) 350-400 |
|
|
Окисление |
|
|
Вюстит |
FeO |
|
|
|
(+) 295-300 |
|
|
Окисление FeO до Fe2O3 |
||
Гематит |
α-Fe2O3 |
|
|
|
Не имеет эффектов |
|
||||
Маггемит |
γ-Fe2O3 |
|
|
|
(+) 450-500 |
|
|
Переход γ-Fe2O3 → |
||
|
|
|
|
|
|
|
|
|
α-Fe2O3 |
|
Магнетит |
Fe3O4 |
|
|
|
(+) 275-400 |
|
|
Переход Fe3O4 → γ-Fe2O3 |
||
|
|
|
|
|
(+) 590-1000 |
Переход γ-Fe2O3 → |
||||
|
|
|
|
|
|
|
|
|
α-Fe2O3 |
|
Гидрогематит |
Fe2O3-aq |
|
|
(–) |
120-140 |
|
|
Дегидратация |
||
|
|
|
|
|
(–) |
340 |
|
|
|
|
30

|
|
|
|
|
|
|
|
Продолжение табл. 2 |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
2 |
|
|
3 |
|
4 |
|
|
Гидроталькит |
MgCO3· |
|
|
(–) 200-285 |
|
Потеря 4H2O |
|
||
|
|
·5Mg(OH)2· |
|
(–) 350-400 |
|
Дегидратация Al(OH)3 |
|||
|
|
·2Al(OH)3· |
|
(–) 450-540 |
|
Дегидратация Mg(OH)2 |
|||
|
|
·4H2O |
|
|
|
|
|
и диссоциация MgCO3 |
|
Пироаурит |
|
MgCO3· |
|
|
(–) 215-270 |
|
Потеря 4H2O |
|
|
|
|
·5Mg(OH)2· |
|
(–) 350-400 |
|
Дегидратация Fe(OH)3 |
|||
|
|
·2Fe(OH)3· |
|
(–) 450-540 |
|
Дегидратация Mg(OH)2 |
|||
|
|
·4H2O |
|
|
|
|
|
и диссоциация MgCO3 |
|
Двуокись крем- |
SiO2 |
|
|
(+) 115-117 |
|
Превращение |
тридимита |
||
ния |
|
|
|
|
|
|
|
α1→β1 |
|
|
|
|
|
|
(+) 166-163 |
|
α2→β2 |
|
|
|
|
|
|
|
(+) 220-280 |
|
Превращение |
кристобалита |
|
|
|
|
|
|
|
|
|
И |
|
|
|
|
|
|
|
|
|
α→β |
|
|
|
|
|
|
(–) 573 |
|
Превращение кварца α→β |
||
Двуводный гипс |
CaSO4·2H2O |
|
(–) 100-120 |
|
Потеря адсорбционной во- |
||||
|
|
|
|
|
|
Д |
ды |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(–) 220 |
|
Потеря 0,5H2O |
|
|
|
|
|
|
|
А |
|
Потеря 0,5H2O |
|
|
|
|
|
|
|
(–) 240 |
|
|
||
|
|
|
|
|
(–) 380-420 |
|
Инверсия CaSO4 |
||
|
|
|
|
|
(–)1180-1200 |
Полиморфное превращение |
|||
Ангидрит |
|
CaSO4 |
б |
(–) 1190 |
|
Полиморфное превращение |
|||
Полуводный |
|
α-CaSO4·0,5H2O |
(–) |
160 |
|
Дегидратация примеси (по- |
|||
гипс |
|
и |
|
|
|
|
теря 0,5H2O) |
|
|
|
С |
|
|
(+) 380 |
|
Инверсия ангидрита |
|||
|
|
|
|
|
(–) 1180-1200 |
Полиморфное превращение |
|||
Полуводный |
|
β-CaSO4·0,5H2O |
(–) 120 |
|
Дегидратация примеси |
||||
гипс |
|
|
|
|
(–) 180 |
|
То же |
|
|
|
|
|
|
|
(–) 240 |
|
Потеря 0,5H2O |
|
|
|
|
|
|
|
(+) 410 |
|
Инверсия ангидрита |
||
|
|
|
|
|
(–) 1180-1200 |
Полиморфное превращение |
|||
Эстрихгипс |
CaSO4·nCaO |
|
|
|
Не |
имеет эффектов |
|
||
Эпсомит |
|
MgSO4·7H2O |
|
(–) 52-58 |
|
Инконгруэнтное плавление |
|||
|
|
|
|
|
(–) |
85-96 |
|
То же |
|
|
|
|
|
|
(–) |
105-110 |
|
Выкипание раствора |
|
|
|
|
|
|
(–) |
125-150 |
Дегидратация |
|
|
|
|
|
|
|
(–) |
185-195 |
|
Дегидратация |
до одновод- |
|
|
|
|
|
|
|
|
ной соли |
|
|
|
|
|
|
(–) |
320-370 |
|
Полная дегидратация |
|
Барит |
|
BaSO4 |
|
|
(–) 1150 |
|
Полиморфное превращение |
||
Целестин |
|
SrSO4 |
|
|
(–) 1145 |
|
Полиморфное превращение |
||
Тенардит |
|
NaSO4 |
|
|
(–) 240 |
|
Полиморфное превращение |
||
|
|
|
|
|
(–) |
884 |
|
Плавление |
|
31

|
|
|
|
|
|
|
|
Продолжение табл. 2 |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
2 |
|
|
3 |
|
4 |
|
Арканит |
|
K2SO4 |
|
|
(–) 583 |
|
Полиморфное превращение |
||
Глазерит |
|
Na2SO4·3K2SO4 |
|
(–) 437 |
|
Полиморфное превращение |
|||
Алунит |
|
K2SO4· |
|
|
(–) 940 |
|
Плавление |
|
|
|
|
·Al2(SO4)3· |
|
(–) |
490-550 |
|
Дегидратация |
|
|
|
|
·4Al(OH)3 |
|
|
|
||||
|
|
|
|
|
(–) |
740-760 |
|
Полиморфное превращение |
|
|
|
|
|
|
(–) |
770-810 |
|
Разложение сульфатов |
|
Анкерит |
|
(Mg,Fe)CO3· |
|
(–) 730 |
|
Диссоциация MgCO3 |
|||
|
|
·CaCO3 |
|
|
(–) 810 |
|
Диссоциация FeCO3 |
||
|
|
|
|
|
(–) 900 |
|
Диссциация CaCO3 |
||
Аллофан |
|
mAl2O3·nSiO2· |
|
(–) 110-150 |
|
Дегидратация |
|
||
|
|
·pH2O |
|
|
(+) 920-1000 |
Перекристаллизация |
|||
|
|
|
|
|
|
|
|
И |
|
|
|
|
|
|
|
|
|
аморфного вещества |
|
Каолинит |
|
Al2O3·2SiO2· |
|
(–) 550-610 |
|
Дегидратация |
|
||
|
|
·4H2O |
|
|
(+) 925-1000 |
Кристаллизация |
аморфных |
||
|
|
|
|
|
|
|
|
продуктов |
|
|
|
|
|
|
(+) 1200 |
|
Образование |
кристобалита |
|
|
|
|
|
|
|
|
|
α-Al2O3 |
|
|
|
|
|
|
А |
|
|
|
|
Галлуазит |
|
Al2O3·2SiO2· |
|
(–) 100-120 |
|
Адсорбционная вода |
|||
|
|
·4H2O |
|
|
(–) 450-500 |
|
егидратация |
|
|
|
|
|
б |
|
|
|
|
||
|
|
|
|
|
(+) 925Д-1000 |
Кристаллизация |
аморфных |
||
|
|
|
|
|
|
|
|
продуктов |
|
Монтморилло- |
и |
|
(–) 150-175 |
|
Адсорбционная вода |
||||
Al2O3·4SiO2· |
|
|
|||||||
нит |
|
·nH2O |
|
|
(–) 500-700 |
|
Дегидратация |
|
|
|
С |
|
|
(–) |
800-900 |
|
То же |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
(–) |
915-1000 |
Кристаллизация |
аморфных |
|
|
|
|
|
|
|
|
|
продуктов |
|
Мусковит |
|
K2O·3Al2O3· |
|
(–) 125 |
|
Адсорбционная вода |
|||
|
|
·6SiO2·2H2O |
|
(–) 450-650 |
|
Дегидратация |
|
||
|
|
|
|
|
(–) |
850-900 |
|
Разрушение решетки |
|
Биотит |
|
K2O·6(Mg,Fe)O |
(–) |
1100- |
|
Разрушение решетки |
|||
|
|
·3Al2O3·6SiO2· |
1200 |
|
|
|
|||
|
|
·2H2O |
|
|
|
|
|
|
|
Гидробиотит |
K2O·6(Mg,Fe)O |
(–) 160-180 |
|
Дегидратация |
|
||||
|
|
·3Al2O3·6SiO2· |
|
(–) 220-250 |
|
То же |
|
||
|
|
·nH2O |
гидро- |
(–) 800-1000 |
|
Разрушение решетки |
|||
|
|
Группа |
|
|
|
|
|
||
|
|
слюд |
|
|
|
|
|
|
|
Вермикулит |
|
Группа |
гидро- |
(–) |
120-170 |
|
Дегидратация |
|
|
|
|
слюд |
|
|
(–) |
270-300 |
|
То же |
|
|
|
|
|
|
(–) |
860 |
|
Разрушение решетки |
|
32

|
|
|
|
|
|
|
|
|
Продолжение табл. 2 |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
2 |
|
|
|
|
|
3 |
|
4 |
|
|
|
|
Глауконит |
|
Группа |
гидро- |
(–) |
|
130-170 |
Дегидратация |
|
|
|
|
|
||
|
|
слюд |
|
|
|
(–) |
|
550-600 |
То же |
|
|
|
|
|
Иллит |
|
Группа |
гидро- |
(–) 120-150 |
Адсорбционная вода |
|
||||||||
|
|
слюд |
|
|
|
(–) |
|
500-600 |
Дегидратация |
|
|
|
|
|
|
|
|
|
|
|
(–) |
|
900 |
Разрушение решетки |
|
||||
|
|
|
|
|
|
(+) 935 |
Кристаллизация |
шпинели, |
|
|||||
|
|
|
|
|
|
|
|
|
периклаза |
|
|
|
|
|
Боксит |
|
Группа |
мине- |
(–) |
|
285-310 |
Дегидратация |
гидроаргил- |
|
|
||||
|
|
ралов |
|
|
|
|
|
|
лита |
|
|
|
|
|
Змеевик (сер- |
|
3MgO·2SiO2· |
(–) 130-170 |
Дегидратация |
|
|
|
|
|
|||||
пентин) |
|
·2H2O |
|
|
|
(–) 650-730 |
То же |
|
|
|
|
|
||
|
|
|
|
|
|
(+) 800-830 |
Разрушение решетки |
|
|
|||||
Хризотил-асбест |
Mg6[Si4O11]· |
(–) |
|
до 100 |
Потеря адсорбционной воды |
|
|
|||||||
|
|
·(OH)6·H2O |
|
(–) 660-765 |
Удаление конституционной |
|
|
|||||||
|
|
|
|
|
|
|
|
|
воды |
|
|
|
|
|
|
|
|
|
|
|
(+) 800-830 |
Кристаллизация новой фазы |
|
|
|||||
Тальк |
|
3MgO·4SiO2· |
(–) |
|
850-950 |
егидратация |
|
|
|
|
|
|||
|
|
|
|
|
|
|
||||||||
|
|
· H2O |
|
|
|
А |
И |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
б |
Д |
|
|
|
|
|
|||||
Трехкальциевый |
3CaO·2SiO |
2 |
(–) |
|
|
|
|
|
|
|||||
|
|
|
920-925 |
Полиморфное превращение |
|
|||||||||
силикат |
|
|
|
|
|
(–) |
|
970-980 |
То же |
|
|
|
|
|
|
|
|
|
|
|
(–) |
|
990-100 |
То же |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С |
|
|
2 |
|
|
|
|
|
|
|
|
|
Двухкальцие- |
|
γ-2CaO·SiO2 |
(–) 780-830 |
Переход γ-C2S→γ’C2S |
|
|||||||||
вый силикат |
|
и |
|
|
|
|||||||||
|
(–) 1447 |
Переход γ’-C2S→γC2S |
|
|||||||||||
Алит |
|
54CaO·16SiO2· |
(–) 835 |
Полиморфное превращение |
|
|||||||||
|
|
·Al2O3·MgO |
(–) 1427 |
То же |
|
|
|
|
|
|||||
Ксонотлит |
|
5CaO·5SiO · |
(–) 800-880 |
Дегидратация до воластонита |
|
|||||||||
|
|
·2H2O |
|
|
|
|
|
|
|
|
|
|
|
|
Гиролит |
|
2CaO·3SiO2· |
(–) 70-150 |
Дегидратация |
|
|
|
|
|
|||||
|
|
·2H2O |
|
|
|
(–) 700-780 |
Дегидратация и образование |
|
||||||
|
|
|
|
|
|
|
|
|
воластонита |
|
|
|
|
|
|
|
|
|
|
|
|
(+) 800 |
Кристаллизация |
|
|
|
|
|
|
Тоберморит |
|
4CaO·5SiO2· |
(–) 250-280 |
Дегидратация |
|
|
|
|
|
|||||
|
|
·5H2O |
|
|
|
(–) 780-800 |
То же |
|
|
|
|
|
||
Гидросиликат |
|
CaO·SiO2·H2O |
(+) 800-830 |
Кристаллизация CS |
|
|||||||||
кальция |
|
(CSH-B) |
|
|
|
|
|
|
|
|
|
|
|
|
33

|
|
|
|
|
|
|
Продолжение табл. 2 |
|
|
|
|
|
|
|
|
|
|
1 |
2 |
|
|
|
3 |
|
4 |
|
То же |
CaO·SiO2·H2O |
|
Нет |
отчетли- |
|
|
||
|
(CSH-A) |
|
вых эффектов |
|
|
|
||
- // - |
CaO·SiO2·H2O |
|
(–) 400-410 |
|
Дегидратация |
|
||
|
(CSH-A) |
|
(–) 450-540 |
|
То же |
|
||
- // - (гиллебран- |
CaO·SiO2·H2O |
|
(-400-410) |
|
Дегидратация |
|
||
дит |
(CSH-B) |
|
|
|
|
|
|
|
То же |
CSH-C |
|
|
(–) 720-800 |
|
Дегидратация |
|
|
- // - |
C2SH2 |
|
|
(–) |
110-120 |
|
- // - |
|
|
|
|
|
(–) |
480-520 |
|
- // - |
|
- // - |
C3SH2 |
|
|
(–) 500-600 |
|
Потеря 1 молкулы H2O |
||
|
|
|
|
(–) |
700-800 |
|
Полная дегидратация |
|
Гидроалюминат |
CaO·Al2O3· |
|
(–) 155 |
|
Ступенчатая дегидратация |
|||
кальция |
·10H2O |
|
|
(–) 285 |
|
И |
|
|
Гидроалюминат |
CaO·Al2O3· |
|
(+) 545 |
|
Кристаллизация |
безводных |
||
кальция |
·10H2O |
|
|
(+) 930 |
|
фаз |
|
|
|
2CaO·Al2O3· |
|
|
Д |
|
|
||
То же |
|
(–) 70-100 |
|
Потеря гигроскопической |
||||
|
·8H2O |
|
|
|
|
|
воды |
|
|
|
|
|
А |
|
Ступенчатая дегидратация |
||
|
|
|
|
(–) |
150-200 |
|
||
|
|
|
|
(–) |
250-300 |
|
|
|
То же |
3CaO·Al2O3· |
|
(–) 340 |
|
Потеря 4,5H2O |
|
||
|
|
б |
|
|
Потеря 1,5H2O и дегидрата- |
|||
|
·6H2O |
|
|
(–) 500-550 |
|
|||
|
|
|
|
|
|
|
ция Ca(OH)2 |
|
|
и |
|
|
|
|
|
|
|
То же |
4CaO·Al2O3· |
|
(–) 140-170 |
|
Ступенчатая дегидратация |
|||
|
·14H2O |
|
|
(–) 180-220 |
|
|
|
|
С |
|
|
|
|
|
|
|
|
|
|
|
|
(–) |
300 |
|
|
|
Гидросульфоа- |
3CaO·Al2O3· |
|
(–) 100-170 |
|
Частичная дегидратация |
|||
люминат каль- |
·CaSO4·12H2O |
|
(–) 200-250 |
|
Потеря большей части воды |
|||
ция (низкосуль- |
|
|
|
(–) |
300-320 |
|
Дегидратация |
|
фатная форма) |
|
|
|
(–) |
500 |
|
- // - |
|
|
|
|
|
(+) 800 |
|
Кристаллизация |
аморфной |
|
|
|
|
|
|
|
|
безводной фазы |
|
|
|
|
|
|
|
|||
Гидросульфоа- |
3CaO·3Al2O3· |
|
(–) 100-170 |
|
Потеря большей части воды |
|||
люминат каль- |
·CaSO4·31H2O |
|
(–) 250-300 |
|
Полная дегидратация |
|||
ция (высоко- |
|
|
|
|
|
|
|
|
сульфатная |
|
|
|
|
|
|
|
|
форма) |
|
|
|
|
|
|
|
|
Гидрохлоралю- |
3CaO·Al2O3· |
|
(–) 100 |
|
Ступенчатая дегидратация |
|||
минат кальция |
·CaCl2·12H2O |
|
(–) 180-200 |
|
вторая ступень |
|
||
|
|
|
|
(–) |
450 |
|
третья ступень |
|
|
|
|
|
(–) |
530-550 |
|
четвертая ступень |
|
34

|
|
|
|
|
|
|
|
|
Окончание табл. 2 |
|||
1 |
|
|
|
2 |
|
|
3 |
|
|
4 |
|
|
Карбоалюминат |
|
|
3CaO·Al2O3· |
(–) 180 |
|
То же |
|
|
|
|||
кальция |
|
|
|
·CaCl2·12H2O |
(–) 230 |
|
|
|
|
|
||
|
|
|
|
|
|
(–) |
450-520 |
|
То же |
|
|
|
Гидроалюминат |
|
|
3CaO·3Al2O3· |
(–) 700-800 |
|
Полная дегидратация |
|
|
||||
кальция |
|
|
|
·12H2O |
|
|
|
|
|
|
|
|
Гидрогранат |
|
|
|
3CaO·3Al2O3· |
(–) 450-520 |
|
То же |
|
|
|
||
|
|
|
|
хSiO2·у12H2O |
|
|
|
|
|
|
|
|
|
|
|
|
(у+х=6) |
|
|
|
|
|
|
|
|
Гидросиликат |
|
|
Na2O·SiO2·6H2O |
(–) |
63 |
|
Инконгруэнтное плавление |
|
|
|||
кальция (жид- |
|
|
|
|
(–) |
95 |
|
Ступенчатая дегидратация |
|
|
||
кое стекло) |
|
|
|
|
|
(–) |
170 |
|
|
|
|
|
|
|
|
|
|
|
(–) |
1083 |
|
Плавление безводной соли |
|
|
|
|
|
|
|
|
|
|
|
И |
Таблица 3 |
|||
|
|
|
|
Определитель минералов (по Бергу) |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Температура |
|
|
|
|
|
|
|
|
|
|
|
|
эффекта, °С |
|
|
|
|
|
|
Минералы |
|
|
|
||
100-115 |
|
|
Гипс, алюминит |
|
|
|
|
|
|
|
||
120-140 |
|
|
Алюминит, вермикулит, галлуазит, гидрогематит, змеевик, лимонит, |
|||||||||
|
|
|
метагаллуазит, сепиолит |
|
|
|
|
|
||||
150-200 |
|
|
Аллофан (вермикулит), гидробиотит,гидромусковит, гипс, глау- |
|||||||||
|
|
|
|
|
б |
|
|
|
|
|
|
|
|
|
|
конит, змеевик, монтмориллонитД, алюминит |
|
|
|
||||||
220-300 |
|
|
Боксит, вермикулит, гидробиотит, гидраргиллит, манганит, кон- |
|||||||||
|
|
|
|
и |
|
|
|
|
|
|
|
|
|
|
|
тронит, сингенит |
|
|
|
|
|
|
|
||
|
|
|
А |
|||||||||
310-400 |
|
|
Бейдел т, верм кулит, гетит, гидромагнезит, гипс (экз.), манганит |
|||||||||
|
|
|
(экз.), пол гал т, сапонит, сидерит |
|
|
|
||||||
|
С |
|
|
|
|
|
|
|
|
|||
400-450 |
|
|
Анальц м, арагон т, брусит, гидромагнезит, натролит, сидерит |
|||||||||
460-500 |
|
|
Алун т, мусков т, родохрозит |
|
|
|
|
|
||||
505-550 |
|
|
Алунит, боксит, гидромагнезит (экз.), глабуретит, диаспор, |
|||||||||
|
|
|
манганит (мусковит), нонтронит |
|
|
|
||||||
555-600 |
|
|
Боксит, бейделит, галлуазит, гидромагнезит, глауконит, каоли- |
|||||||||
|
|
|
нит, кварц, магнезит, метагаллуазит, пиролюзит, родохровит, _апонит |
|||||||||
600-650 |
|
|
Аноксит (галлуазит), гидромусковит (мусковит), накрит (пиролюзит) |
|||||||||
650-700 |
|
|
Дикит, змеевик, монтмориллонит (накрит) |
|
|
|
||||||
700-750 |
|
|
Алунит, анкерит, доломит (змеевик), пирофиллит, родохрозит (экз.) |
|||||||||
750-800 |
|
|
Алунит, нонтронит (экз.), пирофиллит |
|
|
|
||||||
800-850 |
|
|
Анкерит, алюминит, змеевик (экз.), сепиолит |
|
|
|
||||||
850-900 |
|
|
Кальцит, анкерит, доломит, алюминит, арагонит, монтморилло- |
|||||||||
|
|
|
нит, мусковит, серицит, тальк, ксенотлит |
|
|
|
||||||
900-950 |
|
|
Браунит, нонтронит (экз.), парагонит, лепидолит (тальк) |
|||||||||
950-1000 |
|
|
Аноксит (экз.), боксит (экз.). галлуаэит (экз.), дикит (экз.), као- |
|||||||||
|
|
|
линит (экз.), манганит, метагаллуазит (экз.), монтмориллонит (экз.), |
|||||||||
|
|
|
накрит (экз.), пиролюзит, аллофан (экз.) |
|
|
|
||||||
1000-1200 Биотит, гаусманит, гидромусковит, манганит, парагонит, флогопит,
пиролюзит, серицит, стронцианит
Примечание. Экз. – экзотермический эффект.
35
