
Облегчённая диффузия
Для облегчённой диффузии веществ (рис. 2–3) необходимы встроенные в мембрану белковые компоненты (поры,переносчики,каналы). Все эти компоненты относятся к интегральным (трансмембранным) белкам. Облегчённая диффузия происходит по градиенту концентрации для неполярных веществ или по электрохимическому градиенту для полярных веществ (уравнение 2–3).
· Поры. По определению, заполненный водойканалпорывсегдаоткрыт(рис. 2–4). Поры формируют разные белки (порины, перфорины, аквапорины, коннексины и др.). В некоторых случаях образуются гигантские комплексы (например, ядерные поры), состоящие из множества разных белков.
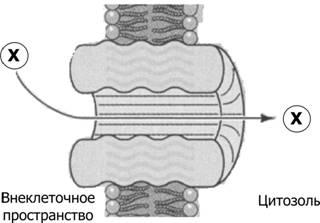
Рис.2–4.Поравплазмолемме[2].
Канал поры всегда открыт, поэтому химическое вещество Х проходит через мембрану по градиенту его концентрации или (если вещество Х заряжено) по электрохимическому градиенту. В данном случае происходит перемещение вещества Х из внеклеточного пространства в цитозоль.
Пориныформируют в наружной мембране митохондрий каналы, через которые из цитозоля в межмембранное пространство митохондрий диффундируют вещества с молекулярной массой до 5 кД.
Аквапорины(AQP) — семейство мембранных пор для воды (рис. 2–5). Идентифицировано 10 аквапоринов, AQP3, AQP7 и AQP9 дополнительно проницаемы для глицерола и других небольших молекул, а AQP0, AQP1, AQP2, AQP4, AQP5 — только для воды.
Перфорины— белки гранул цитотоксических Т-лимфоцитов и NK‑клеток, образуют в клетках–мишенях, подлежащих уничтожению (клетки трансформированные, инфицированные вирусами и чужеродные), трансмембранные каналы. Выделяемые T-киллером молекулы перфорина полимеризуютcя в мембране клетки–мишени в приcутcтвии Ca2+. Сформированные в плазматической мембране клетки–мишени перфориновые поры диаметром около 10 нм пропуcкают воду и cоли, но не молекулы белка. В результате осмотического шока клетка–мишень лизируется. Аналогично образуются поры, сформированные молекулами компонента комплемента C9.
Ядернаяпораимеет диаметр 80–150 нм, содержит канал поры и комплекс ядерной поры. Содержимое ядра сообщается с цитозолем через 2–4 тыс. специализированных коммуникаций — ядерных пор, осуществляющих диффузию воды, ионов и транспорт множества макромолекул (в т.ч. молекул РНК) между ядром и цитоплазмой. Перенос макромолекул через ядерные поры осуществляют специальные транспортные белки — кариоферины, которые специфически распознают и связывают «свои» молекулы и курсируют между ядром и цитоплазмой, перенося связанную молекулу в одном направлении: из цитоплазмы в ядро (импортины) или из ядра в цитоплазму (экспортины).
Коннексон— трансмембранный белок цилиндрической конфигурации; состоит из 6 СЕ коннексина. Два коннексона соседних клеток соединяются в межмембранном пространстве и образуют канал между клетками (см. рис. 4‑7). Канал коннексона диаметром 1,5 нм пропускает ионы и молекулы с Mrдо 1,5 кД. В отличие от других трансмембранных пор коннексоны имеют 2 состояния: открытое и закрытое. Коннексоны соседних клеток образуют так называемый щелевой контакт (см. подраздел «Коммуникационные контакты» в разделе «Специализированные межклеточные контакты» главы 4).
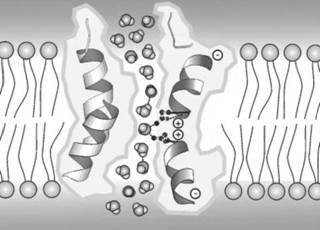
Рис.2–5.Сформированнаяаквапоринамиводнаяпоравплазмолемме.
Через канал поры проходит множество молекул воды.
· Переносчики(транспортёры) осуществляют транспорт через биологические мембраны множества различных ионов (Na+, Cl–, H+, HCO3–и др.) и органических веществ (глюкоза, аминокислоты, креатин, норадреналин, фолаты, лактат, пируват и др.). Транспортёрыспецифичны: каждый конкретный переносчик переносит через липидный бислой, как правило и по преимуществу, одно вещество. Различают однонаправленный (унипорт), сочетанный (симпорт) и разнонаправленный (антипорт) транспорт (рис. 2–6).
Унипорт— однонаправленный транспорт одного вещества (рис. 2–6).
Симпорт(котранспорт). Некоторые переносчики осуществляют однонаправленный сочетанный транспорт одного вещества (рис. 2–6).
Антипорт(обменник). Эти переносчики осуществляют разнонаправленный транспорт двух разных веществ (встречный транспорт, рис. 2–6).
Вторичныйактивныйтранспорт. Переносчики, реализующие как сочетанный (симпорт), так и разнонаправленный (антипорт) трансмембранный перенос с точки зрения энергетических затрат функционируют так, что энергия, накапливающаяся при переносе одного вещества (обычно Na+), затрачивается на транспорт другого вещества. Такой тип трансмембранного переноса называют вторичным активным транспортом (см. ниже).
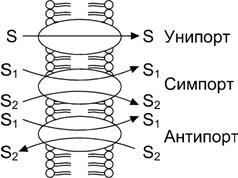
Рис.2–6.Модельвариантовтрансмембранногопереносаразныхмолекул[9]
Кинетикапереноса(рис. 2–7, см. также рис. 2–3Б), как и скорость ферментной реакции, описывается уравнением Михаэлиса–Ментена, но вместо скорости ферментной реакции подставлено значение J (величина трансмембранного переноса):
Уравнение2–4
JX= ([X]Jмакс) ¸ (Km+X)
где Х — транспортируемое вещество, JX— величина транспорта вещества Х, Jмакс— максимальная величина транспорта, Km— константа Михаэлиса (численно равна концентрации вещества Х, когда JXсоставляет половину Jмакс).
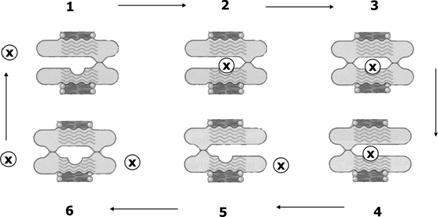
Рис.2–7.МодельвзаимодействияпереносчикаитранспортируемоймолекулыХ[2].
Белки переносчика формируют канал, на внутренней поверхности которого имеется участок связывания молекулы Х (выемка). Диффузия молекул Х через мембрану в принципе может происходить в обеих направлениях, направление определяется концентрационным или электрохимическим трансмембранным градиентом для вещества Х. На рисунке показаны этапы (1–6) переноса молекулы Х слева (межклеточная среда) направо (цитозоль). Канал переносчика может находиться в открытом наружу (1, 2), внутрь клетки (4, 5) или закрытом (3, 6) состоянии.
Примерытрансмембранныхпереносчиков
Глюкоза
Унипортыглюкозы GLUT (от англ. GLUcose Transporter) — интегральные гликопротеины. Клетки, имеющие значительную потребность в глюкозе (в первую очередь нейроны ЦНС), содержат переносчик глюкозы. Инсулин увеличивает захват глюкозы клетками, вызывая быстрое перемещение переносчиков из цитоплазмы клетки в плазмолемму. В кардиомиоцитах экспрессию генаGLUT4усиливают йодсодержащие гормоны щитовидной железы. GLUT5 щёточной каёмки энтероцитов тонкого кишечника обеспечивает всасывание глюкозы (также фруктозы), а GLUT2 базолатеральной части энтероцитов осуществляет выход этих сахаров из энтероцитов во внутреннюю среду организма. Точечная мутация генаGLUT2(замена валина на изолейцин в позиции 197) — одна из причин развития сахарного диабета типа II.
Симпорт. Сочетанный транспорт глюкозы и Na+в тонком кишечнике и канальцах почки обеспечивают мембранные гликопротеины, кодируемые генамиSGLT. Этоглавныймеханизмпочечнойреабсорбцииглюкозы, происходящей в начальном отделе проксимальных извитых канальцев нефрона. Известно несколько мутаций генаSGLT2, приводящих к потере глюкозы (глюкозурия) в почках (до 60 г/сут).
Аминокислоты
Всасывание аминокислот в кишечнике, их реабсорбция в канальцах нефрона, а также поглощение аминокислот–нейромедиаторов нейронами и глиоцитами мозга реализуются при помощи переносчиков, кодируемых генами SLC1иSLC3. Идентифицированы десятки переносчиков, специфичных по отношению к a-, двухосновным и нейтральным аминокислотам.
Цистинурия. Мутации генаSLC3A1приводят в почечных канальцах к избыточной секреции цистина (при некоторых формах также лизина, аргинина и орнитина) и к образованию мочевых камней.
Глутаматиаспартат(аминокислоты–нейромедиаторы), накапливаясь в межклеточном пространстве ЦНС, могут оказыватьцитотоксическийэффект. Кодируемый геномSLC1A2белок–переносчик транспортирует эти аминокислоты в цитоплазму нейронов и глиоцитов.
Анионообменники— регуляторы внутриклеточного pH, осуществляютобменCl–набикарбонат.
«Полоса3мембраныэритроцитов»— многофункциональный транспортный белок глюкозы, анионов и воды.
Респираторный обмен CO2. Этот анионообменник обеспечивает эффективный обмен Cl–на HCO3–: поступление бикарбоната в эритроциты в обмен на Cl–в капиллярах разных органов, обратный процесс происходит в капиллярах лёгкого.
Аг старения клеток. При деградации этого белка образуется т.н. Аг старения клеток — метка, распознаваемая иммунной системой. Эритроциты, несущие эту метку (повреждённые, заканчивающие жизненный цикл, инфицированные плазмодиями малярии), распознаются макрофагами селезёнки и печени и фагоцитируются ими.
Фосфаты. Реабсорбция фосфатов происходит в проксимальных извитых канальцах нефрона при помощи переносчиков фосфатов.
ОбменNa+наH+. ГеныSLC9Aкодируют белки плазмолеммы NHE (отNa, H, Exchanger [обменник]),осуществляющиеобменвнеклеточногоNa+навнутриклеточныйH+. Мембранные белки NHE — регуляторы внутриклеточного pH. Диуретик амилорид ингибирует NHE1, NHE2 и NHE4 и не оказывает эффекта на NHE3 и NHE5.
Разныепереносчики
Креатин. Кардиомиоциты и скелетные МВ не синтезируют креатина, необходимого для энергетического обеспечения их функции. Ингибирование переносчика креатина ведёт к развитию мышечной слабости. Дефекты кодирующего переносчик генаSLC6A8— причина одной из форм кардиомиопатии.
Фолаты. Этот переносчик обнаружен в плаценте и печени.
Лактатипируваттранспортируются в обоих направлениях через плазмолемму эритроцитов, гепатоцитов, эпителия кишечника и почки, клеток мышечных тканей.
Норадреналин. Выделившиеся в синаптическую щель нейромедиаторы частично транспортируются обратно в пресинаптические терминали.Трициклическиеантидепрессанты(например, дезипрамин, имипрамин), а такжекокаиниамфетаминывзаимодействуют с синаптическими транспортными системами биогенных аминов. Мутации генов, кодирующих переносчики норадреналина исеротонина, могут привести к развитию психиатрической патологии (например, маниакально–депрессивного психоза).
·Ионныеканалысостоят из связанных между собой белковых СЕ, формирующих в мембране гидрофильную пору (рис. 2–8). Через открытую пору по электрохимическому градиенту диффундируют ионы. Свойства ионных каналов (в том числе специфичность и проводимость) определяют как аминокислотная последовательность конкретного полипептида, так и конформационные изменения, происходящие с разными частями полипептидов в составе интегрального белка канала (рис. 2–10).
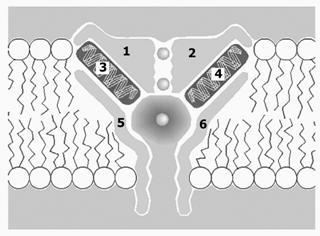
Рис.2–8.Моделькалиевогоканала. Интегральный белок (на рисунке цифрами помечены фрагменты белка) пронизывает всю толщу липидного бислоя, формируя заполненную водой пору канала (на рисунке в канале видны 3 иона калия, нижний из ионов находится в полости поры).

Рис.2–9.Модельворотногомеханизмаионногоканала[2].А. Ворота канала закрыты, ион Х не может пройти через мембрану.Б. Ворота канала открыты, ионы Х проходят через мембрану по поре канала.

Рис.2–10.Потенциалозависимыйнатриевыйканал[4]. Двумерная модель канала (А), выделенная часть в увеличенном виде представлена на Б.А. Модель предусматривает наличие 4 доменов (I–IV), каждый из которых состоит из 6 трансмембранных a-спиралей белка. a-Спирали домена IV — чувствительный к изменениям мембранного потенциала a-спиралисенсор: перемещения в плоскости мембраны этих a-спиралей (конформации) приводят к активации (открытию) канала. Внутриклеточная петля между доменами III и IV функционируют как закрывающийворотныймеханизм: после деполяризации мембраны эта петля смещается к поре канала, закрывает её и тем самым прекращает трансмембранную ионную проводимость.Б, Домен IV. Часть внеклеточной петли между a-спиралями 5 и 6 погружена в мембрану и участвует в определение специфичности канала для ионов (избирательныйфильтр).
Специфичность. Ионные каналы специфичны (селективны) по отношению к конкретным катионам и анионам (например, для Na+[натриевый канал], K+[калиевый канал], Ca2+[кальциевый канал], Cl–[хлорный канал] и др.). См. рис. 2–10Б.
Проводимостьопределяется количеством ионов, способных пройти через канал в единицу времени. Проводимость канала изменяется в зависимости от того, открыт канал или закрыт.
Ворота. Канал может находиться либо в открытом, либо в закрытом состоянии (рис. 2–9). Поэтому модель канала предусматривает наличие устройства, открывающего и закрывающего канал — воротный механизм, или ворота канала (по аналогии с открытыми и закрытыми воротами). См. рис. 2–10А.
Функциональныекомпоненты. Помимо ворот, модель ионного канала предусматривает существование таких функциональных компонентов, как сенсор, избирательный фильтр и пора открытого канала.
Сенсор. Каждый канал имеет один (иногда больше) сенсоров к разным типам сигналов: изменениям мембранного потенциала (МП), вторым посредникам (с цитоплазматической стороны мембраны), разным лигандам (с внеклеточной стороны мембраны). Эти сигналы регулируют переход между открытым и закрытым состоянием канала.
Классификацияканаловпо чувствительности к разным сигналам. По этому признаку каналы подразделяют на потенциалозависимые, механочувствительные, рецептор–зависимые, G‑белок–зависимые, Са2+–зависимые.
Потенциалозависимыеионные каналы управляются мембранным потенциалом (МП). Колебания МП приводят к конформационным изменениям белковой структуры канала, что и переводит канал в открытое либо закрытое состояние. Благодаря наличию потенциалозависимых Na+‑каналов в возбудимых структурах (например, плазмолемма мышечных клеток и аксолемма нервных клеток) происходит генерация и распространение потенциала действия (ПД).
Лиганд–зависимыеионные каналы (хемоуправляемые каналы: рецептор–зависимые и G‑белок–зависимые) имеют прямое отношение к мембранным рецепторам. Соединение лиганда с рецептором вызывает конформационные изменения в канале, изменяющие его функциональное состояние. Лиганд–зависимые каналы не столь избирательны, как потенциалозависимые и, будучи в открытом состоянии, пропускают несколько разных, но одинаково заряженных ионов. Например, связываниеацетилхолинас никотиновым рецептором ацетилхолина на мембране скелетной мышцы активирует рецептор ацетилхолина (рецептор сам по себе является лиганд–зависимым ионным каналом), который в физиологических условиях проводит Na+внутрь, а K+из клетки.
Рецептор–зависимыеионные каналы открываются или закрываются при участии нейромедиаторов, биогенных аминов, АТФ, циклических нуклеотидов. Например, в клетках обонятельной выстилки внутриклеточный цАМФ связывается с цитоплазматическим участком каналообразующего белка.
G‑белок–зависимыйK+‑канал присутствует в кардиомиоцитах и открывается при взаимодействииацетилхолинас его рецептором в составе комплекса «G‑белок + мускариновый холинорецептор».
Механочувствительныеионные каналы открываются при деформации мембраны (например, волосковые клетки внутреннего уха или чувствительная нервная терминаль механорецепторов — телецПачини).
Са2+–зависимыеионные каналы регулируют внутриклеточную (цитозоля) концентрацию Са2+.
Избирательныйфильтропределяет, какие именно типы ионов (анионы или катионы) или конкретные ионы (например, Na+, К+, Ca2+, Cl–) имеют доступ в пору канала.
Пораоткрытогоканала. После приобретения интегральным белком канала конформации, соответствующей открытому состоянию канала, формируется трансмембранная пора, внутри которой перемещаются ионы.
Состоянияканала. Благодаря наличию ворот, сенсора, избирательного фильтра и поры ионные каналы могут быть в состояниях покоя, активации и инактивации.
Состояниепокоя— канал закрыт, но готов к открытию в ответ на химические, механические или электрические стимулы.
Состояниеактивации— канал открыт и пропускает ионы.
Состояниеинактивации— канал закрыт и не способен к активации. Инактивация возникает тотчас после открытия канала в ответ на действие стимула и длится от нескольких до нескольких сотен миллисекунд (в зависимости от типа канала).
Примеры. Наиболее распространённые каналы — для Na+, K+, Ca2+, Cl–, НСО–3.
Натриевыеканалы(рис. 2–10) присутствуют практически в любой клетке. Поскольку трансмембранная разность электрохимического потенциала для Na+(DmNa)отрицательна, при открытом состоянии Na+‑канала ионы натрия устремляются из межклеточного пространства в цитозоль (слева на рис. 2–11).
В электровозбудимых структурах (например, скелетные МВ, кардиомиоциты, ГМК, нейроны) натриевые каналы генерируют ПД, точнее — начальный этап деполяризации мембраны. Потенциаловозбудимые натриевые каналы — гетеродимеры; в их состав входят большая a‑субъединица (Mrоколо 260 кД) и несколько b‑субъединиц (Mr32–38 кД). Свойства канала определяет трансмембранная a‑СЕ.
Антагонисты натриевых каналов(вещества, блокирующие функцию каналов): местные анестетики (например, лидокаин), противосудорожные препараты (например, карбамазепин), токсины (например, тетродотоксин, сакситоксин, батрахотоксин), антиаритмические препараты класса IA (например, хинидин), диуретик амилорид (мочегонные свойства амилорида объясняют закрытием натриевых каналов в почечных канальцах).
Генные дефекты a‑субъединицы(мутации генаSCN4А) — причина ряда заболеваний с эпизодически возникающей мышечной адинамией (гиперкалиемический периодический паралич типа II, миотония врождённая, парамиотония врождённая). Удлинённого интервала QT синдром (тип 3) развивается вследствие мутации генаSCN5A, кодирующего a‑СЕ натриевого канала кардиомиоцитов.
В канальцах нефрона и в кишечнике Nа+‑каналы концентрируются на верхушке эпителиальных клеток, поэтому Na+входит в эти клетки из просвета и далее поступает в кровь, обеспечивая реабсорбцию натрия в почке и всасывание натрия в ЖКТ.
Калиевыеканалы(рис. 2–8) — интегральные мембранные белки; эти каналы обнаружены в плазмолемме всех клеток. Трансмембранная разность электрохимического потенциала для K+(DmK) близка к нулю (илислегкаположительна), поэтому при открытом состоянии K+‑канала ионы калия перемещаются из цитозоля во внеклеточное пространство («утечка» калия из клетки, справа на рис. 2–11).ФункцииK+‑каналов: поддержание МП покоя (отрицателен по внутренней поверхности мембраны), регуляция объёма клетки, участие в завершении ПД, модуляция электрической возбудимости нервных и мышечных структур, секреция инсулина из b‑клеток островковЛангерханса.
Классификация. Калиевые каналы подразделяют на потенциалозависимые, потенциалонезависимые (в т.ч. активируемые Ca2+и выпрямляющие) и управляемые рецепторами и лигандами (например, ацетилхолином, АТФ).
Cекрецияинсулина. Калиевый канал KCNA1 регулирует в b‑клетках островковЛангерхансасекрецию инсулина в ответ на повышение содержания глюкозы в крови, а также в ответ на гипогликемические препараты сульфонилмочевины. Препараты сульфонилмочевины, принимаемыеperos, широко используют для снятия гипергликемии при инсулин–независимом сахарном диабете (сахарный диабет типа II). ЛС этого типа блокируют калиевые каналы в плазмолемме b‑клеток островков поджелудочной железы, взаимодействуя с белком SUR (от SUlfonylurea Receptor — рецептор сульфонилмочевины — СЕ К+[АТФ–зависимого]–ионного канала).
УдлинённыйинтервалQT, фиксируемый на ЭКГ, — фактор риска внезапной коронарной смерти — может быть приобретённым (при выраженной гипокалиемии) и врождённым (в т.ч. при дефектах генов калиевых каналовKCNA8иKCNC1).
Кальциевыеканалы— белковые комплексы, состоящие из нескольких СЕ (a1, a2, b, g, d). Поскольку трансмембранная разность электрохимического потенциала для Ca2+(DmCa) существенноотрицательна, то при открытом состоянии Ca2+‑канала ионы кальция устремляются из внутриклеточных мембранных «депо кальция» и межклеточного пространства в цитозоль. При активации каналов происходит деполяризация мембраны, а также взаимодействие лигандов с их рецепторами. Ca2+‑каналы подразделяют на потенциалозависимые и на управляемые рецепторами (например, адренергическими).
Классификация. Фармакологические и кинетические характеристики кальциевого тока позволили выделить кальциевые каналы типовL(от long lasting — медленные),T(от transient — быстрые),N(от neuronal — нейронные),Р(по имени моравского физиолога Яна ЭвангелистаПуркинья—Purkinje).
L–тип. 1,4-Дигидропиридины (например, нифедипин), а также другие блокаторы кальциевых каналовугнетаюткальциевый ток (например, в кальциевых каналах скелетных мышц, миокарда, эндокринных клеток/нейронов).
P–тип. Дигидропиридинынеблокируютактивность каналов (например, в кальциевых каналах нервных клеток).
Анионныеканалы. Многие клетки содержат разные типы анионоселективных каналов, через которые происходит пассивный транспорт Cl–и в меньшей степени — НСО–3. Поскольку трансмембранная разность электрохимического потенциала для Cl–(DmCl) умеренноотрицательна, при открытом анионном канале ионы хлора диффундируют из цитозоля в межклеточное пространство (справа на рис. 2–11).
Плазмолемма скелетных МВ имеет высокую Cl––проводимость, регулирующую электрическую возбудимость плазмолеммы. Уменьшение Cl–-проводимости ведёт к электрической нестабильности мембраны МВ и к развитию миотонии.
