
- •Нуклеотидный состав днк и рнк
- •Кислот в листьях и побегах растений может изменяться в пределах 0,1–1% сухой массы.
- •3.3.6.1. Генетическая роль и строение днк
- •3.1. Содержание и соотношение азотистых оснований в днк различных организмов
- •3.3.6.2. Виды рнк и их строение
- •3.3.7. Генетический код
- •3.2. Кодоны генетического кода*
- •3.3.8. Синтез днк
- •3.3.9. Cинтез рнк
- •3.3.10. Синтез белков
- •3.3.11. Синтез нуклеотидов
- •3.3.12. Процессы распада нуклеиновых кислот и нуклеотидов
- •3.3.13. Распад белков.
3.3.11. Синтез нуклеотидов
Для синтеза нуклеиновых кислот, коферментных нуклеотидных группировок ферментов, макроэргических нуклеозидполифосфатов необходимы пуриновые и пиримидиновые нуклеотиды. Продуктами их первичного синтеза являются соответствующие рибонуклеотиды, из которых в дальнейшем в результате восстановительных реакций образуются дезоксирибонуклеотиды.
П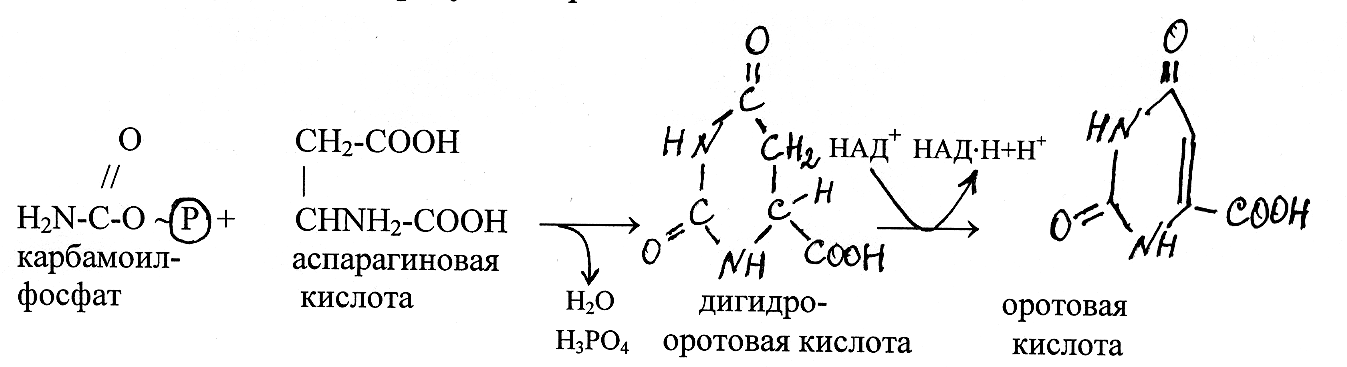 иримидиновые
рибонуклеотиды синтезируются из
аспарагиновой кислоты и карбамоилфосфата,
на образование которого используются
аммонийный азот, бикарбонат-ионы и
молекулы АТФ (с. 135–136). Под действием
фермента карбамоилтрансферазы
карбамоильная группировка
кар-бамоилфосфата переносится на остаток
аспарагиновой кислоты, и в результате
отщепления молекулы воды из указанных
компонентов синтезируется молекула
дигидрооротовой кислоты. На следующем
этапе дигидрооротовая кислота окисляется
флавиновым ферментом, который отщепляет
от неё атомы водорода и переносит их на
окисленные динуклеотиды НАД+. В
результате этой реакции образуется
оротовая кислота:
иримидиновые
рибонуклеотиды синтезируются из
аспарагиновой кислоты и карбамоилфосфата,
на образование которого используются
аммонийный азот, бикарбонат-ионы и
молекулы АТФ (с. 135–136). Под действием
фермента карбамоилтрансферазы
карбамоильная группировка
кар-бамоилфосфата переносится на остаток
аспарагиновой кислоты, и в результате
отщепления молекулы воды из указанных
компонентов синтезируется молекула
дигидрооротовой кислоты. На следующем
этапе дигидрооротовая кислота окисляется
флавиновым ферментом, который отщепляет
от неё атомы водорода и переносит их на
окисленные динуклеотиды НАД+. В
результате этой реакции образуется
оротовая кислота:
Д алее
в реакции вступает рибозо-5-фосфат,
который фосфорилирует-ся от АТФ и
превращается в 5-фосфорибозил-1-пирофосфат:
алее
в реакции вступает рибозо-5-фосфат,
который фосфорилирует-ся от АТФ и
превращается в 5-фосфорибозил-1-пирофосфат:
рибозо-5-фосфат 5-фосфорибозил-1-пирофосфат
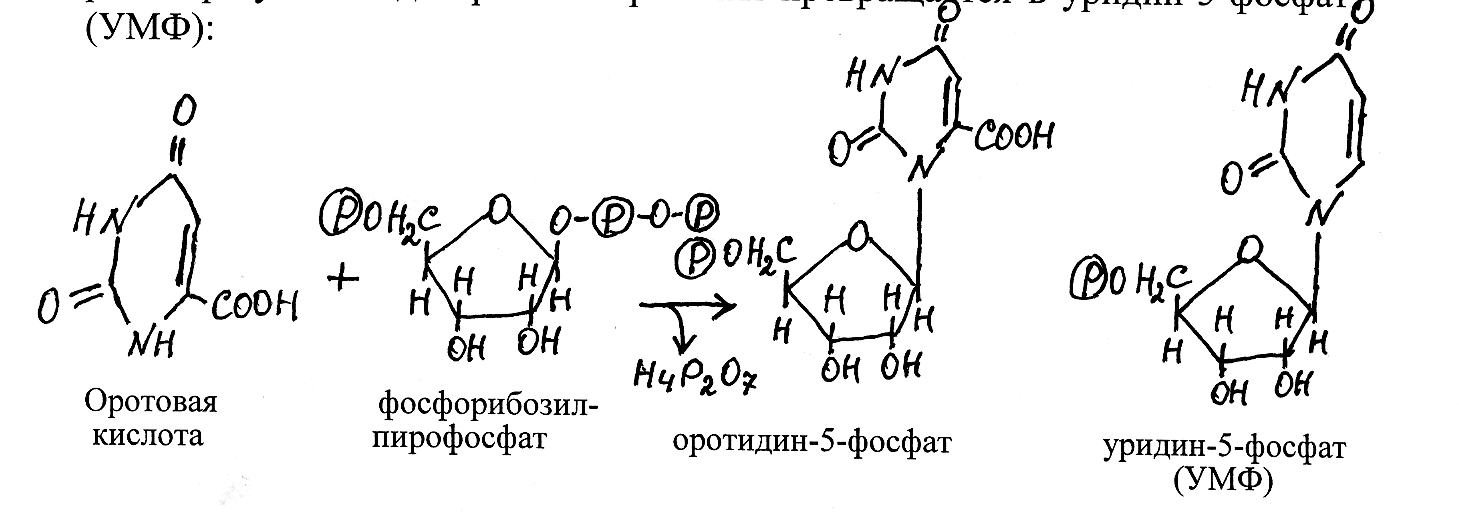
Образовавшийся фосфорибозилпирофосфат при взаимодействии с оротовой кислотой даёт оротидин-5-фосфат, который в результате декарбоксилирования превращается в уридин-5-фосфат (УМФ):
0 0
 ||
||
||
||
В
АТФ
АТФ
УМФ
УДФ УТФ
↓ ↓
АДФ АДФ
ЦТФ (цитидинтрифосфат), необходимый для синтеза РНК, образуется из УТФ в результате аминирования азотистого основания в составе нуклеотида. Донором аминной группы служит амидная группировка гдутамина. Реакция аминирования сопряжена с гидролизом АТФ до АМФ:
АТФ
УТФ + глутамин ЦТФ + глутаминовая кислота
↓
АМФ
Н₄Р₂О₇
 Исходным соединением для синтеза
пуриновых нуклеотидов, как и пиримидиновых,
служит фосфорибозилпирофосфат, к
которому присоединяются радикалы
глутамина, глицина, аспарагиновой
кислоты, углеродсодержащие группировки
СО2, формил- и метенилтетрагидрофолиевой
кислоты. В ходе довольно сложных
превращений постепенно в соединении с
фосфорибозильным радикалом строится
структура азотистого основания. На ряде
этапов построение гетероциклической
группировки азотистого основания
сопряжено с гидролизом АТФ.
Исходным соединением для синтеза
пуриновых нуклеотидов, как и пиримидиновых,
служит фосфорибозилпирофосфат, к
которому присоединяются радикалы
глутамина, глицина, аспарагиновой
кислоты, углеродсодержащие группировки
СО2, формил- и метенилтетрагидрофолиевой
кислоты. В ходе довольно сложных
превращений постепенно в соединении с
фосфорибозильным радикалом строится
структура азотистого основания. На ряде
этапов построение гетероциклической
группировки азотистого основания
сопряжено с гидролизом АТФ.
Первичным пуриновым нуклеотидом, который синтезируется в процессе указанных выше превращений, является инозиновая кислота (ИМФ). Два атома углерода азотистого основания ИМФ гипоксантина включены в его гетероциклическую группировку из молекул глутамина (амидный азот), один атом азота из аспарагиновой кислоты и ещё один атом азота из аминогруппы глицина. Кроме того, глицин является также донором двух атомов углерода. Ещё два атома углерода гипоксантина происходят от формильных группировок 5,10-метенилтетрагидрофолиевой кислоты (5,10-метенил-ТГФК) и 10-формилтетрагидрофолиевой кислоты (10-фор-мил-ТГФК). Донором карбонильной группы гипоксантина служит СО2.
В результате аминирования от аспарагиновой кислоты в ходе двух-
этапного превращения из инозиновой кислоты синтезируется адениловая кислота. В связи с тем что эта реакция эндергоническая, она сопряжена с гидролизом ГТФ:
ГТФ
ИМФ + аспарагиновая кислота АМФ + фумаровая кислота
↓
ГДФ
Н3РО4
При окислении инозиновой кислоты НАД-зависимой дегидрогеназой происходит её превращение в ксантиловую кислоту, которая далее в результате аминирования от глутамина и сопряжённого гидролиза АТФ образует гуаниловую кислоту (ГМФ):
Н2О + НАД+
ИМФ ―――― ксантиловая кислота
НАД ∙ Н + Н+
АТФ
Ксантиловая кислота + глутамин ГМФ + глутаминовая кислота
↓
АМФ
Н4Р2О7
И
Н3РО4
Н3РО4
АМФ
АДФ АТФ
↓
↓
Н2О
Н2О
П
АТФ
АТФ
ГМФ
ГДФ ГТФ
↓ ↓
АДФ
АДФ
АДФ
АДФ
Таким образом, нами рассмотрены механизмы образования пиримидиновых и пуриновых рибонуклеотидов и их трифосфатпроизводных, необходимых для синтеза рибонуклеиновых кислот и использования в качестве макроэргических соединений.
SН
S
ⓅОⓅ
основание ∕
ⓅОⓅО
∕
│
+
R
+ R │
╲
╲│
SН
S
дифосфатрибо-
тиоредоксин дифосфатдезокси-
тиоредоксин
нуклеотид
восстановленный
рибонуклеотид окисленный

Восстановление окисленной формы тиоредоксина катализирует фер-мент тиоредоксинредуктаза, который переносит электроны и протоны на тиоредоксин от восстановленного НАДФ Н.
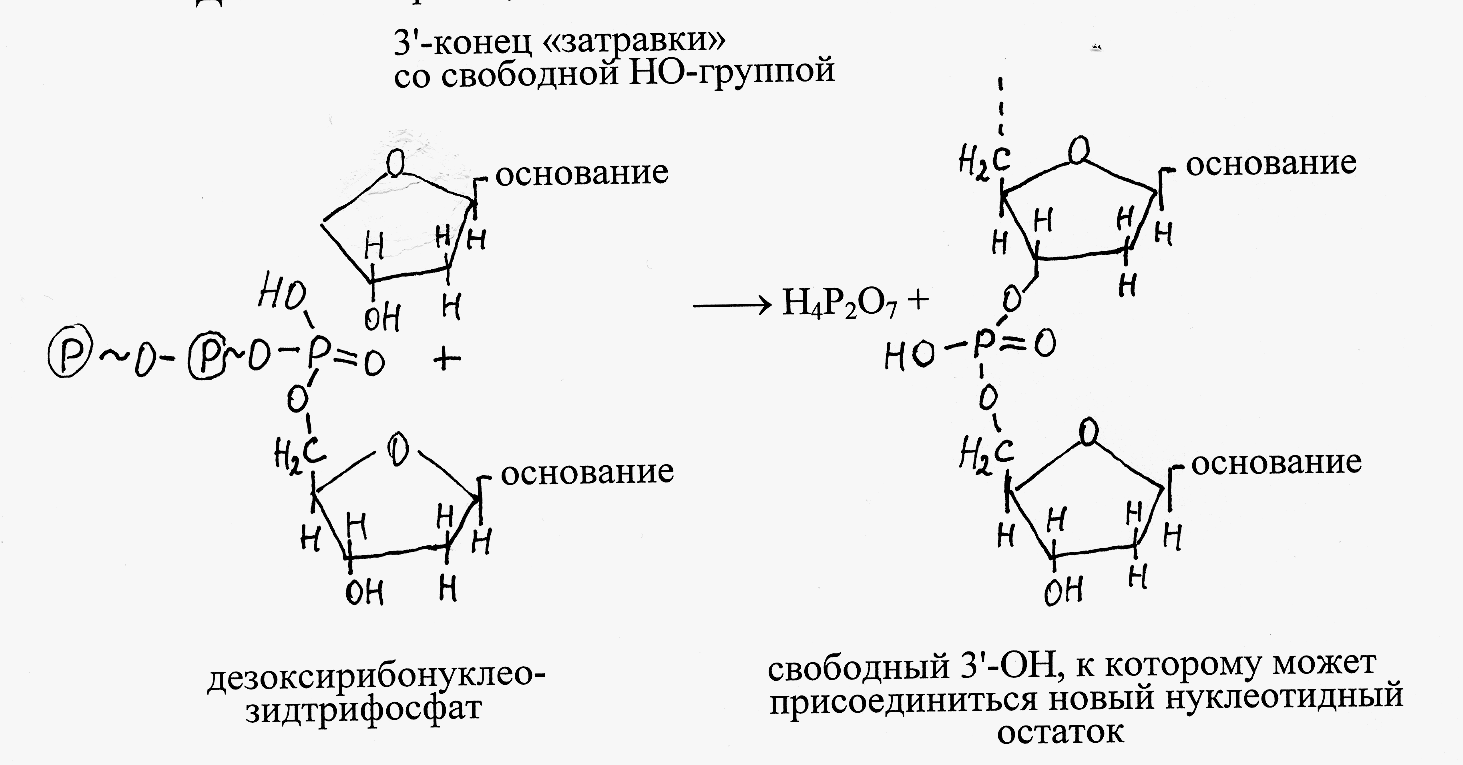
В ходе указанных реакций происходит синтез дАДФ из АДФ, дГДФ из ГДФ и дЦДФ из ЦДФ. В результате фосфорилирования дифосфатпроизводных образуются соответствующие трифосфаты дезоксирибонуклеотидов, необходимые для синтеза ДНК.
Б олее
сложным путём осуществляется синтез
дезокситимидиловой кислоты. У эукариот
исходным соединением для её образования
служит дезоксицитидиндифосфат (дЦДФ).
Превращение дЦДФ в дезокситимидиловую
кислоту (дТМФ) осуществляется по следующей
схеме:
олее
сложным путём осуществляется синтез
дезокситимидиловой кислоты. У эукариот
исходным соединением для её образования
служит дезоксицитидиндифосфат (дЦДФ).
Превращение дЦДФ в дезокситимидиловую
кислоту (дТМФ) осуществляется по следующей
схеме:
В первой реакции происходит гидролитическое отщепление от дЦДФ остатка фосфорной кислоты, во второй – дезаминирование цитозиновой группировки в составе нуклеотида и превращение её в остаток урацила. Более сложное превращение происходит на третьем этапе, которое катализирует фермент тимидилатсинтетаза. Под действием этого фермента осуществляется метилирование остатка урацила в нуклеотиде с участием метилентетрагидрофолиевой кислоты (метилен-ТГФК) и превращение его в остаток тимина, при этом из метилен-ТГФК образуется дигидрофолевая кислота (ДГФК).
В
АТФ
АТФ
дТМФ
дТДФ
дТТФ
↓
↓
АДФ
АДФ
В
НАДФН+Н+
серин
ДГФК
ТГФК
5,10-метилен-ТГФК
↓
↓
НАДФ+
глицин
Ферменты тимидилатсинтетаза и дигидрофолат редуктаза, сущест-венно влияющие на скорость образования тиминовых нуклеотидов, являются активными инициаторами синтеза ДНК. При понижении их активности замедляется или прекращается образование дезокситимидиловой кислоты, что приводит к прекращению синтеза ДНК. Подбирая эффективно действующие ингибиторы этих ферментов, можно при необходимости направленно подавлять синтез ДНК в клетках организма. Такие ингибиторы положены в основу химиотерапии рака, так как способны подавлять развитие раковых клеток, в которых интенсивно происходит синтез ДНК.
