
- •Опыт 4. Свойства фенола
- •Лабораторная работа №3. Альдегиды и кетоны опыт 1. Реакции окисления альдегидов
- •Опыт 3. Получение и свойства предельных высших кислот и их солей
- •1. Пробирки (3 шт.).
- •Опыт 4. Сложные эфиры органических кислот. Реакция этерификации
- •2. Термометр.
- •4. Пробирки (2шт).
- •Опыт 5. Непредельные одноосновные карбоновые кислоты Свойства олеиновой кислоты
- •1. Пробирки (2шт).
- •Лабораторная работа №4. Азотсодержащие соединения опыт 1. Образование солей анилина
- •Опыт 2. Реакции на карбонильные группы в моносахаридах
- •Опыт 3. Реакция на гидроксильные группы дисахаридов. Реакция дисахаридов с гидроксидом меди (II) в щелочном растворе
- •1. Пробирки (2шт.).
- •Опыт 4. Реакции дисахаридов по карбонильным группам (сравнение свойств восстанавливающих и невосстанавливающих дисахаридов)
- •1. Пробирки (3 шт.).
- •Лабораторная работа № 6. Качественные реакции на аминокислоты и белки
- •Лабораторные работы по вмс углеводы
Лабораторная работа № 6. Качественные реакции на аминокислоты и белки
При взаимодействии белков с определенными реактивами образуются окрашенные продукты реакции, что обусловлено присутствием в белке той или иной аминокислоты или группировки. Эти так называемые цветные или качественные реакции на белки широко используются для установления белковой природы веществ или обнаружения в исследуемых веществах той или иной аминокислоты.
При ознакомлении с цветными реакциями следует обратить внимание на химическую структуру той аминокислоты или химической группировки, присутствие которых в белке обуславливает данную реакцию.
Результаты лабораторной работы оформить в виде таблицы:
№ п/п |
Название реакции |
Материал исследований |
Ход работы |
Наблюдения |
Чем обусловлена реакция |
|
|
|
|
|
|
ОПЫТ 1. Биуретовая реакция Пиотровского
При добавлении к щелочному раствору белка раствора сернокислой меди жидкость приобретает красно-фиолетовый или сине-фиолетовый цвет. Реакция обусловлена присутствием в белке пептидных связей, которые с ионами меди образуют окрашенное комплексное соединение. В щелочной среде кетонная форма полипептида переходит в енольную.
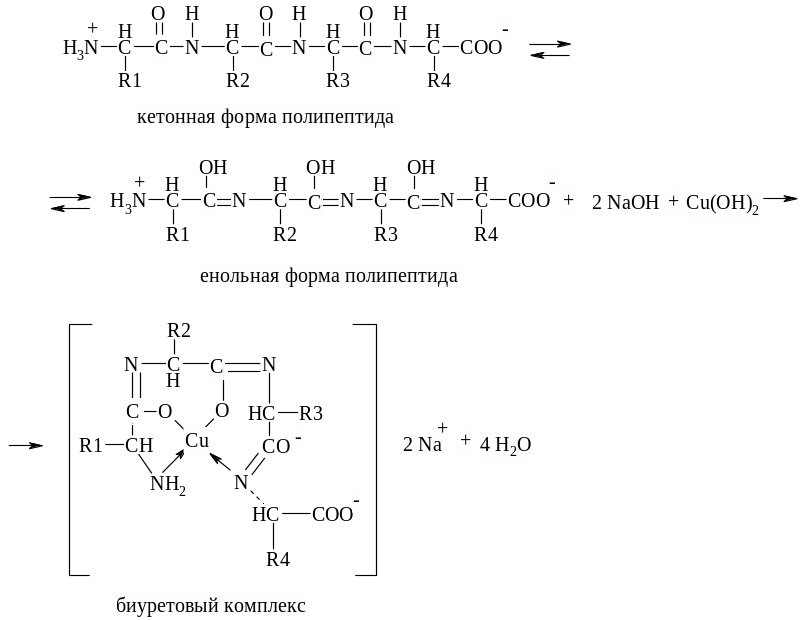
Енольная форма полипептида взаимодействует со щелочным раствором медной соли с образованием так называемого биуретового комплекса.
Интенсивность окраски зависит от длинны пептида и варьирует от сине-фиолетовой до красно-фиолетовой. Положительную реакцию дают соединения, содержащие не менее двух пептидных связей.
Ход работы:
В одну пробирку налить 2 мл раствора яичного белка, в другую столько же раствора желатина. Затем в каждую прибавить равный объем 10%-ного раствора едкого натра и по 2-3 капли 1%-ного раствора сернокислой меди СuSO4. Проявляется красно-фиолетовое окрашивание.
ОПЫТ 2. Нингидриновая реакция на α-аминокислоты
Эта реакция обусловлена присутствием в белке аминокислот, имеющих аминогруппу в α-положении.
Белки, пептиды и аминокислоты образуют с нингидрином соединение синего или сине-фиолетового цвета. α-Аминокислоты, реагируя с нингидрином, окисляются и распадаются с образованием аммиака, альдегида и углекислого газа. Нингидрин восстанавливается и конденсируется с другой молекулой нингидрина и аммиаком. В результате образуется сложное соединение, окрашенное в синий цвет /пурпурный Руэмана/.
Реакция может быть представлена следующим образом:
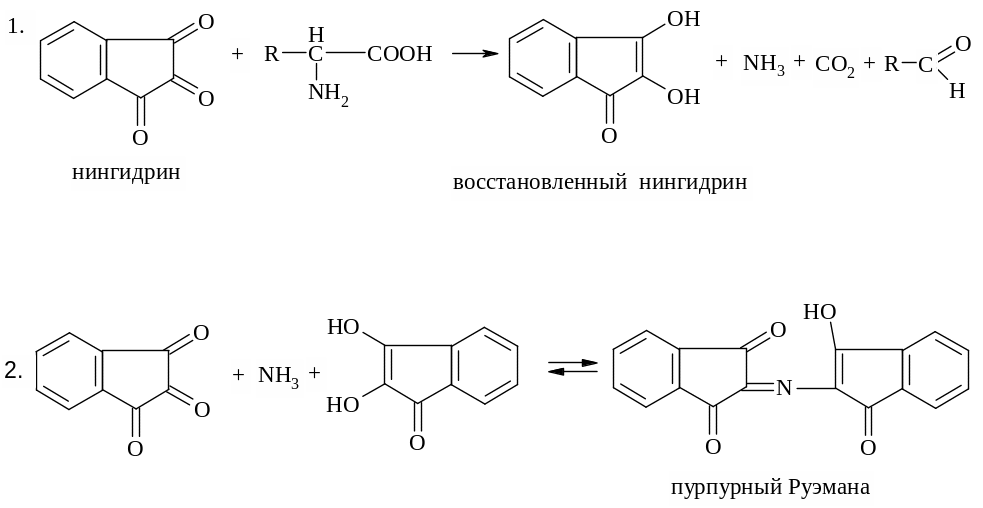
Ход работы:
В одну пробирку налить 1-2 мл 1%-ного раствора глицина, в другую столько же раствора яичного белка. В обе пробирки добавить 0,1-ный спиртовый раствор нингидрина (в первую пробирку 5-6 капель, во вторую 10-12 капель) и нагревать около минуты. В пробирке с глицином быстро появляется сине-фиолетовое окрашивание. В пробирке с белком окраска более бледная красно-фиолетовая и развивается медленнее.
ОПЫТ 3. Ксантопротеиновая реакция на циклические аминокислоты
Ксантопротеиновая реакция характерна для некоторых ароматических аминокислот (фенилаланина, тирозина, триптофана). При нагревании белков, содержащих эти аминокислоты, с концентрированной азотной кислотой образуется соединение желтого цвета:
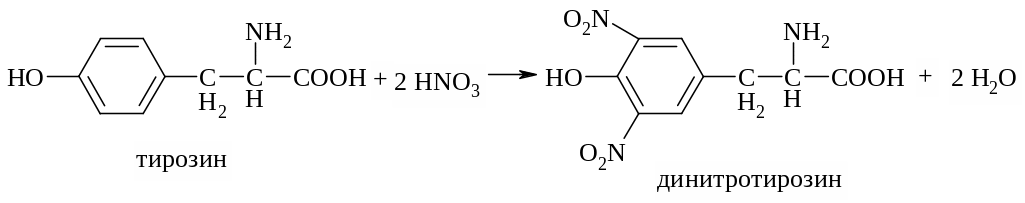
На второй стадии нитропроизводное реагирует с гидроксидом аммония с образованием аммонийной соли желто-оранжевого цвета.
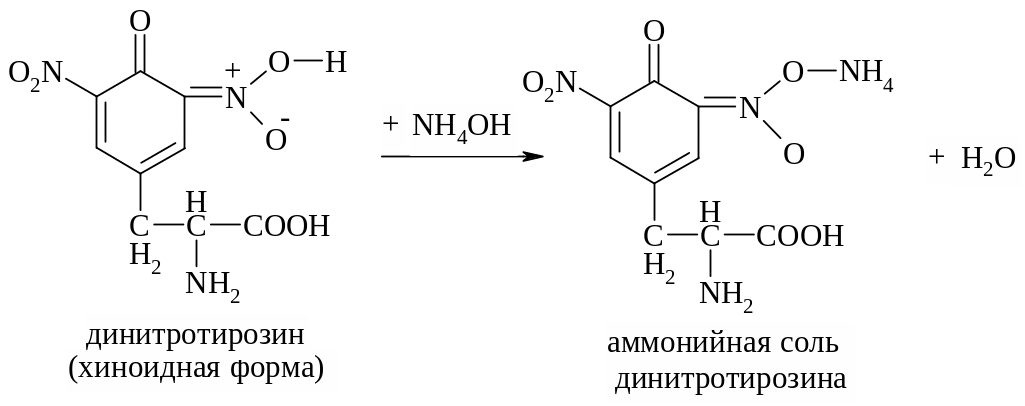
Ксантопротеиновую реакцию, кроме белков, пептидов и циклических аминокислот, дают также многие простые ароматические соединения (бензол, фенол др.)
Ход работы:
К 2 мл 0,1%-ного раствора фенола осторожно по стенке прилить 1-2 мл концентрированной азотной кислоты и осторожно нагреть. Появляется желтое окрашивание.
В другую пробирку налить 2 мл яичного белка, прибавить 8-10 капель концентрированной азотной кислоты и осторожно нагреть. Выпадает осадок, который окрашивается в желтый цвет.
После охлаждения в пробирку осторожно по стенке приливают избыток концентрированного раствора аммиака. Жидкость приобретает желто-оранжевый цвет.
Реакцию проводят под тягой!
3. Те же реакции проводят с раствором желатина. Однако желтое окрашивание с ней не появляется, так как желатин не содержит ароматических аминокислот.
