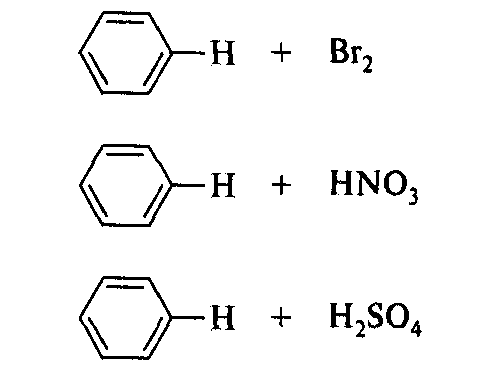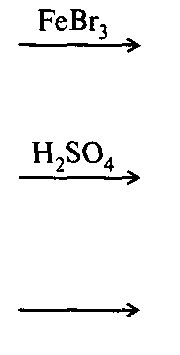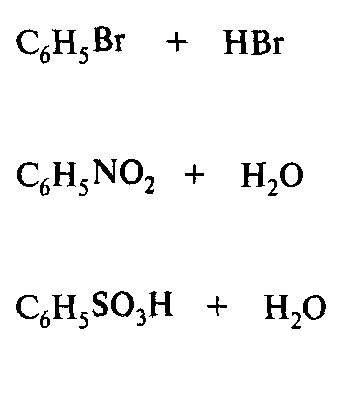- •II. Окислительно-восстановительные реакции
- •1.Значение окислительно-восстановительных реакций (овр)
- •1. Замещение s
- •2. Присоединение а
- •III. Характерные реакции основных классов органических соединений
- •2 . Свойства основных классов органических соединений Алканы и циклоалканы sr,
- •1. Инициирование цепи
- •2. Рост цепи
- •3. Обрыв цепи
- •Дегидрогеназное окисление
- •Алкены и малые циклоалканы, ае
- •Правило Марковникова
- •Окислительно восстановительные и качественные реакции алкенов
- •Ароматические соединения se
- •Спирты, простые эфиры, тиолы, сульфиды, амины, sn,e
- •Карбонильные соединения альдегиды и кетоны, an
- •Карбоновые кислоты, их функциональные производные, sn
- •Строение карбоксильной группы
- •Важнейшие функциональные производные карбоновых кислот
- •Реакции нуклеофильного замещения sn карбоновых кислот и их функциональных производных
- •Этерификация,sn
- •2. Образование тиоэфиров с тиолами
- •3. Образование амидов с аминами или n-ацилирование, sn
Окислительно восстановительные и качественные реакции алкенов
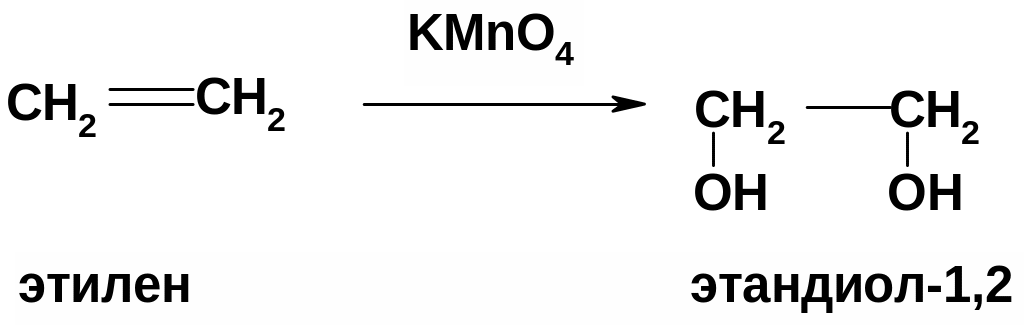
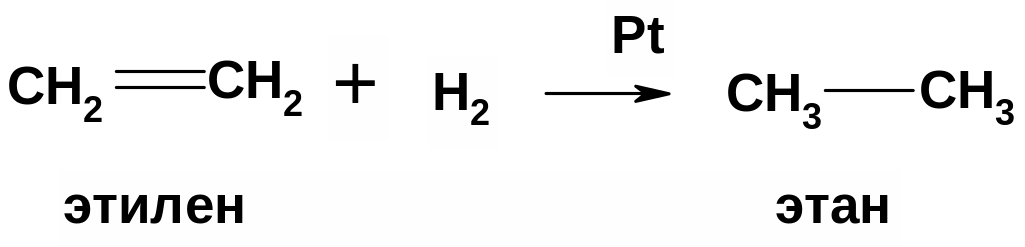
Окислительно – восстановительные реакции алкенов идут легко. Ненасыщенные углеводородные фрагменты (алкены) окисляются до двухатомных спиртов (in vitro) и восстанавливаются до насыщенных (in vitro и in vivo) (р. гидрогенизации). Качественная реакция на двойную связь это также окисление раствором КMnO4 с образованием двухатомного спирта (диола-1,2).
а) окисление
б) восстановление
Ароматические соединения se
Реакции электрофильного замещения SE в ароматических соединениях идут по ионному механизму (ТюкавкинаН.А. Биоорганическая химия стр.135-144 ).
Примеры реакций:
|
Галогенирование
Нитрование
Сульфирование
Ориентирующее действие заместителей в бензольном кольце ((ТюкавкинаН.А. Биоорганическая химия стр. 141-142 )
Заместители (ориентанты) I рода направляют атаку электрофила в орто- и пара- положения (2,4,6).
Примеры:
-OH, -NH2, –Hal, -CH3.
Заместители II рода направляют атаку электрофила в мета- положение (3 или 5).
Примеры:
-COOH, –CHO, -SO3H, -NO2.
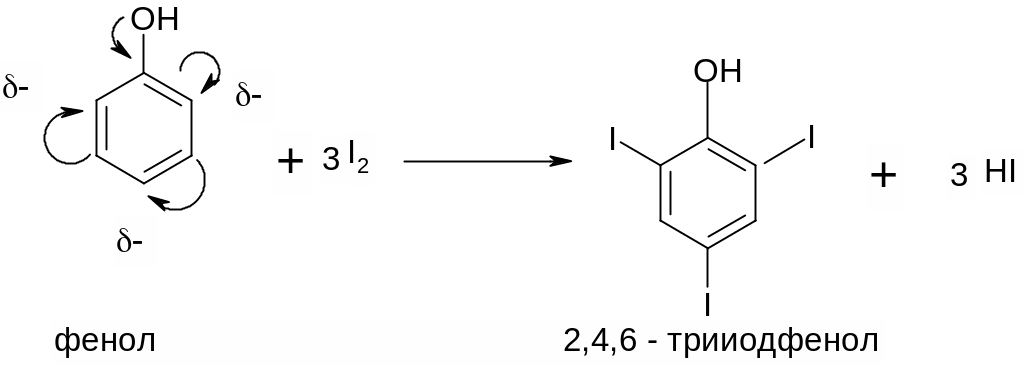
Пример: галогенирование фенола или анилина идет очень активно, в несколько положений т.к. заместитель очень сильный электронодонор.
Спирты, простые эфиры, тиолы, сульфиды, амины, sn,e
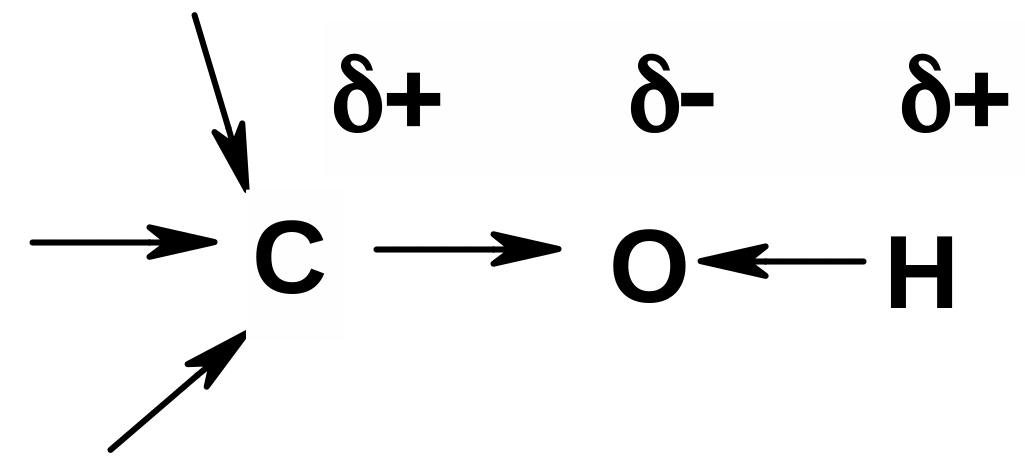
Спирты в организме встречаются как в виде монофункциональных соединений, так и в виде спиртовых фрагментов гетерофункциональных метаболитов. Причина появления качественно новых свойств у спиртов – наличие полярной функциональной группы. Между молекулами спиртов возникают водородные связи, поэтому спирты имеют более высокую температуру кипения и плавления и лучше растворяются в воде, чем углеводороды.
![]()
![]()
….
Спирты являются слабыми кислотами, взаимодействуют только с металлическим натрием. Характерные реакции нуклеофильного замещения SN у насыщенного атома углерода и элиминирование, если в спирте не менее 2х атомов углерода.
Спирты в организме легко окисляются по дегидрогеназному типу. Метанол и первичные спирты окисляются до альдегидов, вторичные до кетонов, третичные устойчивы к окислению.
Характерные химические реакции спиртов
Нуклеофильное замещение SN.
А.Спирты субстраты и нуклеофилы. (О-алкилирование) Пример: межмолекулярная дегидратация
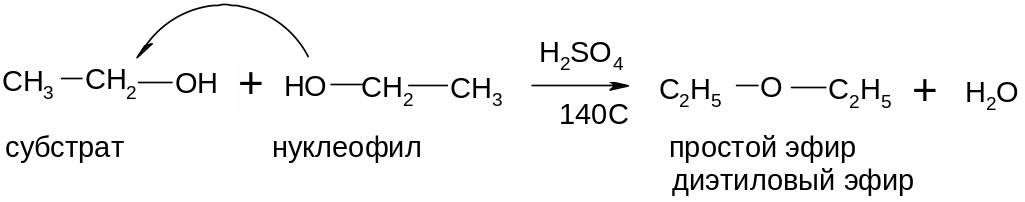
Б. Спирты- только нуклеофилы. (О-ацилирование)
Пример: реакция этерификации
Элиминирование, Е
Пример: внутримолекулярная дегидратация спиртов. Идет по правилу Зайцева: водород отщепляется от менее гидрогенизированного атома углерода
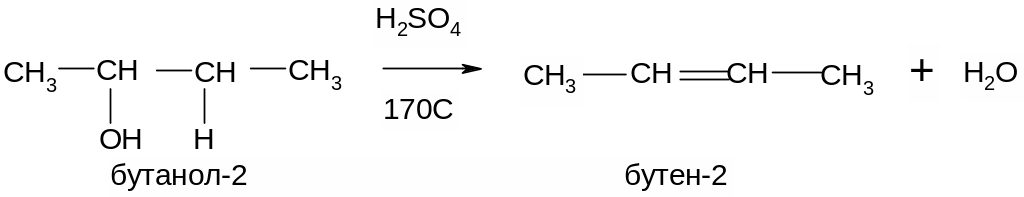
Окисление спиртов
1)Метанол и первичные спирты окисляются до альдегидов, которые затем легко окисляются до карбоновых кислот.
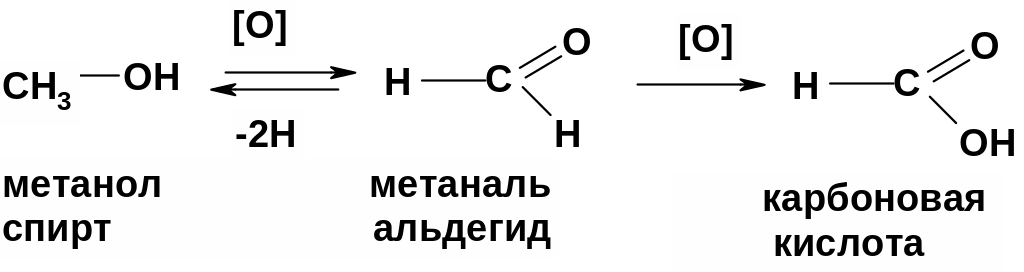
2) Вторичные спирты окисляются до кетонов

3) Третичные спирты устойчивы к окислению
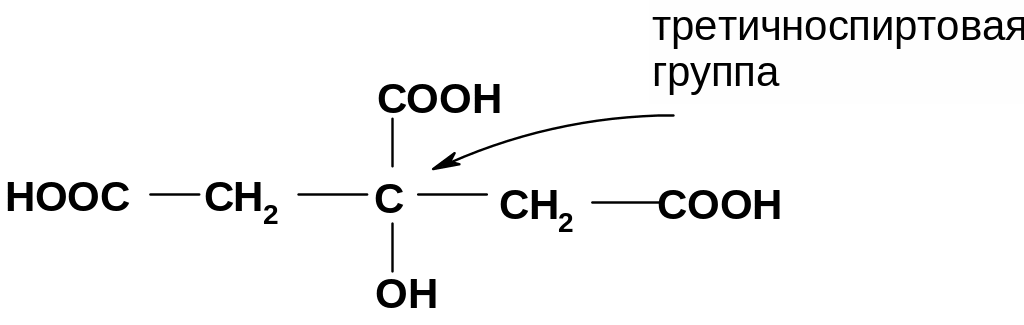
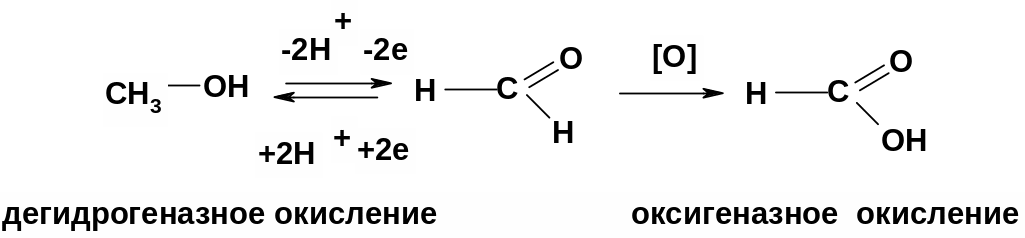
Условия окисления спиртов:
in vivo - фермент дегидрогеназа кофермент НАД+ окислитель/НАДН восстановитель
in vitro – K2Cr2O7,H+, t или CuO, t
Тиолы
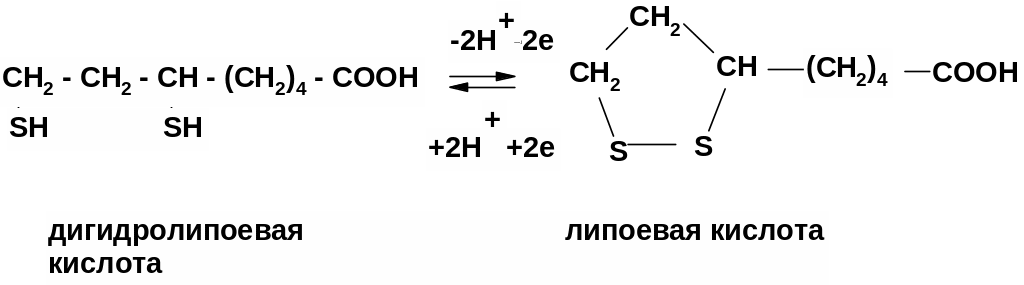
Тиольные ФГ встречаются в метаболитах довольно часто (аминокислоты, дигидролипоевая кислота, глутатион …). В основном это ФГ антиоксидантов, т.к. тиолы легко окисляются до дисульфидов, восстанавливая окислители, а дисульфиды также легко восстанавливаются в тиолы
Окисление тиолов
Реакция идет в мягких условиях (кислородом воздуха и другими слабыми окислителями).
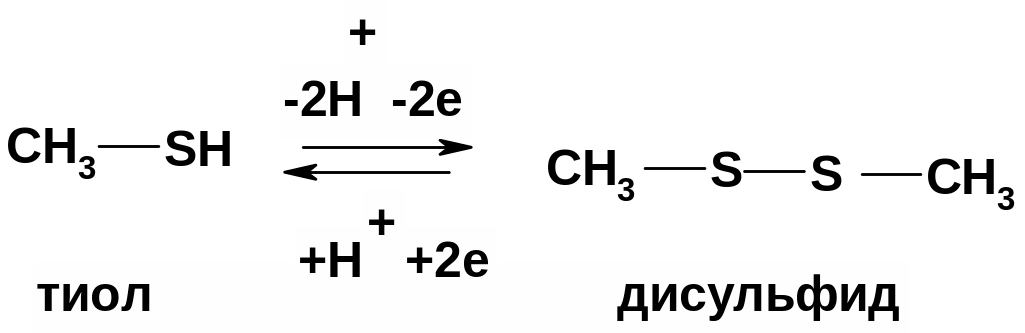
Фенолы
Это сильные ОН-кислоты, и ароматические субстраты в реакции SE , но наиболее важное свойство фенольных гидроксилов в организме – реакции ОВР.
Окисление фенолов
В организме особую роль играет процесс окисления двухатомных фенолов. Так двухатомный фенол гидрохинон окисляется в хинон, который восстанавливается в гидрохинон.
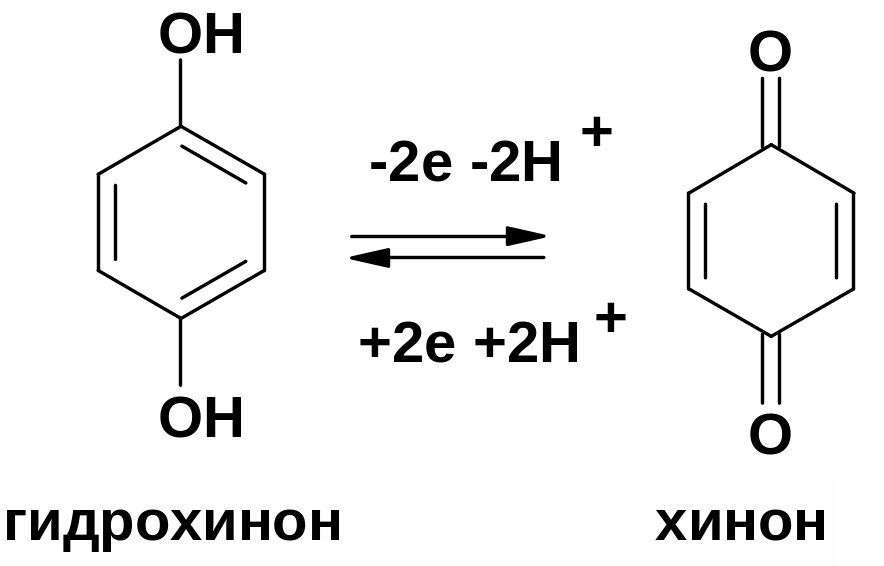
Окислительно-восстановительные свойства системы хинон-гидрохинон лежат в основе действия цепи дыхания в митохондриях. Производное хинона – убихинон или кофермент Q окисляет органические соединения, превращается в гидрохинон (гидроубихинон) и передает электроны через цитохромы кислороду.