
- •Т. В. Скрипко общая и неорганическая химия Практикум
- •1. Основные классы неорганических соединений
- •Примеры составления условий задач и их решения
- •2. Газовые законы. Простейшие стехиометрические законы
- •2.1. Взаимозависимые параметры состояния газов
- •Примеры составления условий задач и их решения
- •2.2. Химические эквиваленты
- •Примеры составления условия задач и их решения
- •3. Основные закономерности протекания химических реакций
- •3.1. Энергетика химических реакций. Химико-термодинамические расчеты
- •Примеры составления условий задач и их решения
- •3.2. Скорость химических реакций и химическое равновесие
- •Примеры составления условий задачи и их решение
- •4. Окислительно – восстановительные процессы
- •4.1. Окислительно-восстановительные реакции
- •Ионно-электронный метод
- •Примеры составления условий задач и их решения
- •4.2. Гальванические элементы
- •Примеры составления условий задач и их решения
- •4.3. Электролиз
- •Примеры составления условий задач и их решения
- •5. Растворы
- •5.1 Способы выражения содержания растворенного вещества в растворе
- •Примеры составления условий задач и их решения
- •5.2. Физико-химические свойства разбавленных растворов неэлектролитов
- •Свойства растворов неэлектролитов
- •Примеры составления условий задач и их решения
- •5.3. Растворы электролитов
- •5.4. Ионное произведение воды. Водородный показатель
- •Примеры составления задач и их решения
- •5.5. Молекулярно-ионные уравнения обменных реакций между растворами электролитов
- •Примеры составления задач и их решения
- •5.6. Произведение растворимости
- •Примеры составления задач и их решения
- •5.7. Гидролиз солей
- •Примеры составления задач и их решения
- •6. Строение атома
- •Примеры составления условий задач и их решения
- •7. Комплексные соединения
- •Примеры составления задач и их решение
- •Библиографический список
Примеры составления условий задач и их решения
Задача 889
Составить электронную формулу атомов Be, As в стабильном и возбужденном состояниях и изобразить орбитали внешнего энергетического уровня.
Решение:
Атом бериллия Be.
Стабильное состояние
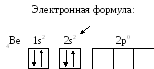
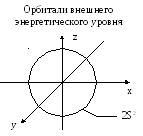
В
Орбитали
внешнего энергетического уровня


После Sp –гибридизации строение возбужденного атома бериллия

Атом мышьяка As.
Э лектронная
формула:
Стабильное
состояние
лектронная
формула:
Стабильное
состояние
Возбужденное состояние
Электронная
формула:

Задача 893
Определить, какие частицы Mg, Si, Al+ , S2– являются изоэлектронными, то есть содержащими одинаковое число электронов. Написать электронные формулы данных частиц.
Решение:
Изоэлектронными являются частицы Mg и Al+. Их электронные формулы следующие:
С табильное
состояние
табильное
состояние
В озбужденное
состояние
озбужденное
состояние
Возбужденное состояние

Задача 897
Пользуясь правилом Гунда, распределить электроны по квантовым ячейкам, отвечающим низшему и высшему энергетическим состояниям атомов мышьяка As, кобальта Co, стронция Sr.
Решение:
Низшее энергетическое состояние:
33As 1s2
2s2
2p6
3s2
3p6
3d10
4s2
4p3
4d0






Валентность равна трем
_____________________________________________________________________
27Co 1s2
2s2
2p6
3s2
3p6
3d7
4s2
4p0


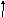







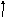
Валентность равна трем
_____________________________________________________________________
38Sr 1s2
2s2
2p6
3s2
3p6
3d10
4s2
4p6
4d0
4f0
5s2
5p0



Валентность равна нулю
___________________________________________________________________
Высшее энергетическое состояние:
33As* 1s2
2s2
2p6
3s2
3p6
3d10
4s1
4p3
4d1






Валентность равна пяти
___________________________________________________________________
27Co*
1s2
2s3
2p6
3s2
3p6
3d7
4s1
4p1










Валентность равна пяти
_____________________________________________________________________
38Sr* 1s2
2s2
2p6
3s2
3p6
3d10
4s2
4p6
4d0
4f0
5s1
5p1


Валентность равна двум
При выполнении заданий рекомендуется использовать учебное пособие [9].
В задачах 881–890 составить электронные формулы атомов элементов в стабильном и возбужденном состояниях и изобразить орбитали внешнего энергетического уровня
|
№ задачи |
Элементы |
№ задачи |
Элементы |
|
881 882 883 884 885 |
Ba, B Al, Sr Ge, Se Pb, Mg Sb, Cd |
886 887 888 889 890 |
Ga, Bi Si, Ra Sn, Cl Be, As S, I |
В задачах 891–896 определить, какие частицы являются изоэлектронными, то есть содержащими одинаковое число электронов. Написать электронные формулы данных частиц
|
№ задачи |
Частицы |
№ задачи |
Частицы |
|
891 892 893 |
Se, As3+ , Ge2+ , Br- Kr, Sr2+ , Se2-, Br- Mg, Si, Al3+, S2- |
894 895 896 |
Fe2+, Cr3+, Co3+, Ni2+ Ti, V3+, Cr2+, Fe3+ Sn2+, Sb3+, Cd, Sn4+ |
В задачах 897–906 , пользуясь правилом Хунда, распределить электроны по квантовым ячейкам (орбиталям), отвечающим низшему и высшему энергетическому состоянию атомов элементов
|
№ задачи |
элементы |
№ задачи |
элементы |
|
897 898 899 900 901 |
As, Co, Sr Mo, Sb, Ca Pb, In, Be Th, As, Fe Te, Ac, Cr |
902 903 904 905 906 |
Sm, Pb, Ag Os, Se, Na B, Re, Mn La, Xe, Ba I, Hg, S |
