
- •Автор-составитель: Пузин ю.И. Проф., д-р хим. Наук
- •Кудашева ф.Х., проф., д-р хим. Наук
- •Оглавление
- •1. Газ, нефть и нефтепродукты
- •Пример решения задач
- •1.1.4. Температуры вспышки и застывания
- •1.2. Классификация нефтей
- •1.3. Практикум
- •Ареометр
- •Затем вычисляют динамическую вязкость исследуемого нефтепродукта (η, мПас) по формуле
- •Лабораторная работа № 2. Первичная перегонка нефти
- •Свойства продуктов фракционирования
- •Нефть как многокомпонентная система
- •2.1. Основные примеси, содержащиеся в нефтях и газах
- •2.2. Нефтяные эмульсии и способы их разрушения
- •2.3. Вода в нефти и нефтепродуктах
- •2.4. Сернистые соединения в нефти и нефтепродуктах
- •2.5. Присутствие минеральных кислот, щелочей и солей в нефтепродуктах
- •2.6. Механические примеси в нефти
- •2.7. Степень ненасыщенности нефтей и нефтепродуктов
- •2.8. Практикум
- •3. Компоненты нефтей, газов, нефтепродуктов. Состав, строение, свойства
- •3.1. Ациклические углеводороды
- •3.1.5. Практикум
- •3.2.1. Алициклические углеводороды (нафтены)
- •Контрольные вопросы
- •3.2.2. Ароматические углеводороды (арены)
- •3.2.3. Практикум
- •Контрольные вопросы
- •3.3.1. Спирты
- •Методы получения спиртов
- •3.3.2. Фенолы
- •3.3.3. Карбоновые кислоты
- •3.3.4. Практикум
- •Опыт 2.Свойства фенола
- •Контрольные вопросы
- •3.4.1. Азотсодержащие соединения
- •3.4.2. Соединения, содержащие серу
- •3.4.3. Практикум
3.2.3. Практикум
Лабораторная работа № 5. Химические свойства аренов
Представители аренов:

Опыт 1. Бромирование бензола и толуола
В одну пробирку помещают 1 мл бензола, в другую - 1 мл толуола. В каждую из пробирок добавляют по 1 мл раствора брома в хлороформе и встряхивают. Пробирки нагревают на водяной бане. Бромирования бензола в этих условиях не происходит, а толуол бромируется - происходит исчезновение окраски брома. Бромирование бензола происходит только в присутствии катализатора (железные опилки). Если в первую пробирку добавить железных опилок, встряхнуть и нагреть на водяной бане, то произойдет исчезновение окраски, следовательно, бензол бромируется.

В молекуле толуола к ароматическому кольцу присоединена группа –СН3. Это заместитель I рода, он облегчает введение следующего заместителя в ароматическое кольцо и направляет его в орто- и пара-положения.
Опыт 2. Сульфирование ароматических углеводородов
В две пробирки помещают по 1 мл бензола и толуола и добавляют по 4 мл концентрированной серной кислоты. Затем нагревают пробирки на водяной бане до 80°С при частом и сильном встряхивании. Углеводороды образуют с кислотой эмульсию и затем постепенно растворяются в ней. Отмечают различие во времени, необходимое для полного растворения исследуемых углеводородов при одинаковых условиях (нагревание и встряхивание). Когда растворение закончится, охлаждают обе пробирки, выливая содержимое каждой пробирки в стаканчики с 10-15 мл холодной воды, и отмечают, выделяется ли исходный углеводород или продукт реакции.
В противоположность насыщенным углеводородам ароматические углеводороды легко сульфируются серной кислотой, образуя сульфокислоты по схеме:
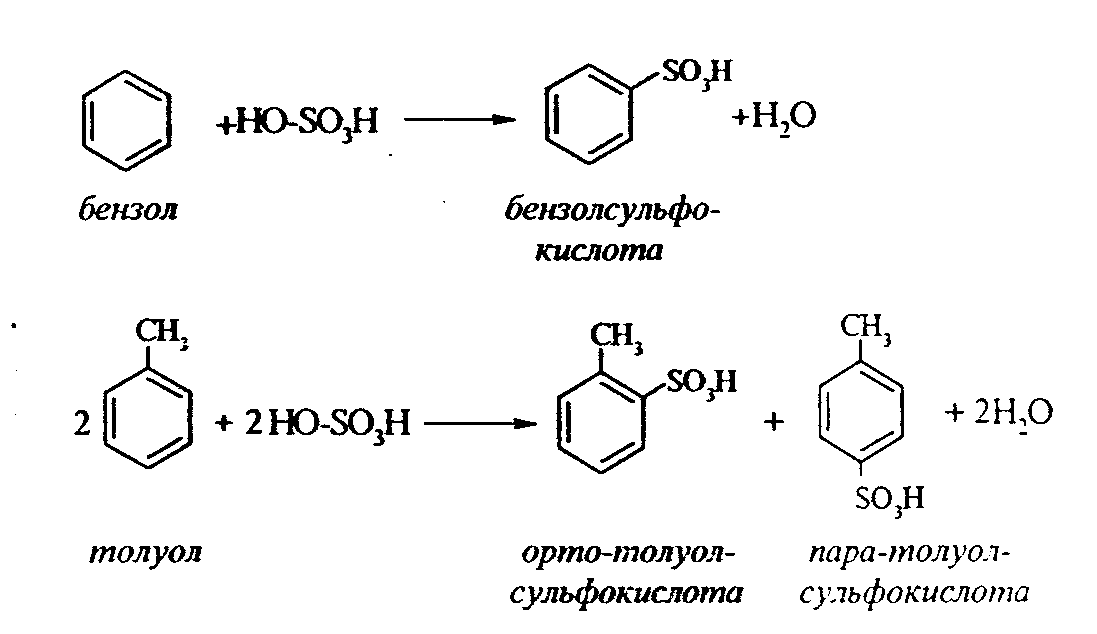
Толуол с серной кислотой образует орто-толуолсульфокислоту и пара-толуолсульфокислоту.
Опыт 3. Нитрование ароматических углеводородов
а) Нитрование бензола
Сначала в пробирке готовят нитрующую смесь из 1,5 мл концентрированной азотной и 2 мл концентрированной серной кислот. Разогревающуюся смесь охлаждают водой. Затем в полученную нитрующую смесь постепенно добавляют 1 мл бензола при сильном, но осторожном встряхивании и охлаждении в воде. Постоянное встряхивание заставляет отделяющийся верхний слой вновь эмульгировать в нижнем. Через 5 мин реакционную смесь выливают в стаканчик с 20-30 мл воды и дают отстояться. Нитробензол выделяется в виде тяжелого желтоватого масла с запахом горького миндаля.
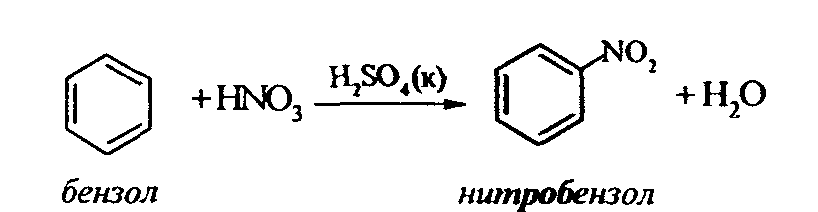
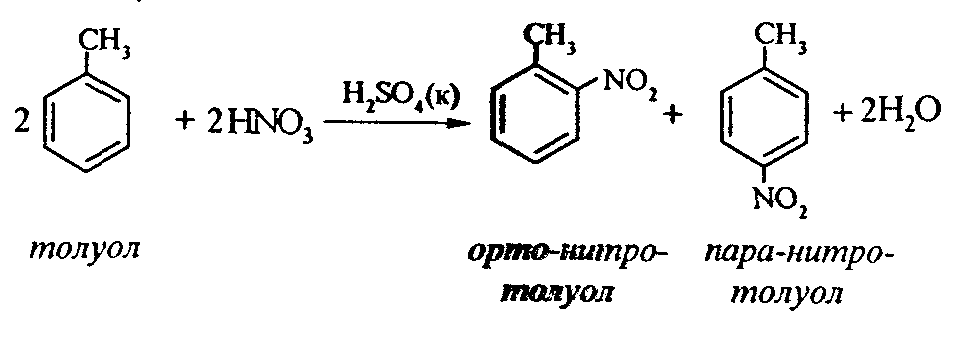
Готовят нитрующую смесь, как в предыдущем опыте. В нее при охлаждении и встряхивании по каплям добавляют 1 мл толуола. Затем содержимое пробирки выливают в стаканчик с холодной водой. Выделяется маслообразная жидкость, которая является смесью орто- и пара-нитротолуолов.
б) Нитрование нафталина
В пробирку наливают 2 мл концентрированной азотной кислоты. К азотной кислоте добавляют 0,5 г нафталина. Содержимое пробирки встряхивают и нагревают на горячей водяной бане 5 мин. Затем содержимое пробирки выливают в стаканчик с холодной водой. Образовавшийся нитронафталин выделяется в виде оранжевого масла, которое быстро затвердевает при встряхивании.

Нафталин нитруется значительно легче, чем бензол и толуол. Поэтому нитрование нафталина проводят не нитрующей смесью, а только концентрированной азотной кислотой.
Опыт 4. Окисление ароматических углеводородов
Опыт проводят одновременно с бензолом и толуолом. В две пробирки помещают по 1 мл раствора перманганата калия и разбавленной серной кислоты, затем добавляют по 0,5 мл в одну пробирку бензола, в другую -толуола. Сильно встряхивают каждую пробирку в течение нескольких минут. Отмечают изменение окраски в пробирках.
Бензол весьма устойчив к окислению и практически не реагирует с перманганатом калия ни в кислой, ни в щелочной среде. (Если реакция идет, вероятно, бензол содержит примесь толуола). Гомологи бензола окисляются значительно легче.

Опыт 5. Качественная реакция на ароматические углеводороды (формолитовая реакция)
Ароматические углеводороды образуют с формалином в присутствии серной кислоты ярко окрашенные продукты конденсации. Это свойство используют как качественную реакцию на присутствие ароматических углеводородов в нефтепродуктах.
В фарфоровую чашечку капают 4-6 капель конц. серной кислоты, затем прибавляют 3-4 капли формалина и 2-3 капли исследуемого вещества. При отсутствии ароматических углеводородов смесь остается бесцветной. Появление яркого красно-бурого окрашивания свидетельствует о наличии ароматических углеводородов в испытуемом продукте. Вместо формалина можно использовать параформ.
