
- •3.1.1 Классификация галогенопроизводных углеводородов
- •3.1.2 Изомерия галогенопроизводных предельных углеводородов
- •3.1.3 Номенклатура галогенопроизводных предельных углеводородов
- •3.1.4 Способы получения галогенопроизводных предельных углеводородов
- •3.1.5 Особенности химических свойств галогенопроизводных предельных углеводородов
- •Вопросы для самоконтроля
- •Тема 3.2 Гидроксильные соединения и их производные
- •1. По природе радикала
- •3.2.5 Способы получения предельных одноатомных спиртов
- •3.2.6 Особенности химических свойств предельных одноатомных спиртов
- •4) Реакции отщепления
- •3.2.7 Многоатомные спирты
- •3.2.8 Фенолы
- •Практическое занятие Вопросы для самоконтроля
- •Тема 3.3 Карбонильные соединения (альдегиды и кетоны)
- •Методические рекомендации
- •3.3.1 Номенклатура и изомерия альдегидов
- •3.3.1 Номенклатура и изомерия кетонов
- •3.3.3 Способы получения альдегидов и кетонов
- •3.3.4 Особенности строения и химических свойств альдегидов и кетонов
- •Практическое занятие Вопросы для самоконтроля
- •Тема 3.4 Карбоновые кислоты и их производные
- •Методические рекомендации
- •3.4.1 Классификация карбоновых кислот
- •По природе радикала
- •3.4.2 Номенклатура карбоновых кислот
- •3.4.3 Изомерия карбоновых кислот
- •3.4.4 Особенности химических свойств одноосновных карбоновых кислот
- •Реакции отщепления;
- •3.4.5 Особенности химических свойств двухосновных карбоновых кислот
- •3.4.6 Способы получения карбоновых кислот
- •Вопросы для самоконтроля
- •Тема 3.5 Азотосодержащие органические соединения (нитросоединения, амины)
- •По природе радикала
- •3.5.1.4 Способы получения предельных и ароматических мононитросоединений
- •3.5.1.5 Химические свойства ароматических мононитросоединений
- •1. По природе радикала
- •3.5.2.5 Химические свойства аминов алифатического ряда
- •Вопросы для самоконтроля
- •Раздел 4 Гетерофункциональные соединения
- •Методические рекомендации
- •4.1 Моносахариды
- •4.1.1 Классификация моносахаридов
- •4.1.2 Строение моносахаридов
- •4.1.3 Химические свойства моносахаридов
- •4.2 Дисахариды
- •4.3 Полисахариды
- •Вопросы для самоконтроля
- •Раздел 5 Синтетические высокомолекулярные соединения
- •Методические рекомендации
- •Вопросы для самоконтроля
Методические рекомендации
Карбоновые кислоты – производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на карбоксильную группу.
В общем виде формула карбоновых кислот R – COOH.
Группа –СООН является функциональной группой.
3.4.1 Классификация карбоновых кислот
Карбоновые кислоты могут быть:
По природе радикала
предельными;
непредельными;
ароматическими.
по количеству карбоксильных групп
одноосновными;
двухосновными;
многоосновными.
Основные представители карбоновых кислот приведены в приложении В.
3.4.2 Номенклатура карбоновых кислот
Карбоновые кислоты называют по тривиальной и международной номенклатурам.
Согласно международной номенклатуре – выбирают главную цепь, в которую входит углерод карбоксильной группы.
Нумерацию главной цепи начинают с атома углерода карбоксильной группы.
Название карбоновых кислот строится следующим образом: дают название пронумерованной цепи по названию соответствующего углеводорода с добавлением окончания –овая (–диовая для двухосновных) и слова «кислота».
Например:
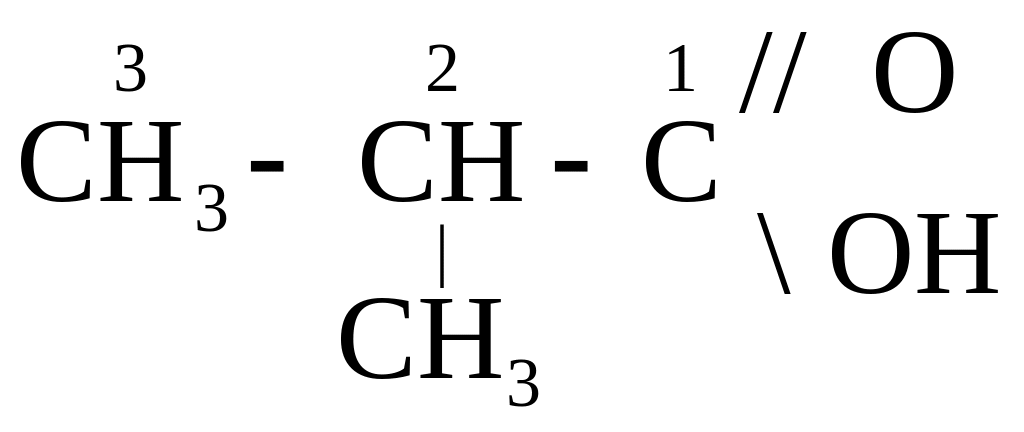
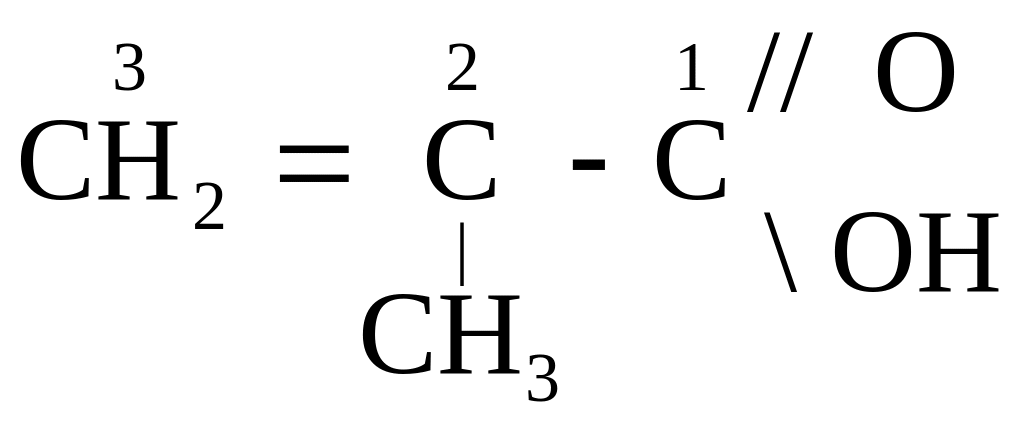
![]()
2-метилпропановая 2-метилпропен-2-овая пропандиовая
кислота кислота кислота
3.4.3 Изомерия карбоновых кислот
Общая формула гомологического ряда предельных одноосновных карбоновых кислот CnH2n+1COOH или CnH2nO2.
Для предельных одноосновных карбоновых кислот характерны изомерии:
углеродного скелета;
межклассовая (предельные одноосновные кислоты изомерны сложным эфирам).
Пример
Напишите по одному изомеру на каждый вид для вещества следующего строения
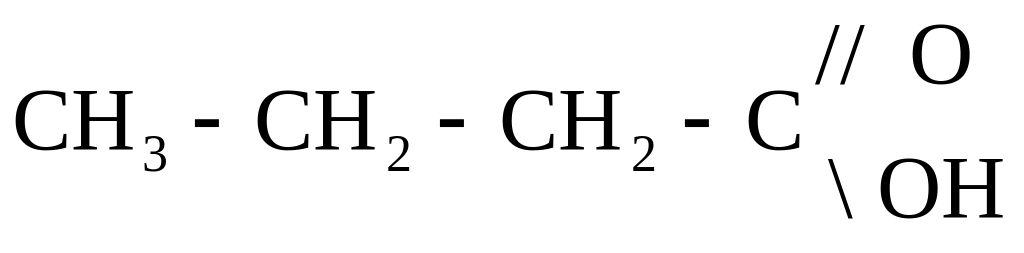
1 изомер – углеродного скелета – меняем строение, делаем углеродную цепь разветвленной
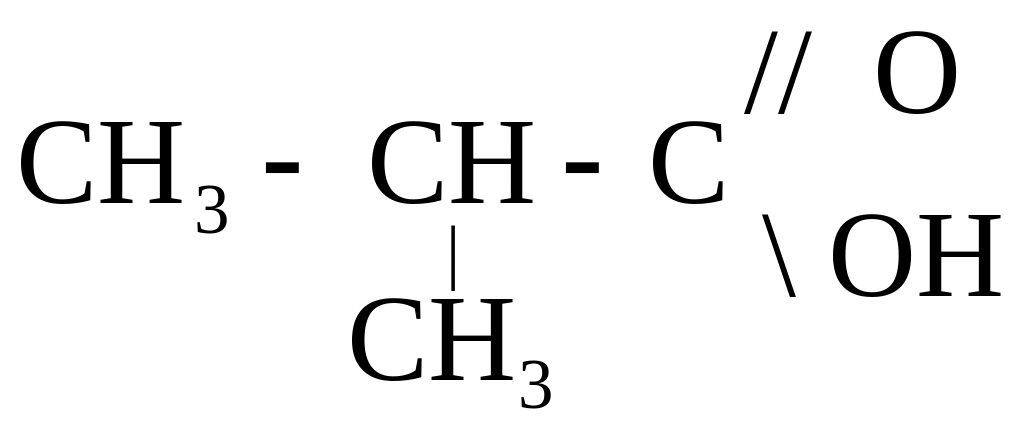 2-метилпропановая кислота
2-метилпропановая кислота
2 изомер – межклассовый – строим формулу сложного эфира, в составе которого 4 атома углерода
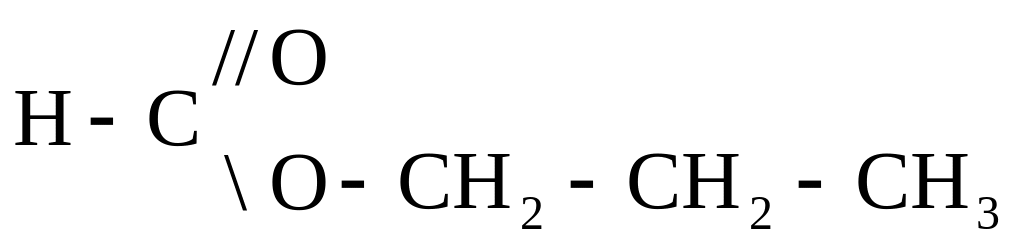 пропиловый эфир муравьиной кислоты
пропиловый эфир муравьиной кислоты
Общая формула гомологического ряда непредельных одноосновных карбоновых кислот
CnH2n-1COOH.
Для непредельных карбоновых кислот характерны изомерии:
углеродного скелета;
положения двойной связи.
3.4.4 Особенности химических свойств одноосновных карбоновых кислот
Химические свойства карбоновых кислот обусловлены наличием функциональной группы.
Все свойства карбоновых кислот можно подразделить на 5 групп:
реакции замещения водорода гидроксильной (–ОН) группы;
реакции замещения гидроксогруппы в карбоксильной группе;
реакции присоединения, идущие по карбоксильной группе;
Реакции отщепления;
реакции, обусловленные углеводородным радикалом.
Реакции замещения водорода
Карбоновые кислоты проявляют ярко выраженный кислотный характер, хотя более слабый, чем у минеральных кислот.
Подобно минеральным карбоновые кислоты способны образовывать соли с металлами, их оксидами и гидроксидами.
Например,
![]()
натриевая соль
карбоновой кислоты
2. Реакции замещения группы –ОН
Такой тип реакций приводит к образованию различных производных кислот.
а) взаимодействие с галогенидами фосфора приводит к образованию галогенангидридов кислот.
Например
![]()
хлорангидрид
кислоты
б) взаимодействие с аммиаком приводит к образованию аммонийной соли
![]()
аммонийная
соль кислоты
При сухой перегонке этих солей отщепляется молекула воды с образованием амидов кислот, последние при дальнейшем нагревании отщепляют еще молекулу воды, образуя нитрилы кислот.
![]()
амид кислоты нитрил кислоты
в) взаимодействие со спиртами в присутствии минеральных кислот приводит к образованию сложных эфиров (реакция этерификации)
![]()
сложный эфир
3.Реакции присоединения
Для карбоновых кислот характерно восстановление, при котором образуются альдегиды, способные восстанавливаться до спиртов.
![]()
альдегид спирт
Восстановительные свойства выражены только у муравьиной кислоты, поэтому она подобно альдегидам, является сильным восстановителем; для нее характерна реакция серебряного зеркала.
4.Реакции, обусловленные углеводородным радикалом
За счет подвижности водорода при α-углеродном атоме в углеводородном радикале предельные одноосновные карбоновые кислоты способны к реакциям замещения – галогенирование на свету.
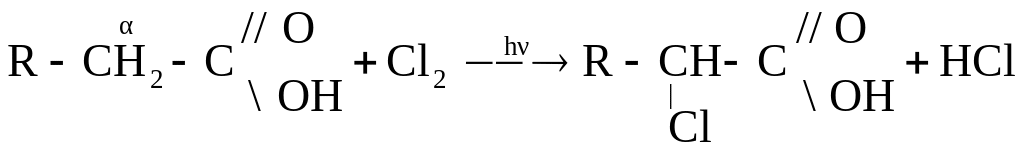
2-хлоркарбоновая кислота
За счет кратной связи в углеводородном радикале непредельные одноосновные карбоновые кислоты вступают в реакции, характерные для алкенов:
а) реакция присоединения – гидрирование, галогенирование, гидрогалогенирование, гидратация.
Присоединение сложных молекул к непредельным кислотам идет против правила Марковникова.
б) реакция окисления – окисление кислородом воздуха, раствором КМnO4.
в) полимеризация
