
- •Лекции по курсу биохимия и молекулярная биология для студентов направления биология
- •Оглавление
- •Введение
- •Модуль 1. Статическая биохимия
- •Лекция 1
- •Строение, свойства, биологическая роль
- •Моно – и олигосахаридов
- •Классификация углеводов
- •Моносахариды
- •Стереоизомерия моносахаридов
- •Представители моносахаридов
- •Олигосахариды
- •Отдельные представители дисахаридов
- •Лекция 2 строение, свойства, биологическая роль
- •Отдельные представители полисахаридов
- •Лекция 3 строение, свойства, биологическая роль простых липидов
- •Классификация
- •Стероиды
- •Желчные кислоты
- •Лекция 4 строение, свойства, биологическая роль сложных липидов
- •Лекция 5 аминокислотный состав белков Белки и их функции
- •Функции белков
- •Элементарный состав белков
- •Методы выделения и очистки белков
- •Аминокислотный состав белков
- •Химические свойства аминокислот
- •Классификация аминокислот, заменимые и незаменимые аминокислоты
- •Лекция 6 уровни структурной организации белков Структурная организация белков
- •Первичная структура белка: методы исследования. Структурные особенности пептидной связи
- •Номенклатура пептидов и полипептидов. Природные пептиды: глутатион, карнозин, ансерин, грамицидин s, окситоцин, энкефалины
- •Отдельные представители пептидов
- •Вторичная структура белков: -спираль, ее основные характеристики, -структура, -изгиб. Роль водородных связей в формировании вторичной структуры. Сверхвторичные (надвторичные) структуры белка
- •Третичная структура белков. Типы нековалентных связей, стабилизирующих третичную структуру. Роль s-s-мостиков в формировании третичной структуры некоторых белков
- •Заимодействия между субъединицами, стабилизирующие четвертичную структуру. Функциональное значение четвертичной структуры белков
- •Лекция 7
- •Физико-химические свойства белков
- •Ионизация, гидратация, растворимость,
- •Осмотические и онкотические свойства, оптические свойства
- •Молекулярная масса и размеры белков. Методы определения молекулярной массы белков. Необходимость применения комплекса методов для точной оценки молекулярной массы белков
- •Денатурация белков
- •Лекция 8 классификация белков. Простые и сложные белки Принципы классификации белков
- •Фибриллярные белки
- •Глобулярные белки
- •Сложные белки
- •Липопротеины
- •Гликопротеины
- •Протеогликаны
- •Фосфопротеины
- •Металлопротеины
- •Нуклеопротеины
- •Хромопротеины
- •Гемоглобин
- •Миоглобин
- •Цитохромы электронтранспортной цепи
- •Хлорофиллы
- •Флавопротеины
- •Лекция 9 сложные белки Гликопротеины
- •Фосфопротеины
- •Липопротеины
- •Металлопротеины
- •Лекция 10 строение, свойства, биологическая роль нуклеотидов
- •Циклические нуклеотиды
- •Лекция 11 строение, свойства, биологическая роль нуклеиновых кислот
- •Рибосомальные рнк
- •Лекция 12 витамины – биологическая роль, классификация. Водорастворимые витамины
- •Витамин в1 (тиамин)
- •Витамин в2 (рибофлавин)
- •Витамин в3 (рр, никотиновая кислота, никотинамид)
- •Витамин в5 (пантотеновая кислота)
- •Витамин в6 (пиридоксин, пиридоксаль, пиридоксамин)
- •Витамин в9 (фолиевая кислота)
- •Витамин в12 (кобалами)
- •Витамин н (биотин)
- •Витамин с (аскорбиновая кислота)
- •Витамин р (рутин)
- •Лекция 13 жирорастворимые витамины Витамин а (ретинол)
- •Витамин d (кальциферол)
- •Витамин е (токоферол)
- •Витамин к (нафтохинон)
- •Лекция 14
- •Ферменты – строение: свойства, механизм действия
- •Понятие о ферментах.
- •Сущность явлений ферментативного катализа
- •Структурная организация ферментов
- •3. Роль металлов в регуляции aктивности ферментов
- •Изоферменты: биологическая роль
- •Механизм действия ферментов
- •Специфичность действия ферментов
- •Стационарная кинетика ферментативных реакций
- •Концентрация субстрата
- •Концентрация фермента
- •Температура
- •Уравнение Михаэлиса-Ментен
- •Единицы ферментов
- •Лекция 15
- •Ингибиторы ферментов
- •Регуляция каталитичекой активности ферментов
- •Изостерическая регуляция
- •Аллостерический контроль активности ферментов
- •Регуляция ферментов ковалентной модификацией
- •Регуляция ферментов ограниченным протеолизом (активация зимогенов)
- •Регуляция активности мультиэнзимных комплексов
- •Классификация и номенклатура ферментов
- •Характеристика отдельных классов ферментов
- •Ферменты в клинической диагностике. Энзимопатии
- •Модуль II. Динамическая биохимия
- •Катаболические, анаболические, амфиболические пути
- •Метаболизм углеводов
- •Расщепление углеводов в пищеварительном тракте
- •Переваривание углеводов в ротовой полости
- •Переваривание углеводов в кишечнике
- •Амилолитические ферменты: характеристика Панкреатическая -амилаза
- •Сахаразо-изомальтазный комплекс
- •Гликоамилазный комплекс
- •Трегалаза
- •Всасывание моносахаридов в тонком кишечнике и их дальнейший транспорт. Глюкозные транспортеры
- •Всасывание моносахаридов в кишечнике
- •Транспорт глюкозы из крови в клетки
- •Лекция 17
- •Анаэробный катаболизм углеводов
- •Анаэробное окисление глюкозы. Гликолиз. Внутриклеточная
- •Локализация процесса
- •Отдельные реакции гликолиза, их термодинамические характеристики. Образование 2,3-дифосфоглицерата в шунте Рапопорта-Люберинга
- •Расщепление гликогена (гликогенолиз). Строение, механизм действия и регуляция гликогенфосфорилазы
- •Спиртовое и молочнокислое брожение
- •Лекция 18
- •Аэробный катаболизм углеводов (часть 1)
- •Аэробный метаболизм пирувата. Митохондрии: структура
- •И энергетические функции
- •Окислительное декарбоксилирование пирувата. Строение
- •Цикл лимонной кислоты. Отдельные реакции цикла, их термодинамическая характеристики. Суммарное уравнение окисления ацетил-CоА в цикле Кребса
- •Лекция 19
- •Аэробный катаболизм углеводов (часть 2)
- •Регуляция цикла Кребса на уровне цитратсинтазы,
- •Изоцитратдегидрогеназы и -кетоглутаратдегидрогеназного комплекса
- •Амфиболическое значение цикла Кребса. Необходимость анаплеротических путей, пополняющих запас компонентов, участвующих в цикле
- •Зависимое от атp и биотина карбоксилирование пирувата: анаплеротический путь синтеза оксалоацетата
- •Пентозофосфатный путь (гексозомонофосфатный шунт)
- •Отдельные реакции пфп, их термодинамические характеристики.
- •Суммарное уравнение пентозофосфатного пути.
- •Регуляция пентозофосфатного пути на уровне
- •Глюкозо-6-фосфатдегидрогеназы
- •Участки перекреста пфп с гликолизом
- •Циклический характер пфп
- •Лекция 20 биосинтез углеводов
- •Глюконеогенез
- •В последующей реакции, катализируемой ферментом фосфоенолпируваткарбоксикиназой, из оксалоацетата образуется фосфоенолпируват. Реакция Mg2-зависимая и донором фосфата служит gtp.
- •Лекция 21 расщепление пищевых и тканевых липидов
- •Катаболизм липидов
- •Всасывание продуктов расщепления липидов
- •Транспорт липидов
- •Метаболизм глицерола
- •Лекция 22 катаболизм жирных кислот
- •Активация жирной кислоты
- •Транспорт ацил-СоА в митохондрии
- •Катаболизм ненасыщенных жирных кислот
- •Катаболизм жирных кислот с нечетным числом атомов углерода
- •Образование кетоновых тел (кетогенез)
- •Кетоновые тела как источники энергии
- •Глиоксилатный цикл
- •Лекция 23 биосинтез жирных кислот и триацилглицеролов
- •Строение синтазы жирных кислот
- •Механизм синтеза жирных кислот
- •Транспорт ацетил-СоА из митохондрий в цитозоль
- •Образование малонил-СоА
- •Наращивание (элонгация) углеродной цепи жирной кислоты
- •Синтез других предельных и непредельных жк
- •Биосинтез триацилглицеролов
- •Лекция 24 биосинтез холестерола и желчных кислот
- •Биосинтез холестерола
- •Регуляция биосинтеза хс
- •Биосинтез желчных кислот
- •Лекция 25
- •Биологическое окисление. Ферменты, участвующие в биологическом окислении
- •Свободное окисление и его биологическая роль. Цитохром р-450
- •Микросомальная система окисления
- •Механизм гидроксилирования
- •Лекция 26
- •Цепь переноса электронов и протонов внутренней мембраны
- •Митохондрий (дыхательная цепь, редокс-цепь). Компоненты
- •Дыхательной цепи: флавопротеины, железосерные белки, коэнзим q, цитохромы в, с1, с, аа3. Топография дыхательных переносчиков
- •В редокс-цепи
- •Убихинон окисленный CoQ
- •Энергетическое значение ступенчатого транспорта электронов от окисляемых субстратов к молекулярному кислороду. Окислительное фосфорилирование в дыхательной цепи
- •Организация компонентов дыхательной цепи в виде четырех
- •Локализация пунктов сопряжения окисления и фосфорилирования в дыхательной цепи на основании редокс-потенциалов, действия специфических ингибиторов (ротенон, амитал, антимицин а, цианид, со, NaN3)
- •Полные и редуцированные дыхательные цепи
- •Лекция 27
- •Строение атp-синтазного комплекса. Механизм образования атp. Обратимость реакции, катализируемой атp-синтазой. Разобщение транспорта электронов и синтеза атp; действие 2,4-динитрофенола
- •Механизм образования атp
- •Окисление цитоплазматического nadh в дыхательной цепи. Глицеролфосфатный и малат-аспартатный челночные механизм
- •Лекция 28 интеграция клеточного метаболизма
- •Основные аспекты регуляции метаболизма
- •Регуляция на уровне транскрипции
- •Аллостерическая регуляция активности ферментов
- •Ковалентная модификация ферментов
- •Гормональная регуляция
- •Посттранскрипционная и посттрансляционная модификация макромолекул
- •Изменение концентрации метаболитов
- •Мембранная регуляция
- •Модуль III. Молекулярная биология лекция 29 репликация днк
- •Точность репликации
- •Репликация днк у эукариот
- •Репаративный синтез днк
- •Лекция 30 транскрипция (биосинтез рнк)
- •Транскрипция у прокариот
- •Инициация транскрипции
- •Элонгация транскрипции
- •Терминация транскрипции
- •Транскрипция у эукариот
- •Механизм индукции на примере Lac-оперона
- •Катаболитная репрессия
- •Лекция 31 тРансляция (биосинтез белка)
- •Роль тРнк в трансляции
- •Аминоацил-тРнк-синтетазы
- •Белоксинтезирующая система клетки
- •Эффективность трансляции
- •Точность белкового синтеза
- •Энергетические затраты на трансляцию
- •Посттрансляционные модификации полипептидной цепи
- •Библиографический список Основная литература
- •Дополнительная литература
Лекция 21 расщепление пищевых и тканевых липидов
Пищевые липиды являются источниками высших жирных кислот, глицерола, аминоспиртов и некоторых других соединений, используемых организмом для синтеза свойственных для него структурных или резервных липидов. Свободные жирные кислоты, наряду с глицеролом и аминоспиртами образуются в организме также при расщеплении резервных или структурных липидов. Еще одним источником высших жирных кислот может служить их синтез из ацетил-СоА, который в свою очередь может быть промежуточным продуктом обмена углеводов или аминокислот (рис.21.1).

Рис. 21.1. Схема ключевых процессов липидного обмена
Одним из ключевых метаболитов липидного обмена является ацетил-СоА, поскольку, во-первых, именно через это соединение осуществляется окислительное расщепление высших жирных кислот; во-вторых, через ацетил-СоА атомы углерода жирных кислот могут быть использованы для пластических целей – для синтеза холестерола или полипреноидов; в третьих, через ацетил-СоА в гепатоцитах углеродные цепи жирных кислот преобразуются в кетоновые тела – гидрофильные «топливные» молекулы, легко транспортируемые в клетки различных органов и тканей; в четвертых, через ацетил-СоА осуществляются метаболические превращения углеродных скелетов аминокислот и моносахаридов в жирные кислоты (ЖК), используемые в дальнейшем для синтеза сложных липидов.
Соединения других классов – аминокислоты и моносахариды – в ходе своего метаболизма образуют промежуточные продукты, которые могут в дальнейшем использоваться в клетке как для синтеза высших жирных кислот, так и для образования других мономерных единиц, необходимых для синтеза сложных липидов: глицерола, этаноламина, холина, сфингозина и пр. Таким образом, обмен липидов оказывается тесно связанным с обменом соединений других классов, а метаболические пути обмена липидов различных классов являются частью метаболической сети, функционирующей в организме.
С пищей в организм человека ежедневно поступает от 80 до 150 г липидов животного и растительного происхождения. В составе липидов в организм поступают полиеновые жирных кислот, которые не синтезируются в организме. Кроме того, с липидами в организм поступают и жирорастворимые витамины – А, D, E и К. Основная масса липидов представлена жирами или триацилглицеролами. Они, наряду с глюкозой служат главными источниками энергии. На долю жиров при рациональном питании приходится не более 30% от общего числа калорий, поступающих с пищей. В пожилом возрасте, а также при малой физической нагрузке потребность в жирах снижается; в условиях физической работы – увеличивается.
Катаболизм липидов
В расщеплении простых и сложных липидов принимают участие липолитические ферменты, относящиеся к классу гидролаз, а сам процесс расщепления липидов носит название липолиза. В организме животных до 90% липидов, поступающих с пищей, приходится на долю жиров. Переваривание жиров происходит в тонком кишечнике. Предварительно нерастворимые в воде жиры эмульгируются. Эмульгирование происходит под действием солей желчных кислот, которые попадают с желчью в просвет 12-перстной кишки. Желчные кислоты действуют как детергенты, располагаясь на поверхности капель жира и снижая поверхностное натяжение. В результате крупные капли жира распадаются на множество мелких, т.е. происходит эмульгирование. Из крупной капли жира образуется 1012 мелких капель.
Гидролиз жиров осуществляется панкреатической липазой. Панкреатическая липаза выделяется в полость тонкой кишки из поджелудочной железы (ПЖЖ) в виде неактивной пролипазы. Превращение в активную липазу происходит при участии желчных кислот и еще одного белка панкреатического сока - колипазы. Этот фермент, также секретируемый в виде зимогена, активируется при гидролизе трипсином специфических пептидных связей. Активная колипаза образует с липазой комплекс в молярном отношении 1:1 за счет формирования двух ионных связей Lys-Glu и Asp-Arg.
Колипаза своим гидрофобным доменом связывается с эмульгированным жиром. Другая часть молекулы колипазы способствует формированию такой конформации панкреатической липазы, при которой активный центр фермента максимально приближен к молекуле жира, поэтому скорость гидролиза жира резко возрастает (рис.21.2).
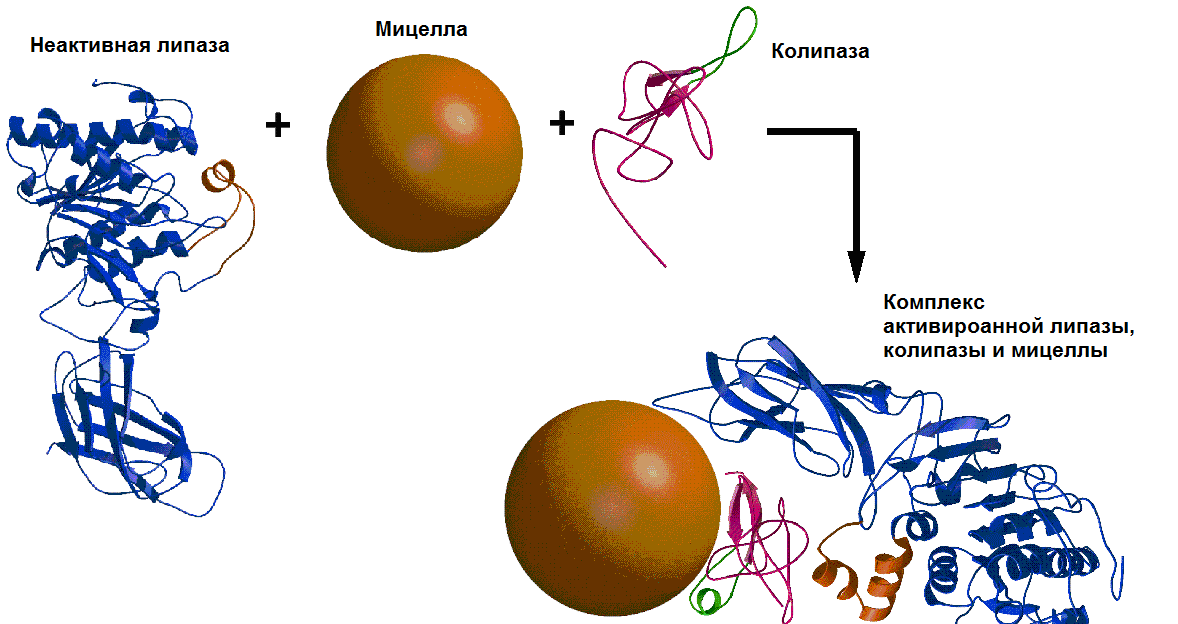
Рис.21.2. Взаимодействие неактивной панкреатической липазы, смешанной мицеллы и колипазы
Панкреатическая липаза гидролизует жиры преимущественно в 1 и 3 позициях (внешние сложноэфирные связи), поэтому основными продуктами гидролиза являются свободные ЖК и β-моноацилглицерол (2-моноацилглицерол, 2-МАГ). Молекулы 2-МАГ также обладают детергентными свойствами и способствуют эмульгированию жира.

β-Моноацилглицеролы всасываются стенкой кишечника и либо участвуют в ресинтезе триацилглицеролов уже в кишечной стенке, либо распадаются до глицерола и высшей жирной кислоты под действием неспецифических эстераз.

На скорость катализируемого липазой гидролиза триацилглицеролов не оказывает существенного влияния ни степень ненасыщенности жирной кислоты, ни длина ее цепи (от С12 до С18).
У растений в семенах и вегетативных органах присутствуют липазы, специфичность которых не выявлена. В дрожжевых грибках найдена липаза, способная отщеплять жирную кислоту как из α-, так и β-позиции.
Общепринято деление липаз на простые липазы, катализирующие гидролиз свободных триацилглицеролов, и липопротеинлипазы, гидролизирющие связанные с белками липиды.
Глицерофосфолипиды расщепляются под действием фосфолипаз. Существует четыре типа этих ферментов: фосфолипаза А1, А2, С и D. Фосфолипаза А1 отщепляет остаток жирной кислоты у С1 атома. Фосфолипаза А2 расщепляет β-сложноэфирную связь, фосфолипаза С отщепляет полярную головку вместе с остатком фосфорной кислоты, при этом продуктами гидролиза являются 1,2-диацилглицерол и фосфохолин. Фосфолипаза D, встречающаяся главным образом у растений, катализирует отщепление от фосфолипида полярной группы (азотистого основания) с образованием в качестве продукта фосфатидной кислоты (рис.21.3):

Рис.21.3. Расщепление сложноэфирных связей фосфолипазами
Фосфолипаза А2 (ФЛА2) гидролизует глицерофосфолипиды с образованием лизофосфолипидов. Лизофосфолипиды – эффективные эмульгаторы жира. Они, в свою очередь, под действием лизофосфолипазы, гидролизующей сложноэфирную связь у С1 атома, расщепляются на жирную кислоту и глицерофосфохолин, который хорошо растворяется в водной среде и всасывается из кишечника в кровь. Глицерофосфохолин также может расщепляться гидролазой до глицерол-3-фосфата и холина. ФЛА2 – неактивна, активируется путем частичного протеолиза, нуждается в Са2+.
Холестерол в пищевых продуктах содержится частично в свободном (неэстерифицированном) виде, частично в виде эфиров с жирными кислотами. Эфиры холестерола гидролизуются под действием особого фермента холестеролэстеразы, который синтезируется в ПЖЖ и секретируется в кишечник. Продуктами гидролиза являются свободный холестерол (ХС) и ЖК. Активность фермента проявляется в присутствии желчных кислот.

+ Н2О → СН3(СН2)14СООН
+

холестерол
Рис. 21.4. Гидролиз пальмитохолестерида холестеролэстеразой
