
- •Молекулярная физика и термодинамика
- •Макроскопические состояния Макроскопические параметры.
- •Основное уравнение молекулярно-кинетической теории.
- •Уравнения состояния идеального и реального газов
- •Функции состояния. Внутренняя энергия. Число степеней свободы молекулы
- •Основы термодинамики Термодинамические процессы. Работа и количество теплоты. Теплоемкость
- •Первое начало термодинамики. Адиабатный процесс
- •Обратимые и необратимые процессы. Тепловые машины. Цикл Карно. Неравенство Клаузиуса
- •Энтропия. Теорема Карно
- •Второе начало термодинамики. Третье начало термодинамики (тепловая теорема Нернста)
- •Статистические распределения Распределение молекул газа по скоростям. Распределение Максвелла. Распределение Больцмана
- •Флуктуации. Микросостояния и вероятность макросостояния. Термодинамическая вероятность и энтропия
- •Элементы физической кинетики
- •Элементарная теория явлений переноса. Диффузия. Теплопроводность. Внутреннее трение (вязкость)
- •Фазовые равновесия и фазовые превращения. Фазы и фазовые равновесия. Фазовые диаграммы.
- •Фазовые переходы первого и второго рода. Уравнение Клапейрона-Клаузиуса. Изотермы Ван-дер-Ваальса
Первое начало термодинамики. Адиабатный процесс
Выражением закона сохранения и превращения энергии в термодинамических процессах является первое начало термодинамики - обобщение многочисленных экспериментальных результатов: изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме совершенной над системой (затраченной) работы dА’ и сообщенной ей теплоты dQ: dU = dA’ + dQ.
Если вместо совершенной над системой работы dA’ ввести равную ей по величине, но противоположную по знаку работу dA, совершенную системой над внешними телами ( dA = - dA’), то тогда первое начало термодинамики можно сформулировать следующим образом: сообщаемая системе теплота расходуется на увеличение ее внутренней энергии и на совершение системой работы против внешних сил.
dQ = dU + dA.
В интегральной форме первое начало термодинамики может быть представлено в следующем виде:
Q = A + DU.
Когда система представляет собой периодически действующую машину, в которой газ или пар, или другое “рабочее тело” в результате некоторого процесса периодически возвращается в исходное состояние, DU = 0 и Q = A - работа машины равна подведенной извне теплоте. Отсюда можно первое начало термодинамики сформулировать следующим образом: нельзя построить периодически действующую машину, которая совершала бы работу большую, чем количество сообщенной извне энергии. То есть вечный двигатель первого рода невозможен.
Все физические величины, входящие в первое начало термодинамики, могут быть как положительными, так и отрицательными. Если к системе подводится теплота, то dQ > 0, если отводится, то dQ < 0. Если система совершает работу, то dA > 0, если же внешние тела совершают работу над системой, то dA < 0. В качестве примера применения первого начала рассмотрим ряд известных процессов.
1. Изохорный процесс (V = const). dA = pdV = 0, так как dV = 0 из-за V = const, то есть А = 0. Тогда dQ = dU. Если СVмол - молярная теплоемкость при постоянном объеме, то dU = nСVмолdT.
2. Изобарный процесс (p = const). dQ = CРмолndT, где CРмол - молярная теплоемкость при постоянном давлении. С другой стороны dQ = dA + dU, тогда
CРмолndT = dA + nСVмолdT = pdV + nСVмолdT. Из уравнения Клапейрона-Менделеева при p = const следует что pdV = nRdT, тогда CРмолndT = nСVмолdT + nRdT, или CРмол = СVмол + R. Найдем работу A12 = pdV = p(V2 - V1). Так как pdV = nRdT, то A12 = nR(T2 -T1).
3. Изотермический процесс (Т = const). dU = 0, так как T = const и dT = 0. Тогда dQ = dA = pdV. При изотермическом процессе внутренняя энергия идеального газа не меняется, поэтому все подводимое тепло идет на совершение работы: dQ = dA = pdV.
4. Адиабатный процесс - процесс, происходящий в системе без теплообмена с внешней средой (dQ = 0). В реальных условиях этот процесс можно провести двумя способами:
а) провести процесс быстро, чтобы теплообмен не успел произойти;
б) изолировать систему от внешней среды.
Тогда: dU + dA = 0 или nСVмолdT = - pdV.
Замечание. При адиабатическом расширении (dV > 0) газ охлаждается, а при адиабатическом сжатии (dV < 0) газ нагревается.
Найдем уравнение адиабатного процесса. Используем уравнение Клапейрона-Менделеева, взяв дифференциал левой и правой частей: pdV + Vdp = nRdT. Из первого начала термодинамики: dT = - pdV/(nСVмол), тогда pdV + Vdp =
= - nRpdV/(nСVмол) или (R/СVмол + 1)pdV + Vdp = (CРмол/СVмол)pdV + Vdp = 0. Разделив на pV, получим (CРмол/СVмол)dV/V + dp/p = 0. Введем обозначение
g = CРмол/СVмол . После интегрирования получим: g lnV + lnp = const. Пропотенцировав это выражение, получим уравнение Пуассона (уравнение адиабаты):
pVg = const.
Используя уравнение Клапейрона-Менделеева, уравнение адиабаты можно записать в других переменных: TV(g-1) = const или Tgp(1-g) = const. На графике в координатах p, V адиабата идет круче, чем изотерма, и спадает более быстро (рис. 4,б).
При изотермическом процессе работа совершается за счет подводимого извне тепла (dT = 0). При адиабатическом процессе первое начало термодинамики имеет вид: dQ = dA + dU = 0, dU = - dA = - pdV = nСVмолdT, тогда работу при адиабатическом процессе можно записать и так:
A12 = dA = - nСVмолdT = -nСVмол (T2 – Т1) = -DU12 = U1 – U2.
При адиабатическом процессе система осуществляет работу за счет внутренней энергии.
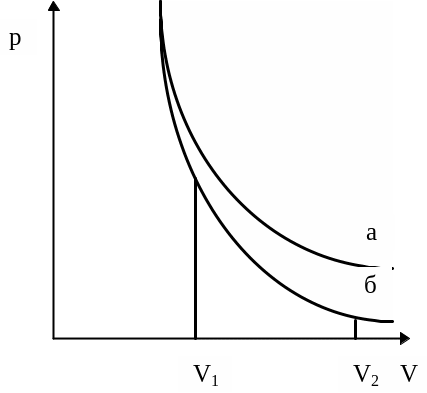
Рис. 4. Термодинамические процессы: а - изотермический, б - адиабатный
