
- •Синтез и исследование свойств нанокатализаторов на углеродном носителе
- •Часть 1 Синтез нанокатализаторов на углеродном носителе
- •Экспериментальная часть
- •Оборудование и материалы:
- •Требования безопасности
- •Порядок выполнения работы
- •Содержание отчета
- •Контрольные вопросы
- •Часть 2 Определение размера частиц методом Шеррера
- •Содержание отчета
- •Контрольные вопросы
Синтез и исследование свойств нанокатализаторов на углеродном носителе
Часть 1 Синтез нанокатализаторов на углеродном носителе
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
Цель работы – сравнение эффективности различных восстановителей для жидкофазного синтеза наноразмерных электрокатализаторов.
В настоящее время человечество сталкивается со следующими экологическими проблемами: смог, парниковый эффект, озоновые дыры, кислотные дожди и т.д. [1]. Причиной большинства из них является массированное загрязнение окружающей среды в результате не рационального природопользования. Основные выбросы вредных компонентов возникают в ходе горения топлива (рис.1).
Следует отметить, что процессы преобразования химической энергии в электрическую характеризуется невысокими значениями КПД (20-30%). Вместе с тем известны способы преобразования энергии, например, электрохимический, практически лишенный указанных недостатков. Осуществляется он в топливных элементах (ТЭ) [2].
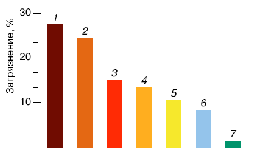
Рис. 1 Доли загрязнений атмосферы различными отраслями техники в России: 1 – теплоэнергетика, 2 – черная металлургия, 3 – нефтедобыча и нефтепереработка, 4 – автотранспорт, 5 – цветная металлургия, 6 – промышленность стройматериалов, 7 – химическая промышленность.
Топливный элемент – это устройство, в котором химическая энергия топлива и окислителя, непрерывно подводимых к электродам, превращается непосредственно в электрическую. В тепловых машинах процесс преобразования энергии проходит через несколько промежуточных стадий (рис.2).
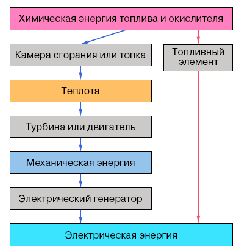
Рис. 2 Ступени преобразования химической энергии традиционным и электрохимическим способами.
В качестве топлива обычно используют водород, реже СО или СН4, окислителем является кислород воздуха. ТЭ бывают двух типов:
1. низкотемпературные - t< 200 oC, топливо – водород или метанол, катализатор – Pt и ее сплавы;
2. высокотемпературные - t> 500 oC, топливо – водород, СО, СН4, электролиты – расплавы солей или твердый электролит, катализаторы – никель/хром, литированный оксид никеля, сложные смешанные оксиды циркония-лантана и др.
Рассмотрим для примера работу кислородно-водородного ТЭ со щелочным электролитом (раствором КОН).
Реакция окисления воды:
2H2 + O2 → 2H2O (1)
В ТЭ протекает через электроокисление водорода на аноде:
2H2 + 4OH - - 4e → 4H2O (2)
и электровосстановление кислорода на катоде:
O2 + 2H2O + 4e → 4OH - (3)
В результате реакции (1) во внешней цепи протекает электрический ток, т.е. происходит прямое преобразование химической энергии в электрическую.
ЭДС для ТЭ можно рассчитать по уравнениям химической термодинамики (4):
![]() (4)
(4)
где Еэ – ЭДС, Gх.р. – изменение энергии Гиббса в результате протекания химической реакции, n – число электронов на молекулу реагента, F – постоянная Фарадея (96 484 Кл/моль). Так для реакции (1) - Еэ, 298 = 1,23 В.
Так как процесс преобразования энергии не имеет промежуточной стадии генерации теплоты (см. рис.2), то для электрохимического способа нет ограничений цикла Карно и теоретический КПД преобразования энергии можно рассчитать по формуле:
![]() (5),
(5),
где Нх.р. – изменение энтальпии в результате протекания химической реакции (тепловой эффект реакции). Например, для метана Т = 1,0, а для водорода Т =0,94.
Реальный КПД р ТЭ ниже теоретического и определяется по уравнению:
![]() (6),
(6),
где nр – реальное число электронов на молекулу реагента, U – напряжение ТЭ.
У большинства ТЭ напряжение лежит в пределах 0,809 В. От величины напряжения зависит мощность ТЭ:
P = U I.
Принципиальная схема ТЭ представлена на рисунке 3. Топливные элементы, как и другие химические источники тока (гальванические элементы и аккумуляторы), состоят из анода, катода и ионного проводника (электролита) между ними. Основное отличие ТЭ от гальванического элемента заключается в том, что в ТЭ используются не расходуемые электроды, поэтому ТЭ могут работать длительное время (до нескольких десятков тысяч часов). Реагенты в ТЭ поступают во время работы, а не закладываются заранее, как в гальванических элементах и аккумуляторах. В отличие от аккумуляторов ТЭ не требуют подзарядки.
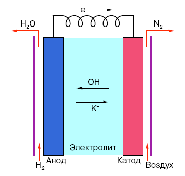
Рис. 3 Принципиальная схема ТЭ.
В процессе работы характеристики ТЭ постепенно ухудшаются, что обусловлено дезактивацией и износом катализаторов, коррозией основ электродов, изменением структуры электродов и другими причинами. Это сокращает их срок службы. Для увеличения срока службы ТЭ применяют химически стойкие катализаторы (платиновые металлы и оксиды некоторых металлов) и основы электродов (графит и никель). Некоторые ТЭ могут работать до 40 тыс. часов. Согласно прогнозам в скором будущем энергоустановки на основе ТЭ будут вносить существенный вклад в генерацию энергии и решении экологических проблем транспорта и энергетики.
