
- •I. Общие положения
- •II. Комплекты измерительных материалов
- •2.1. Комплект измерительных материалов текущего контроля (Контрольная точка 1)
- •1. Паспорт оценочных средств контрольной точки № 1
- •2. Форма текущего контроля и процедура оценивания
- •Система и критерии оценок результатов текущей аттестации
- •4. Пакет заданий
- •Условия выполнения задания
- •5. Эталон ответов Вариант №1
- •Вариант № 2
- •Вариант № 3
- •Вариант №4
- •Вариант №5
- •Вариант№6
- •Задачи повышенной сложности
- •II. Комплекты измерительных материалов
- •2.2. Комплект измерительных материалов текущего контроля (Контрольная точка 2)
- •1. Паспорт оценочных средств контрольной точки № 2
- •Форма текущего контроля и процедура оценивания
- •Система и критерии оценок результатов текущей аттестации
- •4. Пакет заданий Условия выполнения задания
- •Эталон ответов
- •7. Протокол результатов текущего контроля
- •2.N. Комплект измерительных материалов промежуточного контроля
- •1. Паспорт оценочных средств промежуточного контроля
- •2. Форма промежуточного контроля и процедура оценивания
- •3. Система и критерии оценок результатов промежуточной аттестации
- •4. Пакет заданий
- •4.1. Теоретические задания теоретическое задание (тз) № 1-n
- •4.2. Практические задания практическое задание (пз) № 1-n
- •5. Бланк ответов (для тестов)
- •6. Эталон ответов (ключ или решение)
- •7. Протокол результатов промежуточного контроля
- •Зачетная ведомость
Задачи повышенной сложности
Задача 1
Дано
m (Mg+примеси) – 6г
V (Н2) – 4,48л
ω(примеси) -?
Решение
1.Напишем уравнение реакции. Над уравнением запишем имеющиеся данные, под уравнением – число молей
4,48л
Mg + H2SO4 = MgSO4 + H2
1 моль 1 моль
2.Находим по периодической системе молярную массу магния
M(Mg)=24г/моль
Молярный объем газа Vm=22,4л/моль
3.Определяем количество вещества водорода, которое содержится в 4,48л водорода по формуле
Y
=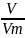 Y(Н2)
=
Y(Н2)
=
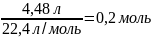
4. Находим количество вещества магния, необходимого по уравнению реакции.
Составляем пропорцию
1моль Mg – 1моль Н2
X моль Mg – 0,2 моль Н2
x = 0,2 моль
5.Находим массу магния по формуле
m = M * Y
где M – молярная масса
Y – количество вещества
m (Mg) = 24г/моль * 0,2 моль = 4,8г
6.Находим массу примесей
m (примеси) = 6г – 4,8г = 1,2г
7.Находим массовую долю примесей по формуле
ω
=
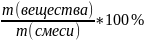
ω
(примеси) =
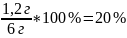
Ответ: ω (примеси) = 20%
Задача 2
Дано
m (СаО) – 5,6г
m (раствор 10% Н2SО4) – 200г
m(СаSО4) -?
Решение
1.Напишем уравнение реакции. Над уравнением запишем имеющиеся данные, под уравнением – число молей
5,6г
СаО + Н2SО4 = СаSО4 + Н2О
1 моль 1моль 1 моль
2.Находим молярные массы оксида кальция, серной кислоты, сульфата кальция
M(CаО) = 40 + 16 =56 г/моль
M(Н2SO4) = 1 * 2 + 32 + 16 * 4 = 98г/моль
М(СаSО4) = 40 + 32 + 64 = 136г/моль
3.Находим массу серной кислоты, которая содержится в 200г раствора
m(Н2SО4) = 200г * 0,1 = 20г
4.Находим количество вещества оксида кальция и серной кислоты
Y(СаО)
=
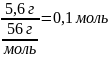
Y(Н2SО4)
=
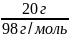 = 0,2моль
= 0,2моль
5.Находим какое из веществ, вступивших в реакцию, дано в избытке, а какое – в недостатке
0,1моль СаО – х моль Н2SО4
1 моль СаО – 1 моль Н2SО4
х = 0,1 моль Следовательно, СаО дан в недостатке, расчет ведем по нему
6.Находим количество вещества сульфата кальция
0,1 моль СаО – х моль СаSО4
1 моль СаО – 1 моль СаSО4
х = 0,1 моль
7.Находим массу сульфата кальция
m (СаSО4) = 136г/моль * 0,1 моль = 13,6г
Ответ: m(СаSО4) = 13,6г
II. Комплекты измерительных материалов
2.2. Комплект измерительных материалов текущего контроля (Контрольная точка 2)
1. Паспорт оценочных средств контрольной точки № 2
В результате оценки осуществляется проверка следующих объектов:
Таблица 22
Объекты оценивания |
Показатели |
Критерии |
Тип задания3
|
Форма аттестации
|
знать: Предмет органической химии; Основные положения теории химического строения А.М. Бутлерова; Классификацию органических соединений; Классификацию реакций в органической химии. Общую формулу алканов, алкенов, алкинов, диеновых углеводородов, гомологические ряды алканов, алкенов, алкинов, диеновых углеводородов; Понятие гомологов и изомеров; Правила систематической номенклатуры (ИЮПАК) для алканов, алкенов, алкинов, диеновых углеводородов; Свойства и практическое значение алканов, алкенов, алкинов, диеновых углеводородов уметь: Составлять структурные формулы алканов, алкенов, алкинов, диеновых углеводородов; Называть по систематической номенклатуре; Составлять уравнения реакций, характеризующих химические свойства алканов и непредельных углеводородов; Определять по характерным реакциям непредельные углеводороды; Решать задачи на нахождение химических формул органических веществ |
Изложение содержания основных положений теории химического строения органических веществ А.М. Бутлерова
Написание общих и конкретных формул алканов, алкенов, алкинов, диеновых углеводородов
Изложение содержания понятий гомологов и изомеров
Составление структурных формул алканов, алкенов, алкинов, диеновых углеводородов
Составление названий алканов, алкенов, алкинов, диеновых углеводородов по структурной формуле
Написание уравнений реакций химических свойств алканов и непредельных углеводородов Решение задач на нахождение химических формул органических веществ
|
Даны правильные формулировки положений теории химического строения органических веществ А.М. Бутлерова в соответствии с эталоном
Правильные записи формул в соответствии с эталоном
Даны правильные определения понятиям в соответствии с эталоном
Правильные Записи структурных формул в соответствии с эталоном
Правильные записи названий углеводородов по систематической номенклатуре в соответствии с эталоном
Правильные записи уравнений реакций в соответствии эталоном
Правильное решение задач в соответствии эталоном |
\
Теоретические и практические задания
|
Тестовый контроль |
