
- •I. Общие положения
- •II. Комплекты измерительных материалов
- •2.1. Комплект измерительных материалов текущего контроля (Контрольная точка 1)
- •1. Паспорт оценочных средств контрольной точки № 1
- •2. Форма текущего контроля и процедура оценивания
- •Система и критерии оценок результатов текущей аттестации
- •4. Пакет заданий
- •Условия выполнения задания
- •5. Эталон ответов Вариант №1
- •Вариант № 2
- •Вариант № 3
- •Вариант №4
- •Вариант №5
- •Вариант№6
- •Задачи повышенной сложности
- •II. Комплекты измерительных материалов
- •2.2. Комплект измерительных материалов текущего контроля (Контрольная точка 2)
- •1. Паспорт оценочных средств контрольной точки № 2
- •Форма текущего контроля и процедура оценивания
- •Система и критерии оценок результатов текущей аттестации
- •4. Пакет заданий Условия выполнения задания
- •Эталон ответов
- •7. Протокол результатов текущего контроля
- •2.N. Комплект измерительных материалов промежуточного контроля
- •1. Паспорт оценочных средств промежуточного контроля
- •2. Форма промежуточного контроля и процедура оценивания
- •3. Система и критерии оценок результатов промежуточной аттестации
- •4. Пакет заданий
- •4.1. Теоретические задания теоретическое задание (тз) № 1-n
- •4.2. Практические задания практическое задание (пз) № 1-n
- •5. Бланк ответов (для тестов)
- •6. Эталон ответов (ключ или решение)
- •7. Протокол результатов промежуточного контроля
- •Зачетная ведомость
Вариант №4
Электролитическая диссоциация – это распад электролита на ионы в растворах или расплавах.
-Взаимодействие хлора с простыми веществами.
а) с неметаллами
Cl2 +H2 → 2HCl
б) с металлами
Ca + Cl2 → CaCl2
-Взаимодействие со сложными веществами
а) с водой
Cl2 +H2 O → HCl + HClO
3. Ca → CaO → Ca (OH)2 → CaCl2
1) 2 Ca + O2 → 2 CaO
2) CaO + H2 O → Ca ( OH)2
CaO + H2 O → Ca2+ + 2OH1-
3) Ca (OH)2 + 2HCl → Ca Cl2 + 2H2O
Ca2+ + 2 OH1- + 2 H1+ + 2Cl1- ⇄ Ca2+ + 2 Cl1- + 2H2 O
2H1+ + 2 OH1- ⇄ 2 H2 O
4 .Дано: Решение:
H
2,N2
D (N2)
=
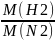
D(N2) - ? M(H2 ) = 2
M (N2) = 28
D
(N2)
=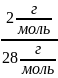 = 0,07
= 0,07
Ответ: D(N2) – 0,07
Вариант №5
Электролиз - это окислительно - восстановительные реакции, протекающие на электродах при прохождении электрического тока через раствор или расплав электролита.
-Взаимодействие кислорода с простыми веществами
а) с неметаллами
2H2 + O2 → 2H2 O
S + O2 → SO2
б) с металлами.
2Ca + O2 → 2CaO
- Со сложными веществами
а) с оксидом серы (IV)
2SO2 + O2 → 2SO3
3.
Cu Cl 2 ( Cu (OH)2 , HCL)
Слабое основание сильная кислота
Cu Cl2 ⇄ Cu2+ + 2Cl1-
H2 O ⇄ H1+ + OH1-
Cu2+ + 2 Cl1- + H1+ OH1- ⇄ CuOH1+ +2 Cl1- + H1+ (кислая среда)
Cu2+ + H1+ + OH1-⇄ CuOH1+ + H1+
CuCl2 + H2 O ⇄ CuOHCl + HCL
4.Дано: Решение:
V
(N2
) – 11,2л
V m =
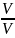 ; V m = 22,4
; V m = 22,4
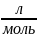
𝒱(N2
) - ? 𝒱(N2)=
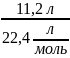 =
0,5 моль
=
0,5 моль
Ответ: 𝒱 (N2)- 0,5 моль
Вариант№6
Гидролиз соли – реакция обмена между солями и водой , ведущая к образованию слабого электролита.
-Взаимодействие углерода с простыми веществами
а) с неметаллами
C+O2 → CO2
C+2H2 → CH4
б) с металлами
4Al + 3C → Al4 C3
-Взаимодействие со сложными веществами
2Fe2 O3 + 3C → 4 Fe + 3CO2
1 2 3
3. Cl2 → HCl → Na Cl → Ag Cl
1.) Cl2 +H2 → 2HCl
Cl2 + H 2 ⇄ 2 H1+ + 2 Cl1-
2.) HCl + Na OH → NaCl+ H2 O
H1+ +Cl1- + Na1+ + OH1- ⇄ Na1+ + Cl1- + H2 O
H1+ + OH1- ⇄ H2 O
3) Na Cl + AgNO3 → Na NO3 + AgCl ↓
Na1+ + Cl1- + Ag1+ + NO31 ⇄ Na1+ + NO31- + Ag Cl↓
Ag1+
+ Cl1-
⇄ Ag
Cl
4. Дано Решение
Д
( возд) = 1,103 Д (возд) =
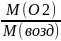 ;
;
М(возд)
- ? М (возд) =
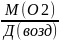 = =
= =
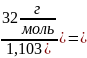 29
29
Ответ М(возд) = 29
