
- •ОрГанИческая химия методические указания и задания для выполнения контрольнЫх работ для студентов, обучающихся по заочной форме специальности
- •240134 Переработка нефти и газа
- •Рассмотрена
- •Содержание
- •2. Рабочая программа учебной дисциплины
- •2.1. Паспорт рабочЕй программы учебной дисциплины Органическая химия
- •2.1.1. Область применения рабочей программы
- •2.1.3. Цели и задачи учебной дисциплины – требования к результатам освоения учебной дисциплины:
- •2.1.4. Рекомендуемое количество часов на освоение рабочей программы учебной дисциплины: Органическая химия
- •2.2. Структура и содержание учебной дисциплины
- •2.2.1. Объем учебной дисциплины и виды учебной работы
- •2.2.2. Тематический план и содержание учебной дисциплины _____Органическая химия_______
- •2.3. Условия реализации учебной дисциплины
- •2.3.1. Требования к минимальному материально-техническому обеспечению
- •2.3.2. Информационное обеспечение обучения
- •3. Методические указания по изучению учебного материала по теме Введение
- •Вопросы для самоконтроля
- •Методические указания по теме 1.1. Общие вопросы теории химического строения органических веществ.
- •Решение:
- •Вопросы для самоконтроля
- •Установление формул веществ по их плотности и количественному составу
- •Решение:
- •Решение:
- •Установление молекулярных формул веществ по продуктам сгорания
- •Решение:
- •Установление молекулярных формул веществ по их общим формулам
- •Решение:
- •Вопросы для самоконтроля
- •Вопросы для самоконтроля
- •Методические указания по теме 2.2. Циклоалканы
- •Вопросы для самоконтроля
- •Методические указания по теме 2.3. Алкены
- •Решение:
- •Вопросы для самоконтроля
- •Методические указания по теме 2.4. Алкины
- •В результате перекрывания гибридных sp3 – орбиталей атома углерода и s – орбиталей четырех атомов водорода образуется молекула метана с прочными
- •В молекуле этана сн3-сн3 образованной из двух углеродных тетраэдров количество орбиталей равно:
- •Рассмотрим задачу.
- •Решение:
- •Вопросы для самоконтроля
- •При изучении данной темы необходимо обратить внимание на:
- •Вопросы для самоконтроля
- •Методические указания по теме 2.7. Нефть и продукты её переработки
- •Вопросы для самоконтроля
- •Методические указания по теме 3.1. Галогенопроизводные
- •Рекомендации к написанию формул, уравнений и схем реакций
- •Вопросы для самоконтроля
- •Методические указания по теме 3.2. Гидроксильные соединения и их производные
- •Вопросы для самоконтроля
- •Методические указания по теме 3.3 Альдегиды и кетоны
- •Вопросы для самоконтроля
- •Методические указания по теме 3.4. Карбоновые кислоты и их производные. Липиды
- •Вопросы для самоконтроля
- •Методические указания по теме 3.5. Органические cоединения серы
- •Вопросы для самоконтроля
- •Методические указания по теме 3.8. Элементорганические соединения
- •Вопросы для самоконтроля
- •Методические указания по теме 4.1. Аминоспирты. Аминокислоты
- •Вопросы для самоконтроля
- •Методические указания по теме 4.2. Гетероциклические соединения
- •Вопросы для самоконтроля
- •Например:
- •Элементный анализ органических соединений
- •Общие вопросы теории химического строения органических веществ
- •Циклоалканы
- •Ароматические углеводороды
- •Галогенпроизводные
- •Гидроксильные соединения и их производные
- •Альдегиды и кетоны
- •Карбоновые кислоты и их производные
- •Нитросоединения
- •Органические соединения серы
- •Элементорганические соединения
- •Аминоспирты. Аминокислоты.
- •Гетероциклические соединения
- •5. Список вопросов к экзамену
Вопросы для самоконтроля
1. Каково современное представление о строении молекул бензола?
2. Чем определяется изомерия гомологов бензола?
3. Напишите формулы изомеров аренов состава С8Н10 и назовите их.
4. Напишите структурные формулы соединений:
4.1. n.– ксилола;
4.2. м. – метилизопропилбензола;
4.3. о. – диэтилбензола.
5. Объясните в чём сходство бензола с алканами и алкенами?
6. Напишите уравнения реакций получения из бензола орто- и пара-
хлортолуола. Объясните последовательность реакций на основе
правил ориентации.
Литература [ 1 ], с.100 –134
Методические указания по теме 2.7. Нефть и продукты её переработки
При изучении данной темы необходимо обратить внимание на особенности физических свойств нефти, на физические и химические методы переработки нефти.
Вопросы для самоконтроля
1. Почему нефть не имеет постоянной температуры кипения?
2. В чём сущность процесса перегонки нефти?
3. Какие наиболее важные фракции образуются при перегонке нефти?
4. Какие химические методы переработки нефти Вы знаете?
5. В чём сущность пиролиза нефти?
6. Каково значение нефти и нефтепродуктов в народном хозяйстве?
Литература [ 1 ], с.100 –134
Методические указания по теме 3.1. Галогенопроизводные
При изучении данной темы необходимо обратить внимание на правильность в написании формул, уравнений и схем реакций, характеризующих химические свойства монофункциональных соединений.
Рекомендации к написанию формул, уравнений и схем реакций
1. При выполнении упражнений необходимо обращать особое внимание на правильность написания структурных формул органических соединений. Удобнее всего использовать полуразвернутые (упрощенные) структурные формулы, в которых черточками указываются все связи между атомами, за исключением связей с атомами водорода. Формулы с горизонтально написанной углеродной цепью выгодно по возможности писать так, чтобы функциональные группы, находящиеся на конце цепей, располагались справа, а заместители у неконцевых атомов углерода – под или над углеродной цепью:
CH3
CH3 – CH – CH2 – Br CH3 – CH2 – CH – CH3
Br
CH3
CH3 – CH – CH3 – Br CH3 – CH2 – CH2 – CH2 – Br
Br
2. В начальных упражнениях с формулами ароматических соединений
в бензольных ядрах лучше писать все С – и Н – атомы. При упрощенном изображении бензольных колец замещающие атомы и группы необходимо отчетливо соединять с атомами бензольного ядра валентными черточками.
![]()
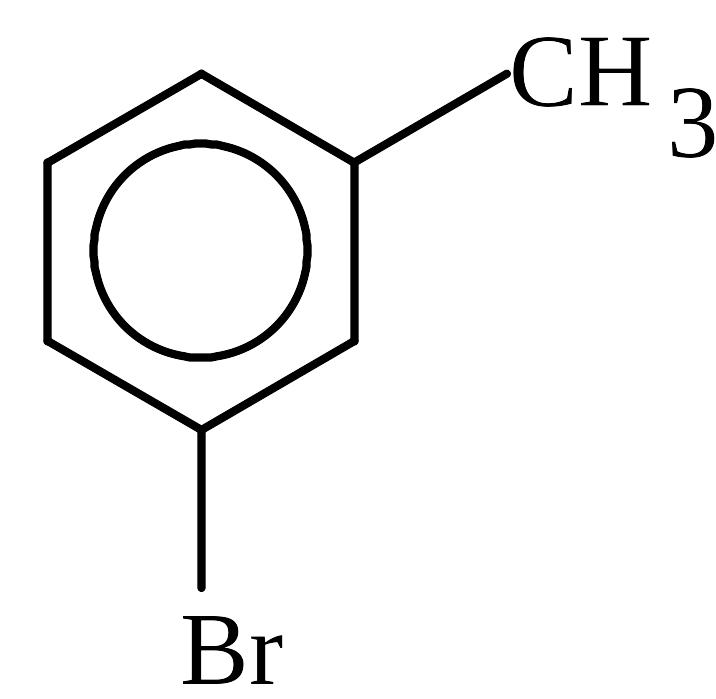
3. Органические реакции могут быть выражены уравнениями, в которых набирают коэффициенты и уравнивают количество атомов в правой и левой частях. Однако часто пишут не уравнения, а схемы реакций. Так поступают в тех случаях, когда процесс протекает одновременно в нескольких направлениях или через ряд последовательных стадий, например:
 CH3
– CH2
– CH2
– CI + HCI
CH3
– CH2
– CH2
– CI + HCI
CI2
 CH3
– CH2
– CH3
CH3
– CH2
– CH3
свет
СH3 – CH – CH3 + HCI
CI
или
NаOH, tC CuО, tC
CH3 – CH2 – CI ––––––– CH3 – CH2 – OH ––––– CH3 – CH = O
Как показано в приведенных примерах, схемах действующий реагент изображают над стрелкой. Для простоты коэффициенты в правой и левой частях схемы не уравнивают, а некоторые вещества, такие, как, например Cu, H2O, NaCI и т.д. образующиеся при реакциях, в схемах или совсем не показывают, или указывают под стрелкой со знаком минус. Направление превращений веществ в реакциях указывается стрелкой. Над стрелкой указывают реагенты и условия реакций, катализатор и т.п.
