
Глава II. Химическая термодинамика
§ 1. Первый закон термодинамики
Первый закон термодинамики есть закон сохранения энергии в применении его к термодинамическим процессам. Можно дать несколько, по существу равноценных, формулировок этого закона:
а) общая энергия изолированной системы остается постоянной независимо от каких бы то ни было изменений, происходящих в этой системе;
б) изменение внутренней энергии системы (ΔU) равно разности между количеством сообщенной системе теплоты q и количеством работы A, совершенной системой.
Математическое выражение первого закона термодинамики будет иметь вид:
ΔU= q - A (II, 1)
q— считается положительной, если теплота поглощается системой, и отрицательной, если теплота выделяется.
Из первого закона термодинамики вытекает ряд следствий, имеющих большое значение для физической химии и решения различных технологических задач. Мы ограничимся применением первого закона термодинамики только для идеальных газов и рассмотрим важнейшие процессы: изохорический, изобарический, изотермический и адиабатический.
Изохорический процесс
Изохорический процесс протекает при постоянном объеме, поэтому система никакой работы не совершает. В этом случае вся теплота расходуется на увеличение внутренней энергии системы. Если V = const, то A =0, тогда
qV = ΔU
При изохорическом процессе количество теплоты, получаемое системой, можно вычислить по уравнениям:
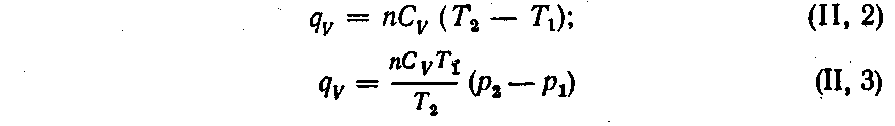
где п — количество вещества; р1 и р2 — соответственно начальное и конечное давление системы; СV — молярная теплоемкость при постоянном объеме; T1 — начальная температура; Т2 — конечная температура.
Изобарический процесс
Если теплота поглощается системой при постоянном давлении, то в системе соответственно увеличивается энтальпия. Если р =const, то ΔU = qp - A, но ΔU + A = ΔH. Тогда
qp = ΔH (II, 4)
Количество теплоты, получаемое системой в этих условиях, может быть вычислено по уравнениям:
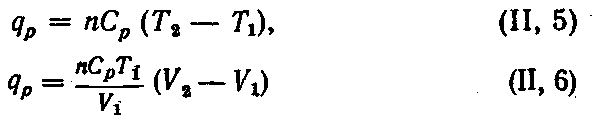 где
Ср
—
молярная теплоемкость при постоянном
давлении; V1
и
V2
— соответственно
начальный и конечный объем системы.
Работа при изобарическом процессе
выражается уравнением:
где
Ср
—
молярная теплоемкость при постоянном
давлении; V1
и
V2
— соответственно
начальный и конечный объем системы.
Работа при изобарическом процессе
выражается уравнением:
А = р(V2 – V1) (II, 7)
Изотермический процесс
Если совершается изотермический процесс, то внутренняя энергия системы при этом не меняется. Вся сообщаемая теплота расходуется на работу по расширению системы.
Если Т = const, то ΔU = 0, тогда q = А.
Работа изотермического расширения системы может быть вычислена по уравнениям:
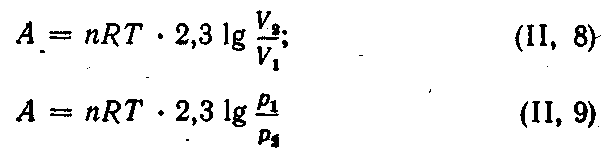
Адиабатический процесс
При
адиабатическом процессе теплообмен
между данной системой и окружающей
средой отсутствует, поэтому q
=
0. При этом система может совершать
работу только за счет убыли внутренней
энергии: А
=
— ΔU.
Работа в этом случае может быть вычислена
по одному из следующих уравнений:
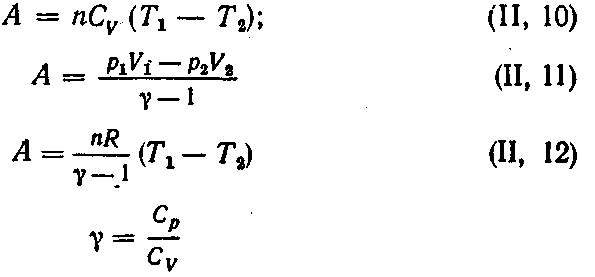
Связь между давлением, объемом и температурой в начале и конце адиабатического процесса выражается уравнениями:
![]()
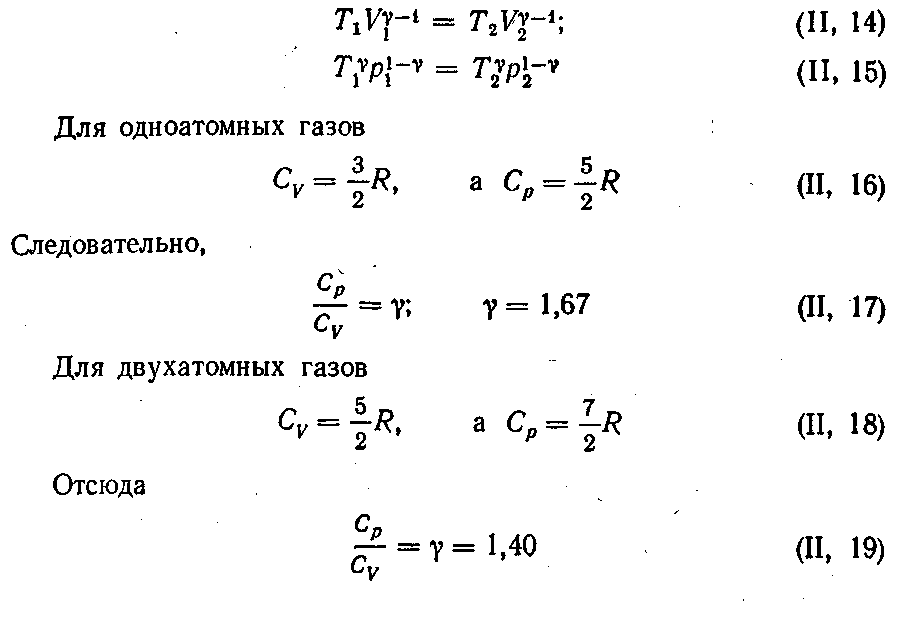
Примеры
1. Путем нагревания при постоянном давлении в 1,013 х 105 Па газу сообщено 2093,4 Дж теплоты. Определить изменение внутренней энергии этого газа, если он при этом расширился от 0,01 до 0,02 м3.
Решение. Согласно первому закону термодинамики ΔU = q – A.. Работа, совершенная газом при изобарическом расширении, может быть вычислена по уравнению (II, 7):
А = р (V2 — V1); A = 1,013 • 106 Па • (0,02 м3 — 0,01 м3) = 1013 Дж
Отсюда ΔU = 2093,4 — 1013 = 1080,4 (Дж).
2. Гелий массой 75 г нагревали при температуре 100 °С и давлении 1,013 • 105 Па. Вычислить количество затраченной теплоты, если объем газа изменился от 3 до 15 л.
Решение. Так как нагревание газа происходит изотермически и изобарически, то количество затраченной теплоты можно вычислить по уравнению (II, 6), только дополнительно необходимо определить количество вещества п и молярную теплоемкость гелия при постоянном давлении:
n(Не)= 75/4 = 18,75 (моль) Гелий — одноатомный газ, поэтому согласно формуле (II, 16)
![]()
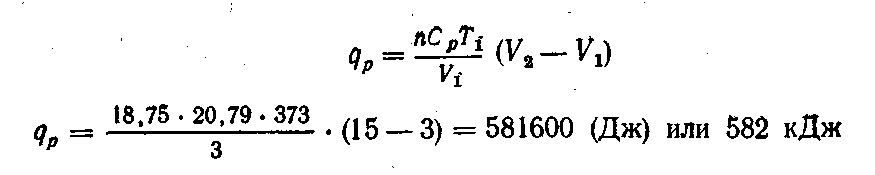
3. Определить работу, совершаемую азотом при изотермическом, (20 °С) расширении его от 0,015 до 0,1 м3, если начальное давление было 3,039 • 105 Па, Каково будет конечное давление?
Решение. Для изотермического процесса работа расширения газа может быть вычислена по уравнению (II, 8). Количество вещества азота находим из уравнения состояния идеального газа:
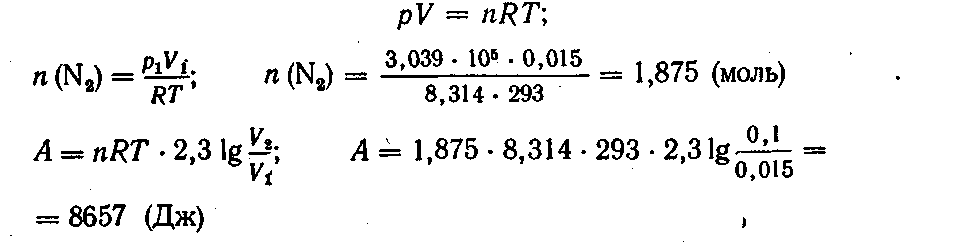
Конечное давление газа при постоянной температуре и известном объеме находим по закону Бойля — Мариотта:
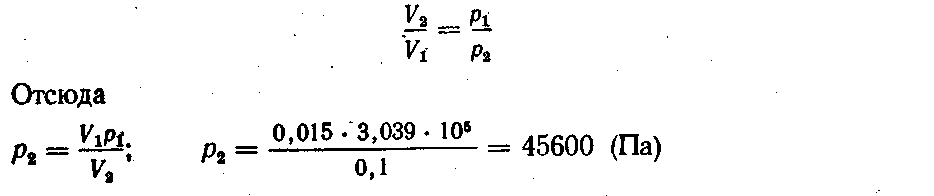
4. Сколько нужно затратить теплоты, чтобы изохорически нагреть кислород массой 25 г от 0 до 50 °С?
Решение. При изохорическом процессе газ никакой работы не совершает, поэтому вся подводимая к газу теплота расходуется на его нагревание. Согласно уравнению (II, 2)
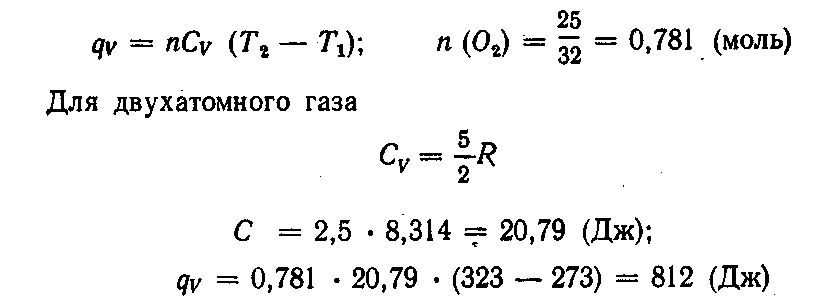
5. Навеску водорода массой 0,5 г, взятую при 25 °С, адиабатически сжимают от 6 до 2 л. Определить конечную температуру газа и работу, затраченную на его сжатие.
Решение. Связь между объемом и Температурой адиабатического процесса показывает уравнение (II, 14):
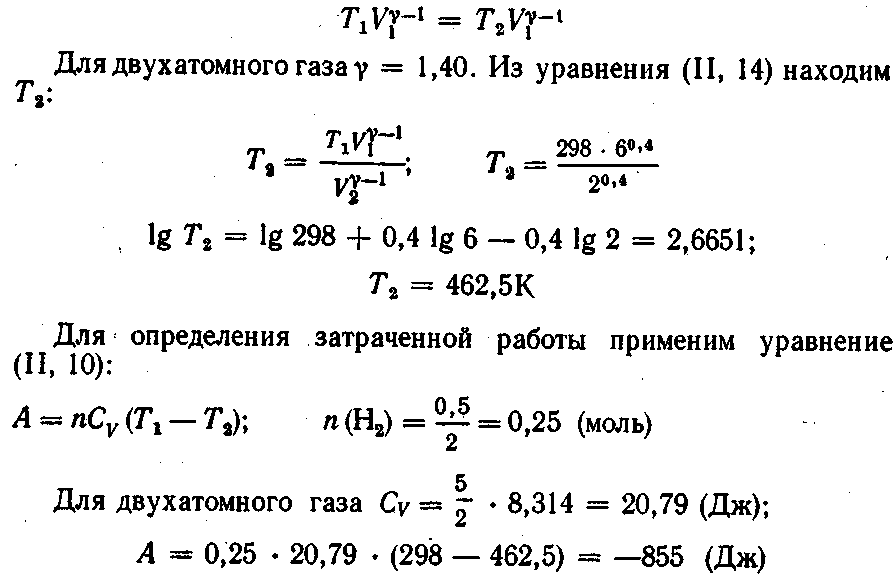
Вопросы и упражнения
1. Что такое термодинамика и какие явления она изучает?
2. Приведите несколько формулировок первого закона термодинамики и покажите, что они не противоречат одна другой. Почему часто первый закон термодинамики называют первым началом?
3. Что такое система? Какие ее виды различают? Приведите примеры.
4. Дайте определение и приведите примеры термодинамических процессов: изотермического, изобарического, изохорического и адиабатического.
5. Что такое внутренняя энергия системы и из чего она слагается? Что такое кинетическая и потенциальная энергия? Почему внутренняя энергия идеального газа слагается только из кинетической энергии его молекул?
6. Почему термодинамика рассматривает не абсолютные значения внутренней энергии, а только ее изменение?
7. Что такое энтальпия и какова ее связь с внутренней энергией? Почему для конденсированных систем разница между энтальпией и внутренней энергией мала, а для систем газообразных значительна?
8. Какие возможны способы передачи энергии от одной системы к другой?
9. Что такое теплота и работа? Можно ли сказать: «Сколько теплоты содержится в стакане горячей воды?» Почему?
10. Что такое теплоемкость удельная, молярная? Какая существует связь между молярной теплоемкостью при постоянном давлении и при постоянном объеме?
11. Работа определяется двумя величинами: фактором интенсивности и фактором экстенсивности. Что будут представлять собой эти факторы при совершении механической работы, электрической и работы по расширению газов?
12. Что такое максимальная работа расширения идеального газа? Почему газ, расширяясь в вакууме, работы не совершает?
13. Напишите уравнения, выражающие максимальную работу расширения идеального газа при изотермическом, изобарическом, изохорическом и адиабатическом процессах.
14. Дайте определения необратимым и необратимым термодинамическим процессам. Приведите примеры. Можно ли реальные природные процессы считать полностью обратимыми?
Задачи
1. Определите изменение внутренней энергии при изобарическом (1,013 • 10б Па) испарении воды массой 100 г при 150° С, если объемом жидкой воды пренебречь. Теплота испарения воды при 150 °С равна 2112,66 Дж/г.
2. Определите изменение внутренней энергии при изобарическом испарении этилового спирта массой 10 г при температуре кипения (78 °С), если теплота испарения спирта равна 922,77 Дж/г. Объемом жидкости пренебречь.
3. Какое количество теплоты необходимо для изохорического нагревания азота массой 10 г от 10 до 20 °С?
4. Одноатомный газ объемом 5 л (условия нормальные) нагревают до 600 °С при постоянном объеме. Каковы конечное давление и количество затраченной теплоты?
5. Какое количество теплоты необходимо для изохорического нагревания углекислого газа массой 50 г в интервале температур от 300 до 400 °С, если СV = 40,2 Дж/моль.
6. При действии кислоты на металл выделился водород объемом 0,007 м3 при давлении в 1,013 • 105 Па. Определите работу, произведенную газом против атмосферного давления.
7. Бензол массой 100 г испаряется при температуре кипения (80,2 °С) и давлении в 1,013 • 105 Па. Определите произведенную парами бензола работу, изменение внутренней энергии и изменение энтальпии, если теплота испарения бензола равна 395,2 Дж/г.
8. Определите затраченную теплоту и совершенную работу изобарического (1,013 • 105 Па) расширения кислорода объемом от 0,005 м3 при 20 °С до 0,00551 м3 при 50 °С.
9. Азот количеством вещества 5 моль при 100 °С занимал объем 0,025 м3. При нагревании газа до 200 °С было затрачено 14 650 Дж. Определите Ср и конечный объем, если давление газа при этом не изменилось.
10. Рассчитайте работу изотермического (27 °С) расширения углекислого газа количеством вещества 1 моль от 2,24 до 22,4 л.
11. Рассчитайте работу изотермического (0°С) расширения хлора количеством вещества 0,5 моль от 1 до 25 л.
12. Рассчитайте работу изотермического (50 °С) расширения водорода массой 20 г от 10 до 40 л.
13. Определите работу изотермического (25 °С) расширения 1 моль идеального газа при изменении давления от 5,065 • 10б до 1,013 • 105 Па. Какое количество теплоты при этом поглощено?
14. 1 моль гелия, взятый при 100 °С и давлении 10,13 • 105 Па, адиабатически расширился. При этом температура понизилась до 25 °С. Определите работу, совершенную гелием.
15*. Какова будет работа адиабатического сжатия 1моль азота, если при этом температура повысилась от 0 до 50 °С?
16*. При адиабатическом сжатии кислорода объемом 0,002 м3 давление газа повысилось от 1,013. - 10б до 2,026 • 105 Па. Чему равен конечный объем?
17*. 1 моль одноатомного газа, взятого при 25 °С и давлении 1,013 • 105 Па, адиабатически расширился до 0,05 м3. Каковы будут конечные давление и температура?
18*. Гелий массой 10 г, взятый при 25 °С, адиабатически расширился от 0,01 до 0,005 м3. Определите работу, совершенную газом.
19*. Аргон массой 10 г нагрели на 10 °С в одном случае при постоянном объеме, а в другом — при постоянном давлении. Какова будет разница в количестве затраченной при этом теплоты?
20*. Взят азот массой 100 г при О °С и давлении 1,013 х 105Па. Определите количество сообщенной системе теплоты. Как изменилась внутренняя энергия и какова совершенная работа при: а) изотермическом расширении газа до объема в 0,1 м3; б) изохорическом сжатии до 2,026 • 105 Па; в) изобарическом расширении объема в 3 раза?
