
- •1. Константы кислотности (Кк) и основности (Ко) слабых электролитов в водных растворах при 298,15 к [1–4]
- •2. Произведения растворимости (пр) малорастворимых электролитов в водном растворе при 298,15 k [1, 2, 4–6]
- •3. Стандартная энтропия (s0298), изменение стандартной энтальпии (h0298) и энергии гиббса (g0298) образования веществ при 298,15 k [1, 4, 5, 7]
- •4. Кислотно-основные индикаторы [2]
- •5. Окислительно-восстановительные индикаторы [2]
- •6. Индикаторы в комплексометрии (металлоиндикаторы) [2]
- •7. Стандартные потенциалы (e0) окислительно-восстановительных пар в водном растворе при 298,15 k [1–4]
- •8. Приближенные значения коэффициентов активности () ионов при различных ионных силах раствора () [7]
- •9. Криоскопические (kт) и эбуллиоскопические (eт) коэффициенты
- •10. Общие константы образования комплексов (n) в водном растворе при 298,15 к [1, 2]
- •11. Плотности (), массовые доли () и молярные концентрации (с) растворов при 293 к [2, 3]
- •Библиографический список
- •620002, Екатеринбург, ул. Мира, 19
- •620002, Екатеринбург, ул. Мира, 19
8. Приближенные значения коэффициентов активности () ионов при различных ионных силах раствора () [7]
, моль/л |
Заряд иона Z |
, моль/л |
Заряд иона Z |
||||||
1 |
2 |
3 |
4 |
1 |
2 |
3 |
4 |
||
0,001 |
0,98 |
0,78 |
0,73 |
0,59 |
0,2 |
0,80 |
0,41 |
0,14 |
0,028 |
0,002 |
0,97 |
0,74 |
0,66 |
0,46 |
0,3 |
0,81 |
0,42 |
0,14 |
0,032 |
0,005 |
0,95 |
0,66 |
0,55 |
0,35 |
0,4 |
0,82 |
0,45 |
0,17 |
0,042 |
0,01 |
0,92 |
0,60 |
0,47 |
0,26 |
0,5 |
0,84 |
0,50 |
0,21 |
0,062 |
0,02 |
0,90 |
0,53 |
0,37 |
0,16 |
0,6 |
0,87 |
0,56 |
0,27 |
0,098 |
0,05 |
0,84 |
0,50 |
0,21 |
0,062 |
0,8 |
0,92 |
0,72 |
0,48 |
0,27 |
0,1 |
0,81 |
0,44 |
0,16 |
0,037 |
1,0 |
0,99 |
0,96 |
0,91 |
0,85 |
9. Криоскопические (kт) и эбуллиоскопические (eт) коэффициенты
Вещество |
KТ, K кг/моль |
EТ, K кг/моль |
Вода |
1,86 |
0,52 |
Бензол |
5,1 |
2,52 |
Этиловый спирт |
– |
1,16 |
Диэтиловый эфир |
1,73 |
2,52 |
10. Общие константы образования комплексов (n) в водном растворе при 298,15 к [1, 2]
В таблице приведены логарифмы констант равновесия реакций комплексообразования: М + nL = [MLn], где [MLn] – комплексная частица, М – комплексообразователь, L – лиганд, n – число лигандов (или координационное число, если лиганд монодентатный). Комплексы сгруппированы по виду лиганда. Данные представлены преимущественно для четных значений n как наиболее распространенных. Значком () указаны нейтральные молекулы в растворе. Знак (?) – отсутствие согласованных данных.
Центр. ион |
lg2 |
lg4 |
lg6 |
Лиганд Br – |
|||
Ag + |
7,34 |
8,73 |
– |
Au + |
12,46 |
– |
– |
Au 3+ |
? |
31,5 |
– |
Bi 3+ |
4,45 |
7,84 |
9,52 |
Cd 2+ |
3,00* |
2,93 |
– |
Cu + |
5,92 |
– |
– |
Hg 2+ |
17,33* |
21,00 |
– |
Центр. ион |
lg2 |
lg4 |
lg6 |
Лиганд Br – |
|||
Pb 2+ |
3,00* |
2,93 |
– |
Pd 2+ |
? |
13,10 |
– |
Pt 2+ |
? |
20,5 |
– |
Tl 3+ |
16,6 |
23,9 |
26,2 |
Лиганд СН3СОО – |
|||
Hg 2+ |
9,30* |
17,01 |
– |
In 3+ |
5,95 |
9,08 |
– |
Центр. ион |
lg2 |
lg4 |
lg6 |
Лиганд СН3СОО – |
|||
Pb 2+ |
4,08* |
8,58 |
– |
UO22+ |
4,9* |
lg3 = 6,3 |
|
Лиганд CN – |
|||
Ag + |
19,85 |
19,42 |
– |
Au + |
38,3 |
– |
– |
Au 3+ |
? |
56 |
– |
Cd 2+ |
9,60* |
17,11 |
– |
Co 2+ |
? |
? |
19,09 |
Co 3+ |
? |
? |
64 |
Cu + |
24,0 |
30,3 |
– |
Fe 2+ |
? |
? |
36,9 |
Fe 3+ |
? |
? |
43,9 |
Hg 2+ |
32,75* |
38,97 |
40,62 |
Ni 2+ |
? |
31,0 |
– |
Pd 2+ |
? |
42,4 |
– |
Tl 3+ |
? |
35 |
– |
Zn 2+ |
11,07* |
19,62 |
– |
Лиганд CNS – |
|||
Ag + |
8,23 |
9,67 |
– |
Au 3+ |
? |
42 |
– |
Bi 3+ |
2,26 |
3,41 |
4,23 |
Cu + |
? |
10,05 |
9,27 |
Cu 2+ |
3,65* |
6,52 |
– |
Fe 3+ |
4,33 |
4,53 |
3,23 |
Hg 2+ |
17,60 |
21,20 |
– |
U 4+ |
1,95 |
– |
– |
Zn 2+ |
1,56* |
3,02 |
– |
Центр. ион |
lg2 |
lg4 |
lg6 |
Лиганд CNS – |
|||
Zr 4+ |
3,4 |
5,8* |
7,9 |
Лиганд СО32– |
|||
Cu 2+ |
10,01 |
– |
– |
Pb 2+ |
9,09 |
– |
– |
UO22+ |
14,6 |
lg3 = 18,3 |
|
Лиганд Cl – |
|||
Ag + |
5,04 |
5,30 |
– |
Au + |
9,42 |
– |
– |
Au 3+ |
? |
21,30 |
– |
Bi 3+ |
4,7 |
5,6 |
6,42 |
Cd 2+ |
2,60* |
1,7 |
– |
Hg 2+ |
13,22* |
15,22 |
– |
Pd 2+ |
10,5* |
15,5 |
11,3 |
Pt 2+ |
11,48* |
16,0 |
– |
Tl 3+ |
13,48 |
18,29 |
– |
Лиганд F – |
|||
Al 3+ |
11,98 |
18,53 |
20,67 |
Be 2+ |
8,32* |
13,39 |
– |
Ce 3+ |
6,90 |
– |
– |
Cr 3+ |
8,54 |
– |
– |
Fe 3+ |
10,74 |
15,74 |
16,10 |
Ga 3+ |
8,3 |
12,5 |
– |
Sc 3+ |
12,88 |
20,81 |
– |
Sn 4+ |
? |
? |
25 |
Th 4+ |
13,46 |
lg3 = 17,97 |
|
TiO 2+ |
11,74* |
20,38 |
– |
U 4+ |
12,41 |
20,91* |
24,80 |
Центр. ион |
lg2 |
lg4 |
lg6 |
Лиганд F – |
|||
UO22+ |
7,7* |
11,7 |
– |
VO 2+ |
5,5* |
7,5 |
– |
Y 3+ |
8,54 |
lg3 = 12,14* |
|
Zr 4+ |
17,37 |
27,17* |
35,86 |
Лиганд HPO4 2– |
|||
Fe 2+ |
lg1 = 7,2* |
||
Fe 3+ |
lg1 = 9,75 |
||
Pu 4+ |
23,7* |
43,2 |
– |
lg5 = 52 |
|||
UO22+ |
18,57 |
– |
– |
Лиганд H2PO4 – |
|||
Al 3+ |
5,3 |
lg3 = 7,6 |
|
Cu 2+ |
1,49* |
– |
– |
Fe 3+ |
? |
9,15 |
– |
UO22+ |
5,43* |
lg3 = 7,33 |
|
Лиганд I – |
|||
Ag + |
11,74 |
13,10 |
– |
Bi 3+ |
? |
14,95 |
19,1 |
Cd 2+ |
3,67* |
5,35 |
– |
Hg 2+ |
23,82* |
29,83 |
– |
Pb 2+ |
2,8* |
3,92 |
– |
Tl 3+ |
20,88 |
31,82 |
– |
Лиганд NH3 |
|||
Ag + |
7,24 |
– |
– |
Au + |
27 |
– |
– |
Au 3+ |
? |
30 |
– |
Центр. ион |
lg2 |
lg4 |
lg6 |
Лиганд NH3 |
|||
Cd 2+ |
4,47 |
6,56 |
– |
Co 2+ |
3,50 |
5,07 |
4,39 |
Co 3+ |
14,0 |
25,7 |
35,21 |
Cu + |
10,86 |
– |
– |
Cu 2+ |
7,33 |
12,03 |
8,9 |
Hg 2+ |
17,5 |
19,3 |
– |
Ni 2+ |
4,79 |
7,47 |
8,01 |
Zn 2+ |
4,43 |
8,70 |
– |
Лиганд NO2– |
|||
Ag + |
2,83 |
– |
– |
Cd 2+ |
3,01* |
3,10 |
– |
Cu 2+ |
1,65* |
– |
– |
Hg 2+ |
? |
13,54 |
– |
Лиганд SO4 2– |
|||
Ag + |
0,50 |
– |
– |
Al 3+ |
5,1 |
– |
– |
Be 2+ |
1,78 |
– |
– |
Fe 3+ |
5,38 |
– |
– |
Hf 4+ |
5,58* |
– |
– |
Hg 2+ |
2,44 |
– |
– |
In 3+ |
2,60 |
lg3 = 3 |
|
Pb 2+ |
3,47 |
– |
– |
Pu 3+ |
1,62 |
– |
– |
Th 4+ |
5,70* |
– |
– |
Tl 3+ |
3,74 |
– |
– |
U 4+ |
5,42* |
– |
– |
Центр. ион |
lg2 |
lg4 |
lg6 |
Лиганд SO4 2– |
|||
UO22+ |
4,20 |
– |
– |
Zr 4+ |
6,64* |
lg3 = 7,77 |
|
Лиганд S2O3 2– |
|||
Ag + |
13,46 |
– |
– |
Ca 2+ |
3,98 |
– |
– |
Cd 2+ |
6,48 |
– |
– |
Cu + |
12,27 |
– |
– |
Cu 2+ |
12,29 |
– |
– |
Hg 2+ |
29,86 |
33,61 |
– |
Pb 2+ |
5,13 |
7,2 |
– |
Tl 3+ |
? |
41 |
– |
Zn 2+ |
4,59 |
– |
– |
Центр. ион |
lg1 |
lg2 |
lg3 |
Лиганд С2О4 2– |
|||
Al 3+ |
7,3 |
13 |
16,3 |
Be 2+ |
4,08* |
5,91 |
– |
Cd 2+ |
4,00* |
5,77 |
– |
Ce 3+ |
6,52 |
10,48 |
11,30 |
Co 2+ |
4,7 |
6,8 |
9,7 |
Центр. ион |
lg1 |
lg2 |
lg3 |
Лиганд С2О4 2– |
|||
Cr 3+ |
5,34 |
10,51 |
15,44 |
Cu 2+ |
6,7* |
10,3 |
– |
Fe 2+ |
3,05* |
4,52 |
5,22 |
Fe 3+ |
9,4 |
16,2 |
20,2 |
In 3+ |
5,30 |
10,52 |
14,7 |
La 3+ |
4,3 |
7,9 |
10,3 |
Mn 2+ |
3,82* |
5,25 |
– |
Mn 3+ |
9,98 |
16,57 |
19,42 |
Nd 3+ |
7,21 |
11,51 |
13,5 |
Ni 2+ |
5,3* |
6,51 |
14 |
Pb 2+ |
4,9* |
6,54 |
– |
Th 4+ |
10,6 |
20,2* |
26,4 |
lg4 = 29,6 |
|||
TiO2 2+ |
6,60* |
9,90 |
? |
U4+ |
10,9 |
20,7* |
26,4 |
|
lg4 = 29,8 |
||
UO22+ |
4,85* |
7,55 |
8,34 |
Zr 4+ |
11,11 |
20,31* |
27,97 |
|
lg4 = 34,0 |
||
Лиганд OH – (гидроксокомплексы) |
||||||
Центр. ион |
lg1 |
lg2 |
lg3 |
lg4 |
lg5 |
lg6 |
Ag + |
2,30* |
4,0 |
5,2 |
– |
– |
– |
Al 3+ |
9,0 |
17,86 |
27* |
33 |
– |
– |
AsO + |
14,33* |
18,73 |
20,60 |
21,2 |
– |
– |
Лиганд OH – (гидроксокомплексы) |
||||||
Центр. ион |
lg1 |
lg2 |
lg3 |
lg4 |
lg5 |
lg6 |
Be 2+ |
7,48 |
14,0* |
15,2 |
15,0 |
– |
– |
Bi 3+ |
12,4 |
15,8 |
? |
35,2 |
– |
– |
Ca 2+ |
1,46 |
11,0* |
– |
– |
– |
– |
Cd 2+ |
6,08 |
8,70* |
8,38 |
8,42 |
– |
– |
Ce 3+ |
4,6 |
– |
– |
– |
– |
– |
Ce 4+ |
13,28 |
27,06 |
– |
– |
– |
– |
Co 2+ |
4,4 |
9,2* |
10,5 |
– |
– |
– |
Cr 3+ |
10,1 |
17,8 |
? |
29,9 |
– |
– |
Cu 2+ |
6,0 |
13,18* |
14,42 |
14,56 |
– |
– |
Fe 2+ |
5,56 |
9,77* |
9,67 |
8,56 |
– |
– |
Fe 3+ |
11,87 |
21,17 |
30,67* |
– |
– |
– |
Ga 3+ |
11,44 |
22,18 |
31,78* |
34,3 |
38,0 |
40,3 |
Hf 4+ |
14,12 |
27,89 |
41,47 |
54,95* |
– |
– |
Hg 2+ |
10,30 |
21,70* |
21,20 |
– |
– |
– |
In 3+ |
11,89 |
23,44 |
34,76* |
35,2 |
– |
– |
La 3+ |
3,9 |
– |
– |
– |
– |
– |
Mn 2+ |
3,90 |
? |
8,3 |
– |
– |
– |
Ni 2+ |
4,97 |
8,55* |
11,33 |
– |
– |
– |
Pb 2+ |
7,52 |
10,54* |
13,95 |
– |
– |
– |
Pd 2+ |
13,0 |
25,8* |
– |
– |
– |
– |
Sb 3+ |
6,07 |
24,3 |
36,7* |
38,3 |
– |
– |
Sn 2+ |
11,93 |
20,94* |
25,40 |
– |
– |
– |
Sn 4+ |
? |
? |
? |
? |
? |
63,0 |
Th 4+ |
10,11 |
21,2 |
32,0 |
? |
? |
38,7 |
Ti 4+ |
18,0 |
35,2 |
47,7 |
58,7* |
– |
– |
Tl 3+ |
12,86 |
25,37 |
– |
– |
– |
– |
Лиганд OH – (гидроксокомплексы) |
||||||
Центр. ион |
lg1 |
lg2 |
lg3 |
lg4 |
lg5 |
lg6 |
U 4+ |
13,3 |
25,7 |
– |
– |
– |
– |
UO22+ |
9,2 |
17,2* |
25,5 |
32,4 |
– |
– |
V 3+ |
11,6 |
21,75 |
– |
– |
– |
– |
VO 2+ |
9,23 |
25* |
– |
– |
– |
– |
Zn 2+ |
6,31 |
11,19* |
14,31 |
17,70 |
– |
– |
Zr 4+ |
14,58 |
29,38 |
43,72 |
57,85* |
– |
– |
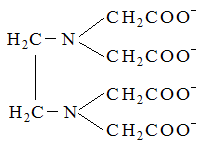
Лиганд (этилендиаминтетраацетатные комплексы)
Центр. ион |
lg1 |
Ag + |
7,31 |
Al 3+ |
16,5 |
Ba 2+ |
7,78 |
Be 2+ |
8,4 |
Bi 3+ |
27,4 |
Ca 2+ |
10,59 |
Cd 2+ |
16,46 |
Ce 3+ |
15,81 |
Co 2+ |
16,31 |
Co 3+ |
40,6 |
Cr 3+ |
23,40 |
Центр. ион |
lg1 |
Cs + |
0,15 |
Cu 2+ |
18,80 |
Fe 2+ |
14,20 |
Fe 3+ |
24,23 |
Ga 3+ |
20,5 |
Hg 2+ |
21,8 |
In 3+ |
25,3 |
K + |
0,96 |
La 3+ |
15,5 |
Li + |
2,85 |
Mg 2+ |
9,12 |
Центр. ион |
lg1 |
Mn 2+ |
14,04 |
Mn 3+ |
24,9 |
Na + |
1,79 |
Ni 2+ |
18,62 |
Pb 2+ |
18,04 |
Pd 2+ |
18,5 |
Pu 3+ |
25,75 |
Pu 4+ |
26,1 |
Rb + |
0,59 |
Sc 3+ |
23,0 |
Sn 2+ |
18,3 |
Центр. ион |
lg1 |
Sr 2+ |
8,80 |
Th 4+ |
25,3 |
TiO 2+ |
17,5 |
Tl + |
6,53 |
Центр. ион |
lg1 |
Tl 3+ |
37,8 |
U 4+ |
25,83 |
UO22+ |
10,4 |
V 3+ |
25,9 |
Центр. ион |
lg1 |
VO 2+ |
18,0 |
VO2+ |
15,55 |
Zn 2+ |
16,26 |
Zr 4+ |
29,5 |
Дополнительные данные можно найти в [1, 2]
