
- •Основные параметры состояния Плотность и удельный объем
- •Давление и единица давления
- •Давление и разрежение
- •Законы идеальных газов
- •Уравнение Менделеева – Клапейрона
- •Смеси жидкостей, газов и паров
- •Газовые смеси. Закон Дальтона
- •Кг/моль.
- •Объемные доли газовой смеси
- •29,33210-3 Кг/моль.
- •Теплоемкость
- •Нахождение истинных и средних теплоемкостей
- •Теплоемкость смесей
- •Термодинамические процессы газов
- •Изохорный процесс
- •Изобарный процесс
29,33210-3 Кг/моль.
Удельная газовая постоянная смеси
R0 =R/Mсм= 8,31/29,33210-3 = 283,3 Дж/(кг К).
Пример 10. Найти для условий предыдущего примера парциальные давления азота и кислорода газовой смеси. Давление смеси равно 0,1 МПа.
Решение. Парциальные давления компонентов:
рO2 = хO2р = 0,3330,1106 =33333 Па;
рN2 = хN2р = 0,6670,1106 =66667 Па.
Контрольное уравнение:
рO2 +рN2 = 33333+66667= 10000 Па = 0,1 МПа.
Пример 11. Продукты сгорания топлива массой 1 кг имеют следующий состав (в моль): nH2O ( паров воды) = 60,3; nCO2 = 73,9; nO2 = 123,2; nN2 = 849,5. Найти молярную массу и массу смеси.
Решение. Количество вещества продуктов сгорания
nсм = nH2O +nCO2 +nO2 +nN2 = 60,3+ 73,9+ 123,2+ 849,5 = 1106,9 моль.
Молярные доли компонентов:
хH2O = nH2O/n = 60,3/1106,9=0,0544;
хCO2 = n CO2/ n = 73,9/1106,9 =0,0668;
хO2 = nO2/ n = 123,2/1106,9 =0,1113;
хN2 = nN2/ n = 849,5/1106,9 =0,7675.
Контрольное уравнение:
хH2O +хCO2 +хO2 +хN2 = 0,0544+0,0668+0,1113+0,7675= 1,000.
Молярная масса смеси
![]()
(0,054418+ 0,066844 +0,111332+0,767628)10-3 = 29,33210-3 кг/моль.
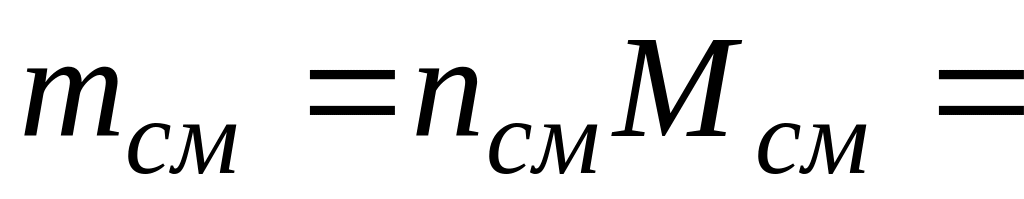 1106,929,33210-3
= 32,47 кг.
1106,929,33210-3
= 32,47 кг.
Задачи
Горючая смесь газового двигателя состоит по объему из 8 частей воздуха и 1 части светильного газа. Найти удельную газовую постоянную и плотность смеси при давлении 0,1 МПа и температуре 15С, если светильный газ состоит из следующих объемных частей: 48,5% водорода; 39,5% метана; 7% угарного газа и 5% азота. Ответ: R0 = 308,2 Дж/(кгК); = 1,126 кг/м3.
Объемные доли сухих продуктов сгорания (т.е. не содержащих водяного пара) следующие: хCO2 =0,123; хO2 = 0,072;хN2 =0,805. Найти удельную газовую постоянную, плотность и удельный объем продуктов сгорания, если их давление 0,1 МПа, а температура 800С. Ответ: R0 = 274,7 Дж/(кг К); v =2,947 м3/кг; =0,339 кг/м3.
Газовая смесь задана следующими молярными долями: хCO2 =0,04; хСО = 0,1;хN2 =0,03; хН2 = 0,45; хСН4 = 0,35; хС2Н4 = 0,03. Давление смеси 90 кПа. Найти удельную газовую постоянную смеси и парциальное давление метана, а также плотность смеси при нормальных условиях. Ответ: R0 = 652,3 Дж/(кгК); рСН4 = 31,5 кПа; =0,569 кг/м3.
Найти массу продуктов сгорания топлива состава: nCO2 = 789 моль; nН2О = 67,4 моль; nО2 = 96,2 моль; nN2 = 787,3 моль. Ответ: 61,052 кг.
Продукты сгорания нефти имеют следующий состав в молях: nН2О = 66; nО2 = 70; nN2 = 660; nCO2 = 70. Найти удельную газовую постоянную и удельный объем смеси при нормальных условиях. Ответ: R0 = 288 Дж/(кг К); v = 0,776 м3/кг.
