
- •060108 «Фармация», 2 курс, III семестр
- •Анализ смеси катионов четвертой-шестой аналитических групп.
- •Четвертая группа
- •1.Предварительные наблюдения и испытания.
- •Систематический ход анализа.
- •Анализ смеси катионов V аналитической группы.
- •II Систематический анализ.
- •Анализ смеси катионов VI аналитической группы
- •I Дробный анализ.
- •II Систематический ход анализа
- •Вопросы для самоподготовки
- •Вопросы для самоконтроля
- •Основная литература
Вопросы для самоконтроля
Напишите уравнение Нернста и поясните значения всех входящих в него величин.
Что такое обратимая окислительно-восстановительная система?
Что такое стандартный потенциал окислительно-восстановительной полуреакции? Какие факторы влияют на его величину?
Что такое реальный потенциал окислительно-восстановительной полуреакции? Какие факторы влияют на его величину?
Как определить направление реакции окисления-восстановления и полноту ее протекания?
Как ускорить медленные окислительно-восстановительные реакции?
Что такое индуцированные реакции?
Чем отличаются индуцированные цепные реакции от индуцированных сопряженных?
В каком случае и почему восстановительная способность железа(II) будет выше: в среде 1М H2SO4 или 1М H3PO4?
Назовите основные окислители и восстановители, используемые в анализе для разделения и обнаружения ионов. Напишите соответствующие полуреакции.
Какие фармакопейные реакции катионов IV группы Вам известны?
Какие специфические реакции катионов IV группы Вам известны?
Составьте схему анализа смеси катионов IV группы:
Al3+, Cr3+, Zn2+;
Sn2+, As3+, Cr3+;
Sn4+, As5+, Zn2+ .
Назовите основные признаки комплексного соединения. Что такое комплексообразователь, лиганд?
Что может быть положено в основу классификации комплексных соединений?
Назовите основные типы комплексных соединений. Приведите примеры.
Приведите примеры однородно- и смешаннолигандных комплексных соединений.
Что такое полиядерные комплексные соединения? Приведите примеры гомо- и гетерополиядерных соединений.
Чем отличаются ступенчатые и общие константы устойчивости комплексных соединений? Ответ поясните примерами.
Напишите выражение для
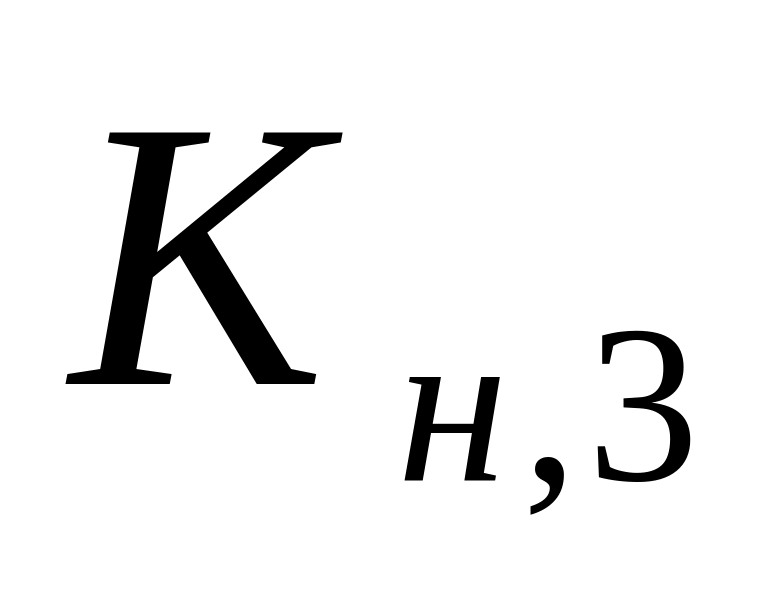 и
и
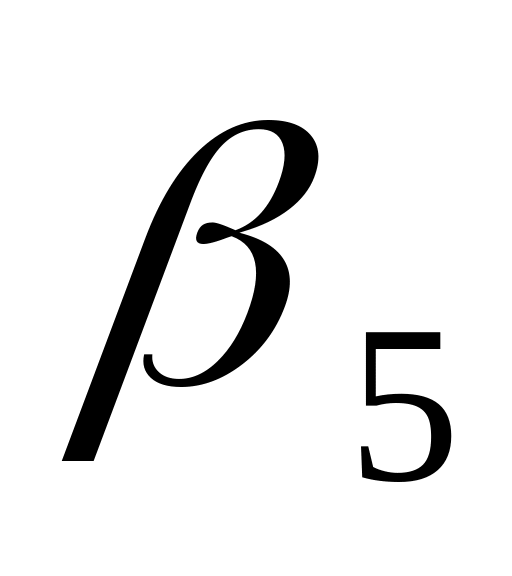 и уравнения реакций образования
соответствующих комплексов в системе
Fe (III) –
фторид-ион.
и уравнения реакций образования
соответствующих комплексов в системе
Fe (III) –
фторид-ион.Приведите примеры практического использования комплексных соединений в анализе.
Какие катионы можно обнаружить реакцией гидролиза?
Какими реагентами можно окислить Mn2+ до MnO4-?
Как отделить Mg2+ от Mn2+?
Какие специфические реакции катионов V аналитической группы вам известны?
Какими реакциями можно доказать присутствие Sb (III) и Sb (V)?
Назовите фармакопейные реакции катионов V аналитической группы.
Почему катионы Fe2+ необходимо открывать в дробном анализе?
Как разделить основные соли сурьмы (III и V) и висмута (III)?
Почему избыток ионов хлора Cl- мешает окислению Mn2+ до MnO4-?
Напишите характерные реакции катионов VI аналитической группы.
Напишите фармакопейные реакции катионов VI аналитической группы.
Приведите 2 варианта разделения ионов Cu2+ и Cd2+.
Как рассчитать константу совмещенного равновесия?
Какие термодинамические константы используют для расчета константы совмещенного равновесия?
Как рассчитать полноту протекания реакции?
Дайте схему систематического анализа смеси катионов VI аналитической группы.
Какие катионы VI группы можно открыть дробным методом?
Источники информации:
