
- •Оглавление
- •Глава 1 Химическая термодинамика. 5
- •Глава 2 Первое начало термодинамики 8
- •Глава 3 Второе начало термодинамики. 15
- •Предисловие
- •Глава 1 Химическая термодинамика. Предмет и основные понятия термодинамики
- •Основные понятия термодинамики
- •Виды процессов
- •Глава 2 Первое начало термодинамики
- •2.1 Первое начало термодинамики как закон сохранения энергии
- •2.2 Первое начало термодинамики для химических реакций
- •2.3 Закон Гесса и следствия из него
- •2.4. Медико-биологическое значение первого начала термодинамики
- •1 Начало термодинамики
- •В химических реакциях
- •Практическое использование
- •Глава 3 Второе начало термодинамики.
- •3.1. Самопроизвольные процессы
- •3.2. Энтропия
- •3.3. Критерии самопроизвольных процессов в различных системах
- •3.4. Энергия Гиббса (изобарно-изотермический потенциал)
- •3.5. Принцип энергетического сопряжения
- •2 Начало термодинамики
- •Тестовые задания для самоконтроля
- •Расчетные задачи
- •Ключ к тесту
- •Термодинамические константы веществ
- •Литература
3.4. Энергия Гиббса (изобарно-изотермический потенциал)
Закрытые и открытые системы реальны. Они обмениваются с окружающей средой энергией, поэтому при поиске критерия самопроизвольного протекания процесса следует учитывать не только изменение энтропии, но и изменение энергии.
Мы уже упоминали, что самопроизвольно протекают процессы, идущие с выделением тепла, т.е. экзотермические процессы, другими словами, система стремится к минимуму энергии, а с другой стороны она стремится к увеличению беспорядка, т.е. к максимальной энтропии.
Параметром, учитывающим обе противоположные тенденции системы при самопроизвольных процессах, является ещё одна термодинамическая функция – изобарно-изотермический потенциал или энергия Гиббса, G. Изменение энергии Гиббса рассчитывают по уравнению

∆G = ∆H – T·∆S (12)
где ∆Н – это энтальпийный член. Он отражает стремление системы к минимуму энергии. Согласно первому началу термодинамики, ∆Н характеризует общий запас энергии системы, находящейся при постоянных давлении и температуре: Q1 = ∆Н.
Т·∆S – энтропийный член, он характеризует стремление системы к максимальной неупорядоченности. Согласно второму началу термодинамики при
T = const это та часть тепла, полученного системой, которая тратится бесполезно, связанное тепло: Q2 = Т·∆S.
∆G называют свободной энергией – часть оставшейся энергии, ∆G = Q1 - Q2, которую можно превратить в работу, т.е. при её расходовании, уменьшении может происходить самопроизвольный процесс. Следовательно, ∆G является критерием возможности самопроизвольного процесса при постоянных давлении и температуре (P = const, T = const).
Уравнение (12) называют объединённым уравнением I и II начал термодинамики.
Соотношение между названными термодинамическими функциями можно представить графически:
U
pΔV
H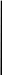



TΔS
ΔG
Отсюда, второе начало термодинамики для любых систем
В системе при постоянной температуре и
давлении самопроизвольно могут
совершаться только такие процессы,
в результате которых уменьшается
энергия Гиббса
системе при постоянной температуре и
давлении самопроизвольно могут
совершаться только такие процессы,
в результате которых уменьшается
энергия Гиббса
∆G < 0 (13)
Это математическое выражение второго начала термодинамики является универсальным критерием самопроизвольного протекания реакции и любого процесса.
Если ∆G > 0, то в этих условиях реакция самопроизвольно протекать не может. Если ∆G = 0, то система находится в состоянии равновесия, энергия Гиббса достигла своего минимального значения и больше не меняется.
Для определения возможности самопроизвольного протекания реакции
а) в стандартных условиях изменение энергии Гиббса реакции рассчитывают, используя закон Гесса, как и в случае других термодинамических функций (∆H и ∆S):

∆G°реакции = Σ i·∆G°298 продукты - Σ i·∆G°298 исх.вещества (14)
где ∆G° кДж/моль – табличные значения стандартной энергии Гиббса образования веществ.
б) для нестандартных условий ∆G реакции рассчитывают, используя объединённое уравнение первого и второго начал термодинамики. Для этого предварительно рассчитывают энтальпию реакции ∆Н° и энтропию реакции ∆S°.
Анализируя объединённое уравнение можно сделать вывод, что самопроизвольно (т.е. ∆G°<0) могут протекать реакции:
- экзотермические (∆Н°<0), если |∆Нреакции| > |Т·∆Sреакции|, т.е. при низких температурах, когда энтальпийный член больше энтропийного.
- эндотермические (∆Н°>0), если |∆Нреакции| < |Т·∆Sреакции|, т.е. при высоких температурах, когда энтропийный член больше энтальпийного.
Пример 6: Определить возможность самопроизвольного протекания реакции синтеза аммиака при 100°С.
Решение: Поскольку условия реакции нестандартные, то расчёт ведём по объединённому уравнению ∆G = ∆H – T·∆S. Выписываем под формулами каждого вещества значения его ∆Н°298 и S°298
N 2(Г)
+ 3H2(Г)
2NH3(Г)
2(Г)
+ 3H2(Г)
2NH3(Г)
∆Н°298, кДж/моль 0 0 - 46
S°298 , Дж/моль·К 131 192 193
1) Расчёт энтальпии реакции
∆Н°реакции = 2·∆Н°(NH3) – [3·∆Н°(H2) + ∆Н°(N2)]
∆Н°реакции = 2·(-46) – (3·0 + 0) = -92 (кДж)
∆Н°<0, реакция экзотермическая
2) Расчёт энтропии реакции
∆S°реакции = 2·S°(NH3) – [3·S°(H2) + S°(N2)]
∆S°реакции = 2·193 – (3·192+ 131) = 386 – 707 = - 321(Дж/К)
Переводим значение энтропии в те же единицы, что и ∆Н° (в кДж)
∆S°= - 0,321кДж/К
3) Расчёт свободной энергии Гиббса реакции
∆Gреакции = ∆H° – T·∆S° Т = 100 + 273 = 373К
∆Gреакции = -92 – 373· (-0,321) = -92 + 119,73 = 27,73 (кДж)
Ответ ∆Gреакции > 0, реакция самопроизвольно протекать не может (хотя и экзотермическая). Решающим оказался энтропийный член.
