- •Часть II
- •Введение
- •Раздел I особенности биологического уровня организации материи Системность живого
- •1.1 Иерархическая организация живого Биологические уровни организации материи
- •1.2 Отличительные признаки живого от неживого
- •Многообразие живых организмов – основа организации и устойчивости биосферы
- •Биологическое разнообразие жизни на земле
- •Вирусы.
- •Прокариоты
- •Бактерии
- •Строение бактерии
- •Размножение
- •Положительная роль бактерий
- •Сине-зеленые водоросли (цианеи)
- •Эукариоты. Строение растительной и животной клетки. Отличие прокариотической клетки от эукариотической.
- •Основные положения клеточной теории
- •Строение ядра. Строение хромосом. Кариотип. Геном.
- •Строение хромосомы.
- •Содержание в клетке химических соединений (в % на сырую массу) ю.И. Полянский
- •Неорганические вещества
- •Требования предъявляемые к органогенам:
- •Вода, ее роль для живой природы
- •Роль воды в живой системе – клетке:
- •Органические соединения Особенности органических биополимеров как высокомолекулярных соединений:
- •Нуклеиновые кислоты: днк и рнк
- •Синтез дhk
- •Функция днк в клетке:
- •1. Строение. Функции в клетке.
- •2. Структуры белка
- •3. Денатурация белка.
- •Генетический код
- •Свойства генетического кода
- •Биосинтез белка в клетке
- •Раздел II. Воспроизведение и развитие живых систем
- •1. Профаза.
- •4. Телофаза.
- •Половое размножение
- •Гаметогенез – процесс образования половых клеток Мейоз
- •Оплодотворение
- •Индивидуальное развитие организмов
- •Раздел III.Происхождение жизни Исторические концепции происхождения жизни на Земле
- •Основные этапы происхождения жизни на Земле
- •Основные стадии биопоэза
- •Абиогенное возникновение биологических мономеров (химическая эволюция).
- •Доказательство абиогенного синтеза
- •Свойства рнк
- •Концепции голо и генобиоза
- •Эволюция живых систем
- •Эволюционная теория ч. Дарвина
- •Генетика и эволюция
- •Моногибридное скрещивание.
- •Закон гомологических рядов в наследственной изменчивости н.И. Вавилова
- •Синтетическая теория эволюции. Ее основные положения.
- •Популяционные волны
- •Изоляция
- •Естественный отбор
- •Микроэволюция
- •Макроэволюция
- •Методы исследования эволюции
- •Развитие жизни на Земле
- •Геохронологическая таблица и история развития живых организмов
- •Основные таксономические группы растений и животных и последовательность их эволюции:
- •Закономерности самоорганизации. Принципы универсального эволюционизма.
- •Концепция самоорганизации в науке. Формирование идеи самоорганизации.
- •Отличие равновесных систем от неравновесных
- •Самоорганизация – источник и основа эволюции
- •Как же происходит эволюция?
- •Эволюции в социальных и гуманитарных системах
- •Универсальный эволюционизм, как научная программа современности
- •Раздел IV. Биосфера и человек. Экосистемы (многообразие живых организмов - основа организации и устойчивости биосферы). Понятия об экосистеме и биогеоценозе
- •Элементы экосистем (биотоп, биоценоз)
- •Виды природных экосистем
- •Биотическая структура экосистем
- •Энергетические потоки в экосистемах.
- •Солнце как источник энергии
- •Пищевые (трофические) цепи, пирамиды
- •Экологические пирамиды (схемы пищевых сетей)
- •Экологические факторы
- •Формы биотических отношений
- •Среда обитания и экологическая ниша
- •Толерантность, пределы толерантности
- •Закон минимума
- •Понятие о биосфере
- •Биогенная миграция атомов химических элементов
- •Структура и основные циклы биохимических круговоротов
- •Раздел V. Человек в биосфере.
- •1. История развития представлений о происхождении человека
- •Приматы
- •Палеонтологические доказательства происхождения человека. Основные этапы эволюции рода Homo и его предшественников (стадиальная концепция).
- •Этапы эволюции человека
- •Факторы антропогенеза
- •Экологические последствия неолитической революции
- •Влияние человека на функции живого вещества в биосфере.
- •Изменение временного фактора развития биосферных процессов.
- •Раздел VI. Глобальный экологический кризис (экологические функции литосферы, экология и здоровье)
- •Экологические кризисы в развитии биосферы и цивилизаций
- •Загрязнение окружающей среды
- •Индикаторы глобального экологического кризиса
- •Усиление парникового эффекта
- •Изменение концентрации основных парниковых газов в атмосфере Земли,
- •Проблема истощения озонового слоя.
- •Кислотные дожди.
- •Закисление озер в мире
- •Деградация водных ресурсов
- •Главные загрязнители воды
- •Приоритетные загрязнители водных экосистем по отраслям промышленности
- •Деградация земельных ресурсов
- •Уменьшение биоразнообразия
- •Понятие ноосферы как этапа развития биосферы при разумном регулировании отношений человека и природы
- •Раздел VII. Экология и здоровье человека Особенности роста и развития современного человека
- •Группировка факторов риска по их удельному весу для здоровья
- •Здоровье и факторы риска
- •Элементы экологии внутренней среды человека
- •Загрязненная внешняя среда, окружающие предметы
- •Трансформирующие агенты биосферы
- •Деградация генофонда человечества
- •Вредные привычки и среда обитания
- •Здоровый образ жизни граждан как основа устойчивого развития общества
- •Раздел VIII. Взаимосвязь космоса и живой природы, космические циклы
- •Солнечные циклы и здоровье человека
- •Биоритмология: узловые годы жизни человека
- •Среднепериодные биоритмы
- •Короткопериодные биоритмы
- •Физиологические особенности психики человека, основные эмоции
- •Эмоциональные реакции. Стресс и здоровье человека.
- •Причины обострения экологических проблем
- •Раздел IX. Принципы охраны природы и рационального природопользования
- •Биоэтика и её сущность
1. Строение. Функции в клетке.
Белки - это биополимеры, мономером которых являются аминокислоты. Все аминокислоты имеют как минимум по одной аминогруппе (NH2) и карбоксильную группу (СООН). Различаются аминокислоты структурой радикалов и физико-химическими свойствами (рис. 18).
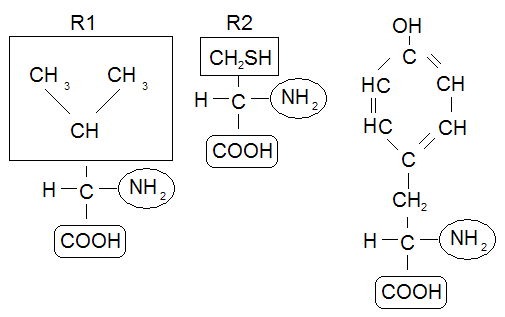
Рис. 18. Строение аминокислоты
Всего аминокислот 20. Аминокислоты, соединяясь друг с другом ковалентными пептидными связями образуют различной длины пептиды (рис. 19).
Пептиды, содержащие от нескольких аминокислотных остатков до нескольких десятков обладают высокой биологической активностью, например, антибиотики. Вообще белки - это полипептиды, в состав которых входит от 100 до несколько тысяч аминокислот.
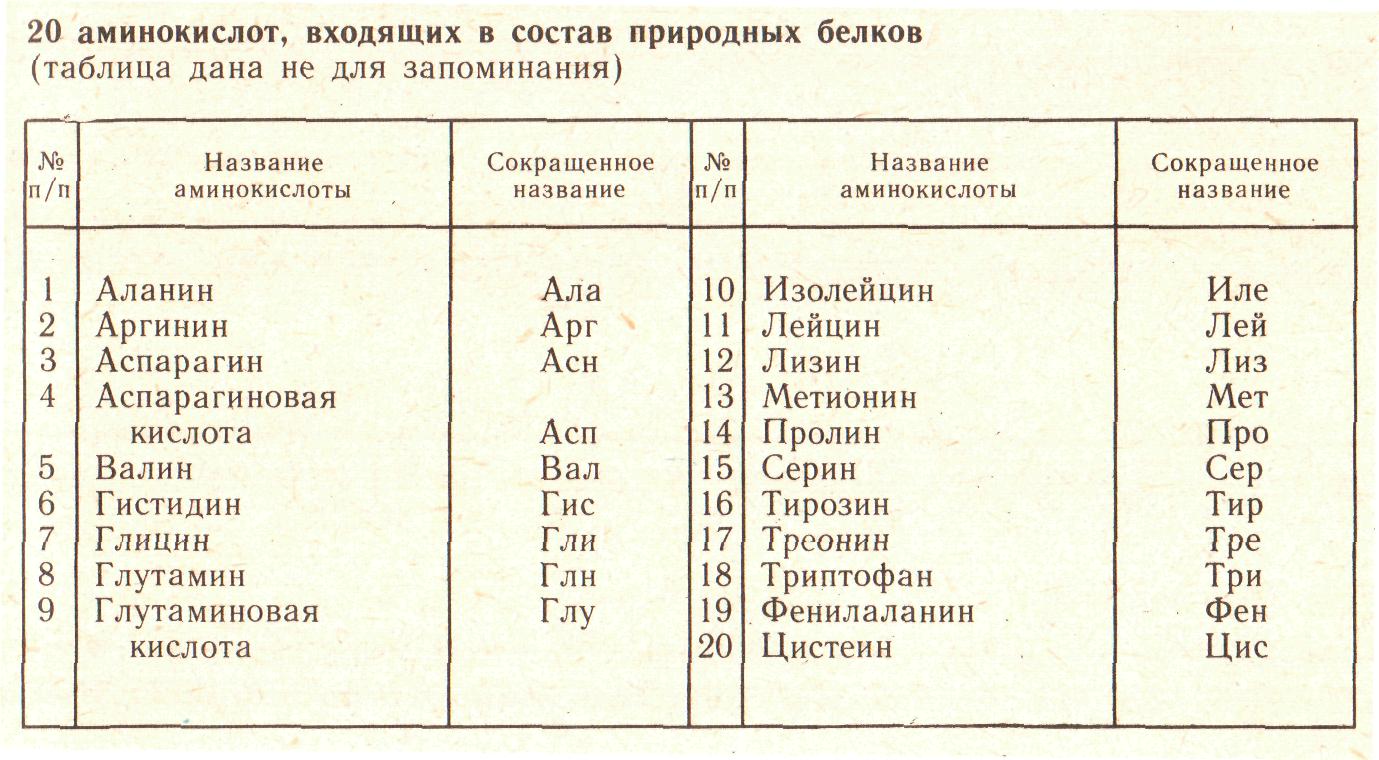
Рис. 19. 20 аминокислот, входящих в состав природных белков
Среди белков выделяют: 1 - простые белки - они состоят только из аминокислот и 2 сложные, включающие кроме аминокислот и другие группы различной химической природы, например, нуклеопротеины (protein - первый, означает белок), содержащие нуклеинозые кислоты, металлопротеины, содержащие различные металлы, липопротеины, имеют в своем составе липидный компонент. Эти группы играют важную роль при выполнении белками их функции. Белки отличаются друг от друга числом, последовательностью, составом аминокислот.
2. Структуры белка
1). Первичная. Аминокислоты соединены пептидной связью в линейной последовательности.
ЛИЗ- |
ГЛУ - |
ТРЕ - |
АЛА - |
АЛА - |
АЛА - |
ЛИЗ - |
ФЕН - |
ГЛУ - |
АРГ - |
ГЛН - |
ГИС - |
МЕТ - |
АСП - |
СЕР - |
СЕР - |
ТРЕ - |
СЕР - |
АЛА - |
АЛА - |
СЕР - |
СЕР- |
СЕР - |
АСН - |
ТИР - |
ЦИС - |
АСН - |
ГЛУ - |
2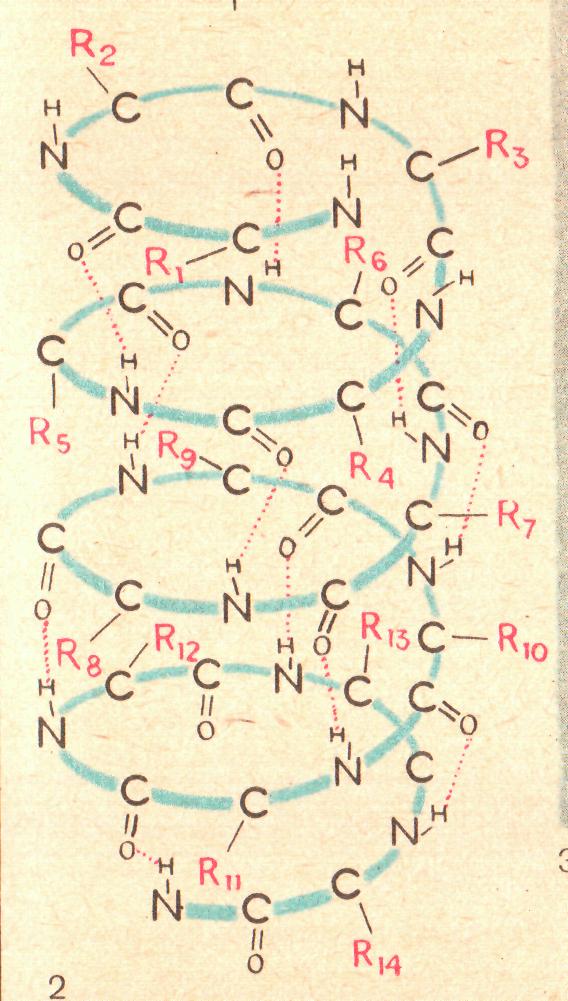 ).
Вторичная
структура,
имеет вид спирали. Возникает в результате
образования водородных связей между
СО и NH
– группами, между аминокислотными
остатками на разных витках спирали
(рис. 20).
).
Вторичная
структура,
имеет вид спирали. Возникает в результате
образования водородных связей между
СО и NH
– группами, между аминокислотными
остатками на разных витках спирали
(рис. 20).
3 ).
Третичная
структура
- имеет вид клубка. Образуется в результате
отталкивания радикалов от воды и слипания
их друг с другом, (гидрофобные связи)
(рис 21).
).
Третичная
структура
- имеет вид клубка. Образуется в результате
отталкивания радикалов от воды и слипания
их друг с другом, (гидрофобные связи)
(рис 21).
Рис. 20. Вторичная
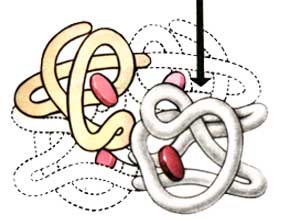 Рис.
21. Третичная
Рис.
21. Третичная
4). Некоторые белки имеют четвертичную структуру. Это сложный комплекс, клубок, (объединяющий несколько третичных структур (белок гемоглобин образован четырьмя полилептиднымин цепями) (рис. 22).
Рис. 22. Четвертичная
3. Денатурация белка.
Под действием высокой температуры, облучением, высокого давления четвертичная структур а белка может переходить в третичную, во вторичную, при этом меняются свойства белка и биологическая активность (вторичная структура белка - биологически неактивна). Денатурация может быть обратимой, т.е. возврат в четвертичную структуру белка. Этот процесс называется ренатурацией (рис. 23). Может быть необратимой, если происходит разрыв пептидных связей в составе первичной структуры белка.
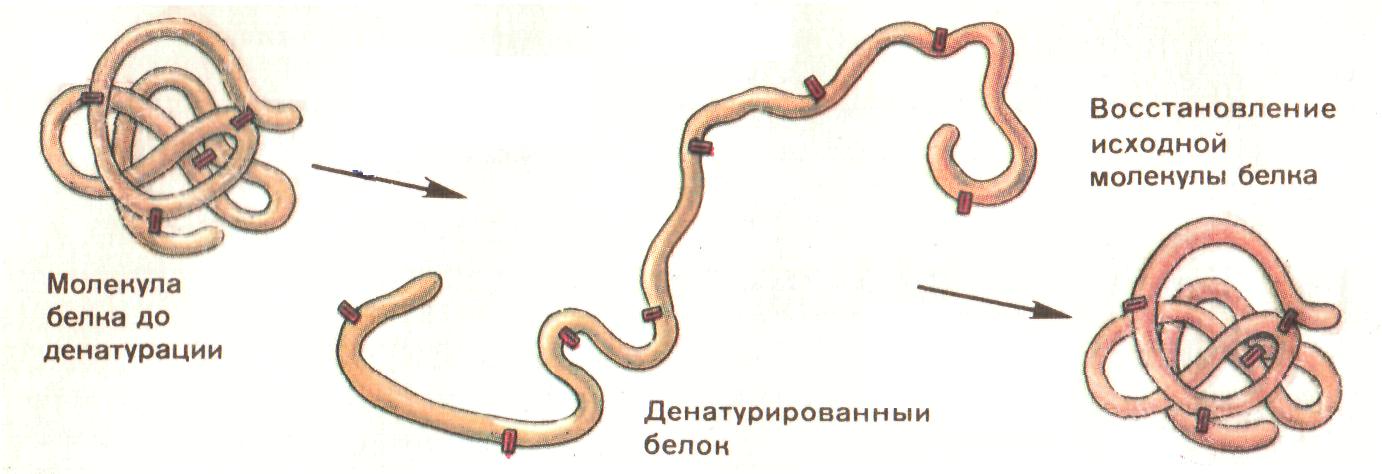
Рис. 23. Схема денатурации белка
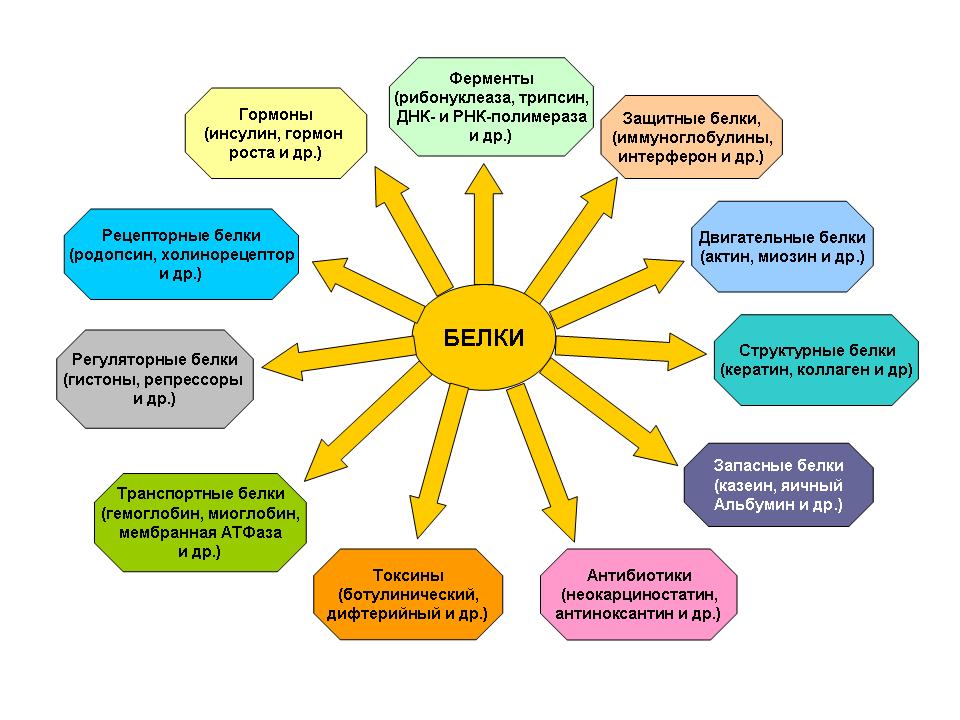
Белки выполняют в организме чрезвычайно важные функции:
1. Каталитическая или ферментативная. Ферменты являются катализаторами, т.е. ускорителями химических реакций в десятки и сотни миллионов раз. Каждый фермент катализирует определенный тип реакций. Например, жиры в пищеварительном тракте расщепляются специальным ферментом липазой, который не действует на сахара (крахмал). В свою очередь, фермент, расщепляющий крахмал-амилаза не действует на жиры. Каждая молекула фермента способна осуществлять несколько тысяч до несколько миллионов операций в минуту. В ходе этих операций фермент не расходуется. Он соединяется с реактирующими веществами, ускоряет их превращения и выходит из реакции неизменными. Активность ферментов зависит от витаминов.
2. Структурная функция или строительная. 80 - 90% сухого вещества клетки - это белки; белки входят в состав биологических мембран. Из структурных белков состоят волосы, ногти, шелк.
3. Транспортная функция. Транспортные белки связывают и переносят специфические молекулы и ионы из одного органа в другой. Гемоглобин переносит кислород.
4. Защитная функция. Защитные белки предохраняют Организм от вторжения других организмов и от повреждений. Эти антитела, вырабатываемые лимфоцитами, блокируют чужеродные антигены. Фиброноген и тромбин предохраняют организм от кровопотерь.
5. Регуляторная функция. Регуляторные белки участвуют в обмене веществ. Инсулин регулирует обмен глюкозы. Соматотропин (гормон роста) регулирует рост костей, пистоны (белки, соединенные с ДНК) - генную активность.
6. Пищеварительная функция. Пищеварительные белки питают зародыш на ранних стадиях развития и запасают биологически ценные вещества: ферритин запасает железо в селезенке.
7. Сократительная функция. Сократительные белки обеспечивают движение клеток; внутриклеточных структур. Например, миозин - сокращение мышечного волокна; тубулин - растяжение хромосом к полюсам клетки.
8. Энергетическая функция. При расщеплении 1 г белка образуется 1,76 кДж энергии.