
- •Лабораторный практикум по органической химии (часть 1)
- •Содержание
- •Введение
- •Указания к подготовке и выполнению лабораторных работ
- •Правила техники безопасности при работе в лаборатории
- •Общие положения:
- •Работа со взрывоопасными веществами и приборами:
- •Работа с горючими веществами:
- •Работа с токсичными веществами:
- •Работа с кислотами и щелочами:
- •Действия в случае возникновения несчастного случая и оказание первой помощи:
- •Методы очистки органических соединений
- •Методики лабораторных работ
- •Лабораторная работа № 1. Качественный анализ органических соединений
- •4.2. Лабораторная работа № 2. Предельные углеводороды и непредельные ряда этилена и ацетилена
- •4.3. Лабораторная работа № 3. Галогенпроизводные углеводородов.
- •4.4. Лабораторная работа № 4. Ароматические углеводороды
- •Опыт 1. Получение бензола из бензойной кислоты
- •4.5. Лабораторная работа № 5. Спирты
- •4.6. Лабораторная работа № 6. Альдегиды и кетоны.
- •Контрольные вопросы:
- •4.7. Лабораторная работа № 7. Карбоновые кислоты и их производные.
- •4.8. Лабораторная работа № 8. Фенолы.
- •Опыт 7. Образование трибромфенола
4.6. Лабораторная работа № 6. Альдегиды и кетоны.
Альдегиды и кетоны являются производными углеводородов, содержащими в своем составе карбонильную группу C=O. В отличие от кетонов, в альдегидах карбонильный углерод связан с одним атомом водорода. Это предопределяет их более высокую реакционную способность. Большинство реакций присоединения протекают за счет двойной связи карбонильной группы, которая поляризована. Реакции нуклеофильного присоединения начинаются с атаки нуклеофильным реагентом ( Nu-) атома углерода и завершаются последующим присоединением электрофильного реагента (чаще всего протона Н+):
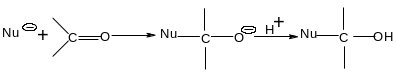
 δ+
δ
_
δ+
δ
_
Альдегиды и кетоны по разному относятся к действию окислителей. Первые окисляются очень легко с образованием карбоновых кислот, кетоны окисляются значительно труднее с разрывом углеродной цепи около карбонильной группы.
Карбонильная группа по индукционному механизму или механизму сопряжения вызывает смещение электронных плотностей соседних с ней простых или двойных связей, что обуславливает подвижность атомов водорода в α -положении к карбонильной группе.
![]()
![]()
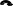 δ
+
δ
-
или δ
+
δ
-
δ
+
δ
-
δ
+
δ
-
или δ
+
δ
-
δ
+
δ
-
Ряд реакций (с галогенидами фосфора (V), гидразином, гидроксиламином и др.) приводит к замещению кислорода карбонильной группы другими атомами.
Материалы: 40 %-ный раствор формальдегида; метиловый красный; 10 %-ный раствор гидроксида натрия; 1 %-ный раствор нитрата серебра; 5 %-ный раствор аммиака; растворы Фелинга-1 (раствор сульфата меди) и Фелинга-2 (щелочной раствор сегнетовой соли); 1 %-ный раствор формальдегида; фуксинсернистая кислота; солянокислый гидроксиламин; безводный карбонат натрия; ацетон; гидросульфит натрия.
Опыт 1. Самоокисление-самовосстановление водных растворов формальдегида
В пробирку помещают 2-3 капли 40 %-ного раствора формальдегида и добавляют 1 каплю индикатора метилового красного. Раствор приобретает красную окраску, что указывает на кислую реакцию.
В водных растворах часть молекул альдегидов может окисляться в кислоту, при этом другая часть молекул восстанавливается в спирт. Подобные окислительно-восстановительные реакции называются реакциями диспропорционирования:
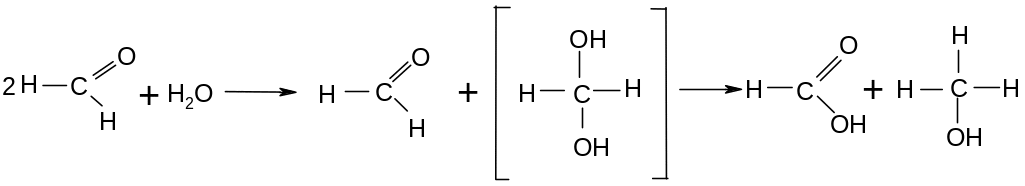
гидратная форма формальдегида
Опыт 2. Реакция «серебряного зеркала»
В чистую пробирку, которую вымыли при нагревании 10 %-ным раствором гидроксида натрия и ополоснули дистиллированной водой, наливают 2-3 мл 1 %-ного раствора нитрата серебра и прибавляют по каплям 5 %-ный раствор аммиака в таком количестве, чтобы образовавшийся вначале осадок снова растворился. К полученному раствору прибавляют 1 мл 40 %-ного раствора формальдегида и смесь осторожно нагревают на водяной бане при температуре 60-70 0С. Стенки пробирки покрываются слоем металлического серебра-зеркала:
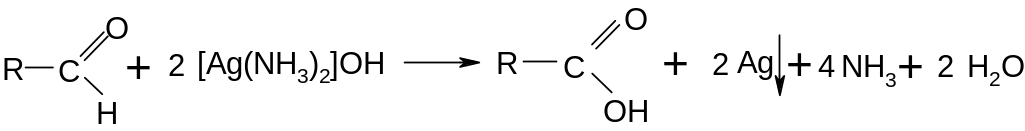
Опыт 3. Окисление формальдегида реактивом Фелинга
![]()

При
сливании растворов Фелинг-1 и Фелинг-2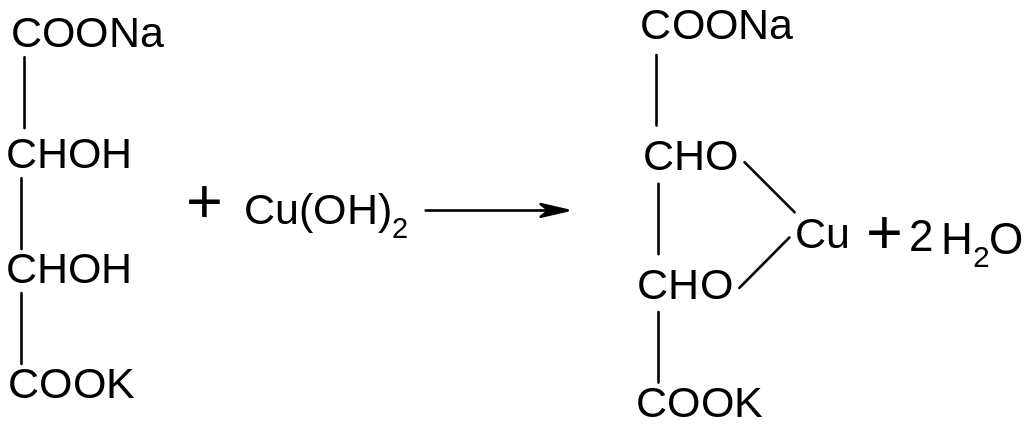
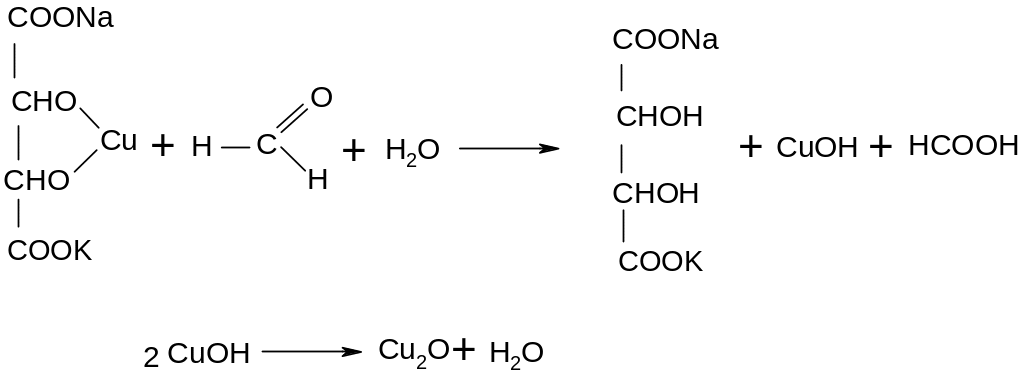
В пробирке смешивают по 2 мл растворов Фелинга-1 (раствор сульфата меди) и Фелинга-2 (щелочной раствор сегнетовой соли). К образовавшемуся синему раствору комплекса (реактив Фелинга) добавляют 1 мл 1 %-ного раствора формальдегида и кипятят. Сначала раствор окрашивается в синий цвет, затем в желтый и, наконец, выпадает оксид меди (I) красного цвета.
Опыт 4. Цветная реакция на альдегиды с фуксинсернистой кислотой
При присоединении альдегидов к бесцветной фуксинсернистой кислоте происходит перегруппировка и возникает хиноидная структура, обуславливающая красную окраску:
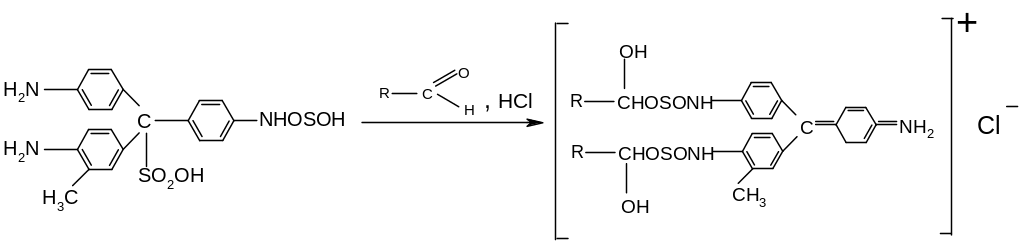
В пробирку наливают 2-3 мл фуксинсернистой кислоты и добавляют 1 мл 1 %-ного раствора формальдегида. Появляется красное окрашивание.
Опыт 5. Получение оксима ацетона
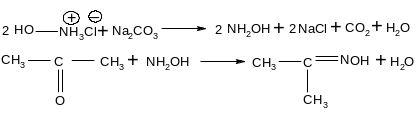
В пробирке растворяют 1 г солянокислого гидроксилами-на, и нейтрализуют кислый раствор безводным карбонатом натрия, добавляя его небольшими порциями при встряхивании. При этом выделяется оксид углерода (IV). Пробирку с полученным раствором охлаждают в стакане с ледяной водой и прибавляют в нее 1 мл ацетона. Выделяются бесцветные кристаллы оксима ацетона.
Опыт 6. Присоединение гидросульфита натрия
В реакцию с гидросульфитом натрия вступают лишь кетоны, имеющие рядом с карбонильной группой СН3 – группу.
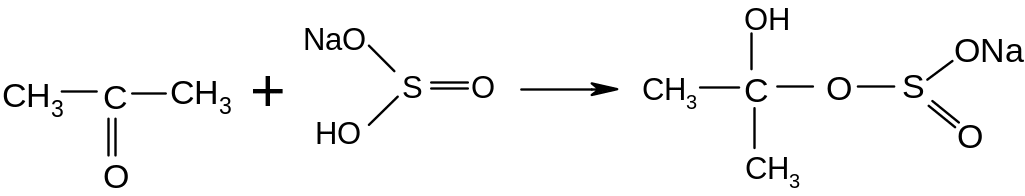
В пробирку наливают 3 мл насыщенного раствора гидросульфита натрия и при энергичном встряхивании добавляют 1 мл ацетона. При охлаждении смеси в ледяной воде выпадает кристаллический осадок. Если осадок не появился сразу, то вызывают кристаллизацию потиранием стеклянной палочкой о стенки пробирки.
