
- •Практикум по общей химической технологии
- •1.1. Теоретические сведения
- •1.2. Методика проведения работы
- •1.2.1. Определение карбонатной жёсткости воды
- •1.2.2. Определение общей и некарбонатной жёсткости воды трилоном б
- •1.4. Умягчение воды ионообменным методом
- •1.5. Порядок оформления работы
- •Вопросы для допуска к работе
- •Рекомендуемая литература
- •Работа №2. Дегидратация этилового спирта
- •2.1. Теоретические сведения
- •2.2. Описание установки и методика проведения работы
- •2.3. Методика проведения эксперимента
- •Работа № 3. Полукоксование твёрдого топлива
- •3.1. Теоретические сведения
- •3.1.1. Влияние температуры
- •3.1.2. Влияние фракционного состава исходного топлива
- •3.1.3. Влияние состава исходного сырья
- •3.2. Методика выполнения работы
- •3.2.1.Определение влажности топлива
- •3.2.2. Определение зольности топлива
- •3.3. Запись результатов
- •Рекомендуемая литература
- •Работа № 4. Обжиг серного колчедана
- •4.1 Теоретические сведения
- •4.2. Методическая часть
- •4.2.1. Описание установки
- •4.2.2. Подготовка установки к работе
- •4.2.3. Ход выполнения работы
- •4.3. Обработка экспериментальных данных
- •4.3.1. Форма записи результатов работы
- •4.3.2 Проведение расчётов
- •4.3.3. Компьютерная обработка данных
- •4.3.4. Определение стадии, лимитирующей скорость процесса
- •5.1.2. Проточный реактор идеального смешения
- •5.3. Обработка результатов эксперимента
- •5.3.1. Форма записи экспериментальных данных
- •5.3.2. Расчёт работы реактора
- •6.1.2. Выполнение работы
- •6.2. Обработка результатов эксперимента
- •6.2.1. Форма записи экспериментальных результатов
- •6.2.2. Расчёт работы реактора
- •Рекомендуемая литература к работе 5 и 6
- •Содержание
5.1.2. Проточный реактор идеального смешения
Проточный реактор идеального смешения представляет собой аппарат, в котором интенсивно перемешиваются реагенты, например, при помощи мешалки. В него непрерывно подаются реагенты и непрерывно выводятся продукты реакции. Поступающие в такой реактор частицы вещества быстро смешиваются с находящимися в нем частицами и равномерно распределяются в объёме аппарата. В результате во всех точках реакционного объёма мгновенно выравниваются параметры, характеризующие процесс: концентрации, степени превращения, скорости реакции, температуры и др.
5.2. Методическая часть
5.2.1. Химизм процесса
В данной работе проводят исследование реактора идеального смешения на примере реакции 2-го порядка - омыления этилацетата щелочью:
![]()
(5.3)
5.2.2. Описание установки
Установка состоит (рис.) из реактора, снабжённого термостатированной рубашкой, мешалкой с приводом.
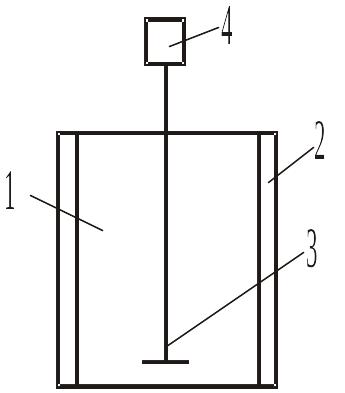
Реактор смешения:
1 - реактор; 2 - рубашка; 3 - мешалка; 4 - привод
5.2.3. Выполнение работы
В колбы для титрования с помощью пипетки вносят 5 мл 0,1 Н раствора соляной кислоты. Заливают в реактор, нагретый с помощью термостата до заданной температуры, рассчитанное количество раствора эфира и включают мешалку. Быстро вливают в реактор раствор 0,1 Н едкого натра и одновременно включают секундомер. Через определенный промежуток времени производят отбор проб с помощью пипетки на 10 мл и переносят их в колбы для титрования. При смешении отобранной пробы с раствором соляной кислоты, находящейся в колбе, происходит нейтрализация щёлочи и прекращение реакции гидролиза эфира.
Проводят титрование избытка соляной кислоты 0,1 Н раствором едкого натра с фенолфталеином в качестве индикатора или с помощью установки автоматического титрования до заданной точки (величина pH равна 8).
Титрование с фенолфталеином ведут до появления устойчивой в течение 10 секунд окраски от последней капли титранта.
После окончания титрования записывают объём щёлочи, пошедший на нейтрализацию соляной кислоты.
Пробы отбирают через 0,5; 1; 2; 3; 5; 7; 10; 13; 15 и 20 минут после начала опыта. Полученные данные сводят в таблицу 2.
5.3. Обработка результатов эксперимента
5.3.1. Форма записи экспериментальных данных
Исходные данные для расчётов реактора смешения периодического действия вносят в таблицу 5.1.
Таблица 5.1. Исходные данные
Название и формула эфира уксусной кислоты |
Объём 0,1 Н раствора щёлочи (Vщ), мл |
Объём 0,1 Н раствора эфира (Vэф), мл |
Начальная
концентрация щёлочи (С |
Начальная
концентрация эфира (С |
|
|
|
|
|
Начальные концентрации щёлочи и эфира в реакторе находят по уравнениям
C = Vщ Nщ/(Vщ + Vэф) , (5.4)
где Vщ - объём щёлочи в реакторе, мл; Nщ - концентрация щёлочи в исходном растворе, моль/л; Vэф - объём раствора эфира в реакторе, мл.
C = Vэф Nэф/(Vщ + Vэф) , (5.5)
где Nэф - концентрация эфира в исходном растворе, моль/л.
Экспериментальные результаты исследования работы РИС заносят в таблицу 5.2.
Таблица 5.2. Экспериментальные результаты
Время опыта (), мин |
Объём 0,1 Н раствора щёлочи на титрование пробы (Vx), мл |
Концентрация щёлочи (Сщ), моль/л |
Концентрация эфира (Сэф), моль/л |
|
|
|
|
