
- •Гоу спо «Ярославский химико-механический техникум» рабочая тетрадь практические и лабораторные работы по физико-химическим и современным методам анализа
- •Содержание
- •Тема: «Кондуктометрический метод анализа» Практическое занятие 1: «Построение кривых кондуктометрического титрования».
- •Повторение пройденного материала.
- •Решение задач:
- •Задания для самостоятельной работы
- •Практическое занятие 2: «Расчет удельной, эквивалентной электрической проводимости».
- •Практическое занятие 3: «Изучение устройства кондуктометра».
- •Принцип действия реохордного моста р-38.
- •Лабораторная работа: «Кондуктометрическое титрование смеси кислот по методу нейтрализации».
- •Работа в лаборатории.
- •Лабораторная работа: «Кондуктометрический анализ смеси серной кислоты и сульфата меди по методу осаждения».
- •Работа в лаборатории.
- •Лабораторная работа: «Кондуктометрическое определение растворимости труднорастворимых соединений».
- •Работа в лаборатории.
- •Кондуктометрический метод анализа. Тест для самоконтроля.
- •Тема: «Потенциометрический метод анализа» Практическое занятие 1: «Расчет эдс системы и практическое применение потенциометрии».
- •Повторение пройденного материала.
- •2. Решение задач:
- •Практическое занятие 2: «Построение кривых потенциометрического титрования».
- •Повторение пройденного материала.
- •2. Решение задач:
- •Общие указания по работе с прибором.
- •Иономер 120.1
- •Органы оперативной настройки:
- •Лабораторная работа: «Потенциометрическое титрование смеси сильной и слабой кислот по методу нейтрализации».
- •Работа в лаборатории.
- •Лабораторная работа: «Потенциометрическое титрование по методу окисления-восстановления».
- •Работа в лаборатории.
- •Лабораторная работа: «Определение галогенов при совместном присутствии».
- •Работа в лаборатории.
- •Работа в лаборатории.
- •Обсчет результатов методом математической статистики:
- •Лабораторная работа: «Определение концентрации ионов водорода потенциометрическим методом с применением стеклянного индикаторного электрода».
- •Работа в лаборатории.
- •Лабораторная работа: «Определение рН с помощью хингидронного электрода».
- •Работа в лаборатории.
- •Потенциометрический метод анализа. Тест для самоконтроля.
- •Тема: «Электрогравиметрический и кулонометрический методы анализа» Практическое занятие 1: «Решение задач на законы Фарадея».
- •Повторение проеденного материала
- •2. Решение задач:
- •Практическое занятие 2: «Расчет количества электричества, изучение электролизеров».
- •Повторение проеденного материала
- •2. Решение задач:
- •Работа в лаборатории.
- •Работа в лаборатории.
- •Электрогравиметрический и кулонометрический методы анализа. Тест для самоконтроля.
- •Тема: «Полярографический метод анализа Практическое занятие 1: «Построение полярограмм».
- •Повторение пройденного материала.
- •2. Решение задач:
- •Практическое занятие 2: «Построение кривых амперометрического титрования».
- •Повторение пройденного материала.
- •2. Решение задач:
- •Полярограф ппт -1
- •1. Назначение полярографа.
- •2. Основные понятия о полярографии.
- •3. Структурная схема полярографа. Конструкция.
- •4.4. Окончание работы.
- •Лабораторная работа: «Качественное определение веществ полярографическим методом».
- •Работа в лаборатории.
- •Лабораторная работа: «Количественное определение веществ методом градуировочного графика».
- •Работа в лаборатории.
- •Лабораторная работа: «Количественное определение концентрации вещества методом добавок».
- •Работа в лаборатории.
- •Полярографический метод анализа. Тест для самоконтроля.
- •Современные методы анализа Тема: «Кинетические методы анализа» Лабораторная работа: «Определение концентрации молибдена (VI) в растворах кинетическим методом (метод тангенсов)».
- •Работа в лаборатории.
- •Обсчет результатов методом математической статистики:
- •Лабораторная работа: «Определение концентрации молибдата (VI) в растворах кинетическим методом (метод фиксированного времени)».
- •Работа в лаборатории.
- •Обсчет результатов методом математической статистики:
- •Лабораторная работа: «Определение концентрации молибдата (VI) в растворах кинетическим методом (метод фиксированной концентрации)».
- •Работа в лаборатории.
- •Обсчет результатов методом математической статистики:
- •Тема: «Термические методы анализа» Лабораторная работа: «Определение массы бария методом термометрического титрования».
- •Работа в лаборатории.
- •Лабораторная работа: «Определение массы щелочи методом термометрического титрования».
- •Работа в лаборатории.
- •Лабораторная работа: «Определение смеси компонентов термометрическим методом».
- •Работа в лаборатории.
Лабораторная работа: «Определение смеси компонентов термометрическим методом».
Цель работы:
1. Освоить методику термометрического титрования смеси компонентов.
2. По графику термометрического титрования определить точки эквивалентности для Ca2+ и Mg2+.
Теоретические основы:
Метод термометрического титрования основан на измерении теплового эффекта реакции титрования или величин пропорциональных этому тепловому эффекту.
![]()
где ∆Т – изменение температуры вследствие теплового эффекта реакции
∆Н – изменение энтальпии реакции 1 моля вещества
П – число молей образовавшегося вещества
К – теплоемкость системы, кДж/к
Следовательно: изменение температуры при титровании прямопропорционально числу молей образовавшегося продукта.
Для уменьшения погрешности титрования следует соблюдать ряд условий. Реакции должны протекать быстро. Концентрация анализируемого раствора должна быть не менее 10-3 М. Изменения объема при титровании должны быть небольшими, для этого применяют концентрированные растворы титранта.
Поскольку все химические реакции происходят с эндо- или экзотермическим изменением энтальпии, метод термометрического титрования может быть использован при проведении самых разных реакций титрования, в том числе и для анализа смеси компонентов без предварительного их разделения.
Титрование ионов Ca2+ и Mg2+ триллоном Б соответствует реакциям:
![]()
![]()
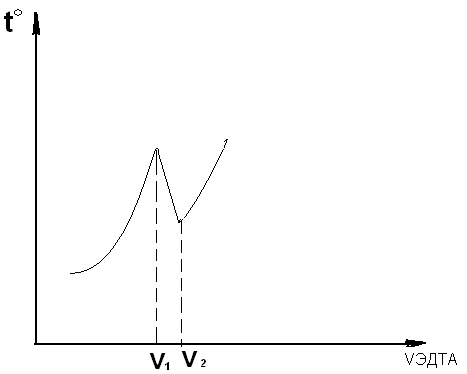
V1 – объем точки эквивалентности для Ca2+
V2 – V1 – объем точки эквивалентности для Mg2+
Расчет результатов определения проводят по формулам:
 ,
(г/ см3)
,
(г/ см3)
![]() ,
(г)
,
(г)
 ,
(г/ см3)
,
(г/ см3)
![]() ,
(г)
,
(г)
Задание:
1. Изучить теоретический материал по данной теме.
2. Изучить особенность термометра Бекмана
3. Проделать работу.
4. Ответить на контрольные вопросы.
5. Сделать выводы по проделанной работе.
Работа в лаборатории.
Необходимое оборудование и реактивы:
1. Установка для титрования с термометром Бекмана.
2. Раствор ЭДТА 0,25 M
3. Смесь растворов Ca2+ и Mg2+ - анализируемый раствор.
4. Дистиллированная вода
5. Колба на 100 см3
6. Пипетка на 20 см3.
7 . Стеклянная палочка.
Схема установки:
1. Термометр Бекмана
2. Стаканчик для титрования
3. Бюретка
4. Термостат.
Ход работы:
Термометр Бекмана перед работой должен быть настроен по анализируемому раствору. Собрать установку для титрования. В бюретку залить раствор ЭДТА. Полученный анализируемый раствор в колбе довести до метки дистиллированной водой. В стакан для титрования залить 40 см3 приготовленного раствора. Термометр опустить в стакан с раствором так, чтобы ртутный резервуар был полностью погружен в раствор. Термометр выдержать в растворе до постоянной температуры, затем провести титрование путем приливания титранта (раствора ЭДТА) по 0,5 см3 и перемешивания стеклянной палочкой. После каждого приливания температура раствора должна быть постоянной. Все измерения занести в таблицу.
Объем раствора ЭДТА, пошедший на титрование, см3 |
Температура анализируемого раствора, 0С |
Температура анализируемого раствора, 0С |
0,00 |
|
|
0,50 |
|
|
1,00 |
|
|
1,50 |
|
|
2,00 |
|
|
2,50 |
|
|
3,00 |
|
|
3,50 |
|
|
4,00 |
|
|
4,50 |
|
|
5,00 |
|
|
5,50 |
|
|
6,00 |
|
|
6,50 |
|
|
7,00 |
|
|
7,50 |
|
|
8,00 |
|
|
8,50 |
|
|
9,00 |
|
|
9,50 |
|
|
10,00 |
|
|
10,50 |
|
|
11,00 |
|
|
После окончания работы построить график зависимости температуры от объема раствора ЭДТА, пошедшего на титрование. По графику определить точки эквивалентности для Ca2+ и Mg2+ и соответствующие им объемы раствора ЭДТА. Рассчитать массу растворов Ca2+ и Mg2+. Рассчитать погрешность определения.
Контрольные вопросы:
1. Кривая термометрического титрования для экзотермической и эндотермической реакции.
2. Как связан тепловой эффект реакции с изменением энтальпии системы?
3. Сущность термогравиметрии.
4. Сущность дилатометрии.
Список использованной литературы:
Основы аналитической химии. Книга 2. методы химического анализа. Ред. Ю.А. Золотова, М.: Высшая школа, 1996 г.
