
- •12.2. Галогенпроизводные углеводородов.
- •12.3. Нуклеофильное замещение.
- •12.4. Побочные реакции при sn1-замещении.
- •12.5. Реакции отщепления.
- •13.1. Введение.
- •14.1. Гликоли.
- •1 4.2. Двухатомные фенолы.
- •14.3. Трехатомные спирты. Глицерин.
- •14.4. Простые эфиры.
- •14.5. Строение и номенклатура оксосоединений.
- •14.6. Методы синтеза оксосоединений.
- •14.7. Строение карбонильной группы.
- •14.8. Химические свойства оксосоединений.
- •15.1. Реакции окисления.
- •15.2. Реакции замещения водорода в -положении по отношению к
- •15.3. Реакции конденсации.
- •15.4. Реакции замещения кислорода на галогены.
- •1 5.5. Реакции восстановления.
- •15.6. Реакции полимеризации.
- •15.7. Дикарбонильные соединения.
- •16.1 Введение.
- •16.2. Монокарбоновые насыщенные кислоты.
- •16.3. Ассоциация карбоновых кислот.
- •16.3. Строение карбоксильной группы.
- •16.4. Химические свойства.
- •16.5. Ненасыщенные карбоновые кислоты.
- •17.1. Классификация, номенклатура, изомерия.
- •17.2. Методы синтеза.
- •17.3. Химические свойства.
- •18.1. Нитросоединения.
- •18.2. Амины.
- •19.1. Свойства ароматических аминов.
- •19.2. Диамины.
- •19.3. Ароматические диазосоединения.
- •19.4. Алифатические диазосоединения.
- •20.1.Введение.
- •20.2. Производные непереходных элементов.
- •20.3. Эос переходных элементов.
- •20.4. Общие методы синтеза.
- •20.5. Серусодержашие соединения.
- •20.6. Фосфорорганические соединения.
15.2. Реакции замещения водорода в -положении по отношению к
карбонильной группе.
Эти реакции идут по механизму SE и катализируются как щелочами, так и кислотами:
H+ , HO
R CH2COH + Cl2 RCHClCOH
HCl
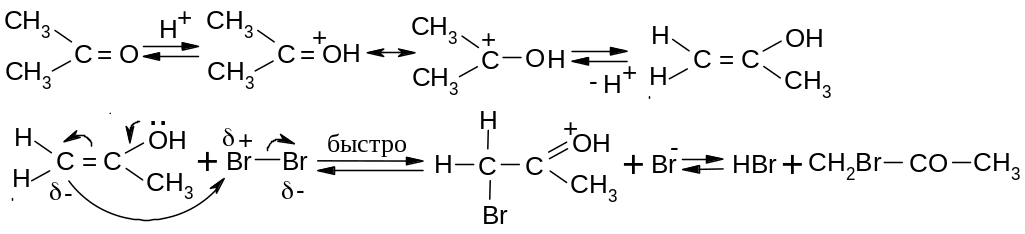 Реакция
протекает с образованием промежуточного
енола, например, при кислотном катализе:
Реакция
протекает с образованием промежуточного
енола, например, при кислотном катализе:
Скорость реакции не зависит от концентрации галогена и определяется скоростью превращения кетона в енол.
Галогенирование легко протекает до полного замещения водорода в -положении, и выделить промежуточные продукты часто не удается:
RCOCH3 + 3Cl2 + 3NaOH RCOCCl3 + 3NaCl + 3H2O
В щелочной среде происходит так называемое галоформное расщепление с образованием галоформа и соли карбоновой кислоты. Эта реакция является качественной на алкилметилкетоны:
 RCOCCl3
+ Н ОNa RCOONa
+ HCCl3 (хлороформ).
RCOCCl3
+ Н ОNa RCOONa
+ HCCl3 (хлороформ).
15.3. Реакции конденсации.
Это очень большая группа реакций, в которых участвует две молекулы, одна из которых обязательно должна содержать карбонильную группу. Такое вещество называют карбонильной компонентой. Вторая молекула альдегида или кетона реагирует за счет -водорода, который подвижен и может отщепляться. Такая молекула (или вещество) называется метиленовой компонентой. Реакции катализируются как кислотами, так и основаниями. Роль кислоты (протона) сводится к активации карбонильной группы:
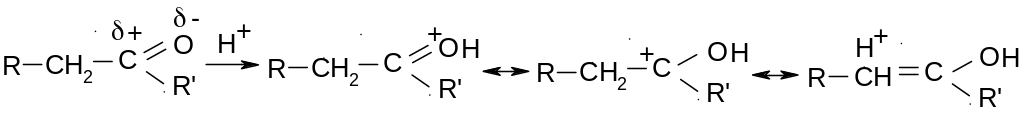 Роль
щелочи сводится к активации метиленовой
компоненты:
Роль
щелочи сводится к активации метиленовой
компоненты:
О бразующийся
анион имеет два нуклеофильных центра
(поэтому называется амбидентным), причем,
атом углерода более нуклеофилен (меньше
поляризован и больше поляризуется), чем
атом кислорода, поэтому этот анион в
первую очередь образует новые С
С связи, но не С О.
бразующийся
анион имеет два нуклеофильных центра
(поэтому называется амбидентным), причем,
атом углерода более нуклеофилен (меньше
поляризован и больше поляризуется), чем
атом кислорода, поэтому этот анион в
первую очередь образует новые С
С связи, но не С О.
По своей активности карбонильные компоненты располагаются в ряд:
П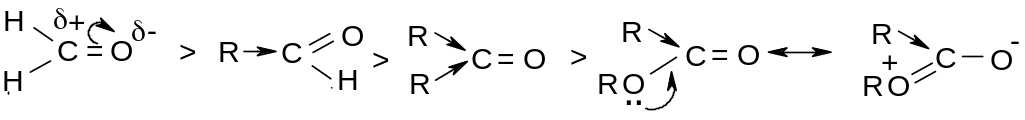 ричиной
снижения активности является +I
эффект R и +M
эффект насыщенного атома кислорода в
сложном эфире, что уменьшает +
заряд на карбонильном углероде.
ричиной
снижения активности является +I
эффект R и +M
эффект насыщенного атома кислорода в
сложном эфире, что уменьшает +
заряд на карбонильном углероде.
В качестве метиленовой компоненты может выступать не только оксосоединение, но и любое соединение, содержащее подвижный водород в -положении по отношению к электроноакцепторной группе, например: RCH2NO2 , RCH2CN , RCH2CCl3 .
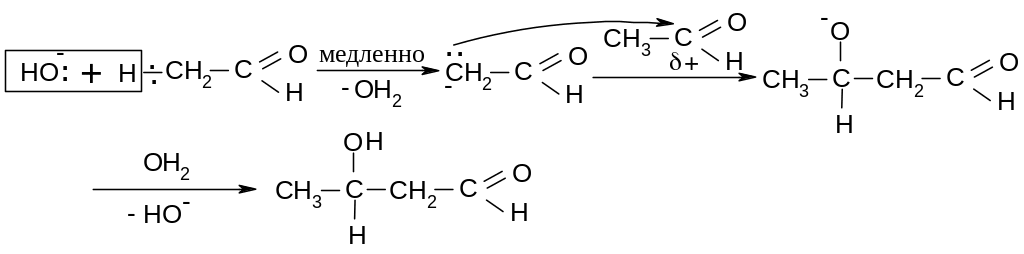
15.3.1.Альдольная конденсация.
А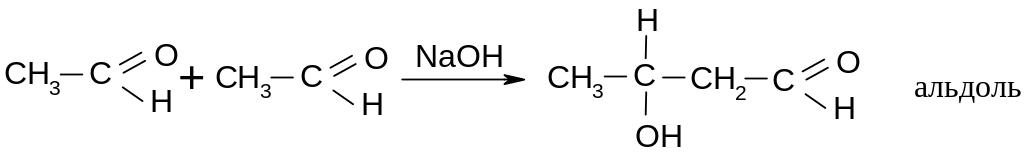 льдегиды
в щелочной среде вступают в альдольную
конденсацию:
льдегиды
в щелочной среде вступают в альдольную
конденсацию:
О
 бразование
названия: альд егидоалког оль альдоль.
бразование
названия: альд егидоалког оль альдоль.
Механизм:
15.3.2. Кротоновая конденсация.
При нагревании альдоль отщепляет воду, превращаясь в кротоновый альдегид, давший название данному типу конденсации:

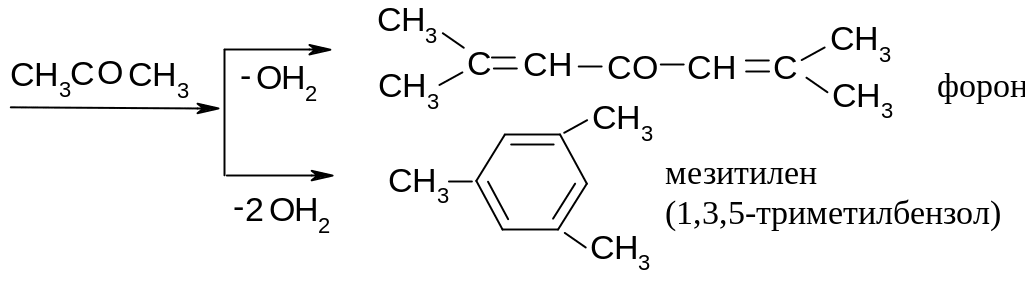
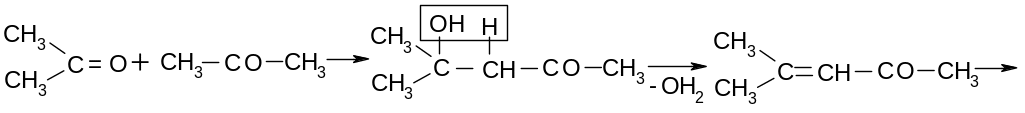 Щелочной
катализ активирует только метиленовую
компоненту, кислотный – обе. Поэтому в
кислой среде процесс не останавливается
на альдоле. Например, ацетон в
концентрированной серной кислоте
реагирует:
Щелочной
катализ активирует только метиленовую
компоненту, кислотный – обе. Поэтому в
кислой среде процесс не останавливается
на альдоле. Например, ацетон в
концентрированной серной кислоте
реагирует:
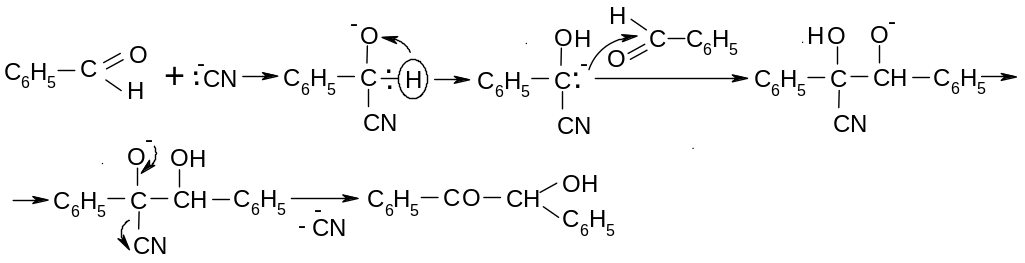
15.3.2. Бензоиновая конденсация.
При действии на бензойный альдегид каталитических количеств цианидов калия или натрия образуется бензоин:
М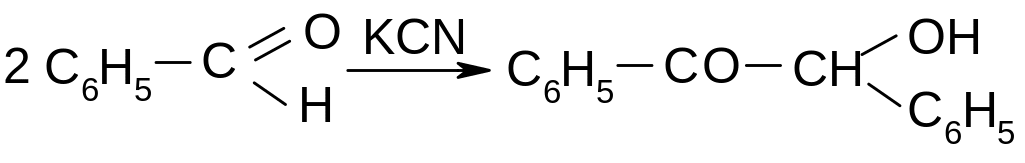 еханизм:
еханизм:
15.4. Реакции замещения кислорода на галогены.
RСОR’ + PCl5 POCl3 + RСCl2R’
