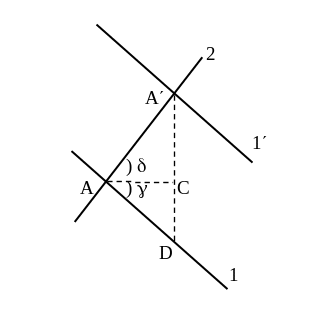- •Теория электрохимического перенапряжения, учитывающая структуру двойного электрического слоя
- •Влияние состава раствора на перенапряжение.
- •Закономерности перенапряжения выделения водорода
- •1. Влияние плотности тока
- •2. Влияние природы металла
- •3. Влияние природы и состава раствора
- •4. Влияние температуры и некоторых других факторов
- •Теория замедленной рекомбинации
- •Теория замедленной электрохимической десорбции
- •Ток обмена и коэффициент переноса
- •Порядок электрохимической реакции и стехиометрическое число
- •Механизм элементарного акта. Безбарьерный и безактивационный разряд
Механизм элементарного акта. Безбарьерный и безактивационный разряд
Итак, при рассмотрении механизма элементарного электрохимического акта целесообразно различать реакции, идущие с разрывом внутримолекулярных связей, и реакции, в ходе которых происходит лишь перестройка структуры частиц и растворителя с сохранением основных связей, существовавших в исходных частицах. Типичным примером реакций первого типа можно считать одну из наиболее часто встречающихся на практике и наиболее интенсивно изучаемую реакцию выделения водорода
2Н3О+ + 2еМ– = Н2 + 2Н2О
или, точнее, отвечающий ей элементарный электрохимический акт
Н3О+ + еМ– = Надс + Н2О ,
в ходе которого происходит разрыв связи Н+ – Н2О и образование связи Н – М. К реакциям второго типа относится, например, перезарядка ионов без изменения их химического состава
Sn4+ + 2еМ– = Sn2+ ,
Fe(CN)63– + еМ– = Fe(CN)64– .
Картину элементарного акта для реакций первого типа дали впервые Гориучи и Поляни (1935), используя метод потенциальных кривых. Обобщённая координата реакции в данном частном случае отождествляется с расстоянием от поверхности электрода или, точнее, с путём, проходимым протоном от его положения равновесия в системе Н+ – Н2О до положения в системе Н – М.
Основное положение теории Гориучи – Поляни заключается в том, что энергия активации стадии разряда – ионизации обусловлена растяжением химических связей в молекулах или ионах реагирующих веществ. Гориучи и Поляни развили свою теорию именно на примере реакции разряда ионов водорода. Элементарный акт этой реакции состоит в том, что один из протонов иона гидроксония переходит на поверхность электрода и, соединяясь с электроном, дает адсорбированный атом водорода
Н3О+ + е– = Надс + Н2О .
Ион Н3О+
может подходить к отрицательно заряженной
поверхности электрода только до
некоторого расстояния, определяемого
его эффективным радиусом. Дальнейшее
приближение протона к поверхности будет
сопряжено с растяжением связи Н+–
ОН2 , а потому потребует затраты
значительной энергии. Зависимость
потенциальной энергии протона в
адсорбированном ионе гидроксония от
расстояния до электрода должна поэтому
иметь вид кривой с минимумом при некотором
равновесном расстоянии R
=
![]() (см.
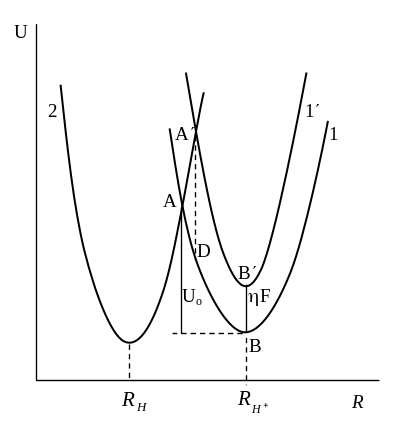
кривую 1 на рис. 41, а). В свою очередь,
потенциальная кривая адсорбированного
атома также должна проходить через
минимум в зависимости от расстояния до
электрода (кривая 2 рис. 41, а). Положение
минимума при R =
(см.
кривую 1 на рис. 41, а). В свою очередь,
потенциальная кривая адсорбированного
атома также должна проходить через
минимум в зависимости от расстояния до
электрода (кривая 2 рис. 41, а). Положение
минимума при R =
![]() на этой кривой соответствует равновесному
состоянию связи М – Н.
на этой кривой соответствует равновесному
состоянию связи М – Н.
|
|
a |
б |
Рис. 41. Потенциальные кривые для процесса разряда иона водорода по теории Гориучи – Поляни |
|
Как видно из рис. 41, а, равновесные положения в ионе Н3О+ и в состоянии адсорбированного атома разделены энергетическим барьером Uo . Таким образом, элементарный акт разряда в теории Гориучи – Поляни связан с движением протона вначале по кривой 1 до точки пересечения (растяжение связи Н+ – ОН2), а затем вдоль кривой 2 (переход растянутой связи М – Н к своему равновесному состоянию). Координатой реакции здесь является расстояние, перпендикулярное поверхности электрода.
Из рис. 41, а также видно, что Uo – энергия активации реакции разряда при равновесном потенциале – определяется разностью ординат точек А и В
Uo = UA – UB .
При изменении потенциала электрода на величину потенциальная кривая иона Н3О+ перемещается параллельно самой себе на величину F в положение 1, а потенциальная кривая адсорбированного атома никуда не сместится, так как Надс – частица незаряженная, и ее энергия не изменяется при изменении потенциала электрода. Новая энергия активации реакции разряда равна
U = UA – UB .
Из потенциальных диаграмм следует, что энергия активации электрохимических процессов зависит от перенапряжения и для прямой реакции, и для обратной.
Из приведённых соотношений вытекает ряд интересных следствий. При увеличении перенапряжения энергия активации исчезает и процесс становится безактивационным. Дальнейшее увеличение перенапряжения уже не может уменьшить энергию активации, то есть увеличить скорость прямой (катодной) реакции, что эквивалентно = 0. Это означает, что для обратной (анодной) реакции коэффициент переноса делается равным единице ( = 1). Для процессов с коэффициентом переноса, равным единице, энергия активации совпадает с тепловым эффектом элементарного акта. Эти процессы часто называются безбарьерными.