
 1.
1.
Полимеры. Общая характеристика.
Классификации. Методы очистки полимеров.
Полимерами называют
макромолекулы построенные
присоединением малых молекул (мономеров) друг к другу.
Выделяют следующие типы
классификации:
1) По происхождению:
Природные (биополимеры)
(белки, каучук, нукл.кисл.)
Синтетические (полиэтилен,
эпоксидные смолы) получаемые
методами поликонденсации и полимеризации.
2) По природе:
Органические
Элементоорганичесие
Неорганические
3) По химическому составу
молекулы:
Карбоцепные (осн. цепь постр. только из углеродных атомов) Гетероцепные (не менее двух
разл. атомов в цепи)
4) По форме молекулы:
Линейная (в виде цепочки)
Сшитые полимеры (сетка,
молекулы связаны
«перемычками»)
Привитые сополимеры (соед. несколько линейных молекул)
5) По назначению:
Для изготовления разл. протезов
Вспомогательные (оттискн. массы)
Клинические
Основными методами очистки
являются:
1) Диализ - удаление с помощью
мембран низкомолекулярных
соединений из коллоидных
растворов и растворов полимеров.
21 Дисперсные системы ,клас-ия.
. Природа коллоидного состояния
.получение и отчистка коллоидов
Дисперсные системы-сист.
Состоящая из дисперсной фазы -
совокупности раздробленных частиц и непрерывной дисперсионойсреды в которой во взвешенном состоянии находятся эти частицы.
Классификация( по степени
дисперсности )
1)грубодисперсные сист. Размер
частиц- >10^-7м
2)коллоидно - дисперсные . размер частиц от 10^-7 до 10^-9.
Классификация (агрегатному
состоянию фазы )
1)газ - аэрозоль
2) жидкость - лиозоль
3) твердое тело - солидозоль Если дисперсионной средой
является вода , то система
Называется гидрофобной или гидрофильной.
Система со слабым
взаимодействием - лиофобные
колоиды ( золи ). Система с сильным
взаимодействием - лиофильными
Если в систему существуют
устойчивые связи - это
связаннодисперсная система ( гель ),
если нет то свободнодисперсные
МЕТОДЫ ПОЛУЧЕНИЯ
Необходимо : 1)достичь коллоидной степени дисперсности . 2) подобрать
дисперсную среду, в которой не
растворимо вещество
дисперсионной фазы .3) подобрать
стабилизатор , сообщающий устойчивость.
Образовывать коллоидные растворы
в воде могут металы, мало
растворимые соли , оксиды ,
 При
этом
используют
св-во
При
этом
используют
св-во
полупроницаемости мембран.
2) Ультрафильтрация -
продавливание жидкости через полупроницаемую мембрану —
проницаемую для малых молекул
и ионов, но непроницаемую для
макромолекул и коллоидных частиц.
3) Переосаждение.
4) Хроматографические методы.
2. Методы получения полимеров и
реакции, лежащие в их основе
(полимеризации, сополимеризации, поликоиденсации).
кислоты гидроксилы .В качестве
стабилизаторов используют
вещества которые препятствуют агрегации.
1)ДИСПЕРГИРОВАНИЕ-измельчение жидкостей и тв. Частиц .Чем больше прикладывается работа тем меньше
размер частиц. Бывают :
1-Механическое дробление - с
помощью коллоидных мельниц.2-
Измельчение с помощью
ультрозвука
3-Электрическое диспергирование- для получениия золей металлов. 4-
Химическое диспергирование
2)КОНДЕСАЦИОННЫЕ МЕТОДЫ
1-физическая конденсация - физ.
Методы воздействия ,чаще всего
метод замены растворителя
2-химическая конденсация,
используют реакции:
Гидролиза :FeCl3 + 3 H2O =Fe(OH)3 +
3 HC l
Обмена ,окисления , нейтрализации
,
Восстановления : 2HAuCl4 + 3 H2O2
= 2Au + 8HCl + 3 O2
Методы отчистки коллоидных
растворов
1)фильтрация -задерживает
крупные частицы при прохождении через поры фильтров.
2)диализ - удаление с помочью
мембран низкомолекулярных
частиц из коллоидных растворов .малые частицы проходят через
капилляры мембран и
растворяются в веществе мембраны.
2 Молекулярно- кинетические
2. свойства коллоидных растворов.
Оптические свойства.
 1)
Полимеризация
- процесс
молекулярно-
кинетические
-
1)
Полимеризация
- процесс
молекулярно-
кинетические
-
образования
высокомолекулярного
вещества (полимера) путём
многократного присоединения молекул низкомолекулярного
вещества
(мономера, олигомера) к
активным центрам в растущей
молекуле полимера.По
классификации Карозерса
полимеризационными полимерами называют
полимеры, которые обр. из мономеров без выделения
низкомолекулярных побочных
продуктов. Механизм
полимеризации обычно
включает в себя ряд связанных
стадий:
Инициирование -
превращение небольшой доли мономера в активную частицу,
способные присоединять к себе новые молекулы мономера. Для созд. активн. центров используют
хим. не стойкие в-ва -
инициаторы, например, перекись бензоила. Инициирование можно
разд. на две стадии первая -
образование свободных
радикалов. вторая -
присоединение радикала к первой
молекуле мономера с
образованием инициирующей частицы растущей цепи.
Рост - процесс роста
заключается в последовательном
присоединении сотен и тысяч молекул мономера.
передача цепи — переход
активного центра на другую
молекулу;
разветвление цепи —
образование нескольких активных
свойства обусловленные
хаотическим тепловым движением частиц.
С точки зрения молек- кинет теории
коллоидные растворы - частный
случай истинных растворов БРОУНОВСКОЕ ДВИЖЕНИЕ Изучая цветочную пыльцу
обнаружил что частицы в воде
совершают : интенсивное
беспрерывное хаотическое
движение .Потом было установлено
что почти все частицы совершают
такие движения. Броуновское
движение присуще частицам размер которых не более 10^-6 м . Эйнштейн и Смолуховский
объяснили природу броуновского
движения
ДИФФУЗИЯ
Описывается законом фика -
скорость диффузии прямо
пропорцеонально площади поверхности,через которую
проходит вещество и градиенту его
концентрации. Уравнение позволяет
объяснить малую скорость
диффузии коллоидных частиц
,потому что коллоидные частицы
примерно в 100 раз больше атомов
молекул ионов
 центров
из
одного;
центров
из
одного;
обрыв цепи — гибель активных
центров в результате
биомолекулярной реакции между радикалами.
2) Сополимеризация -
полимеризация, в которой
участвуют два или несколько
различных мономеров. В
результате сополимеризации
образуются сополимеры,
макромолекулы которых состоят
из двух или более разнородных
структурных звеньев.
Сополимеризация позволяет
получать высокомолекулярные
вещества с разнообразными заданными свойствами.
3) Поликонденсация - процесс
синтеза полимеров из
полифункциональных (чаще
всего бифункциональных)
соединений,
сопровождающийся
выделением
низкомолекулярных побочных
продуктов
(воды, спиртов и т. п.) при
взаимодействии
функциональных групп.
3. Свойства растворов ВМС.
Особенности растворения ВМС.
Форма макромолекул. Механизм
набухания и влияние на этот
процесс различных факторов.
Термодинамика набухания. Влияние
пластификаторов на процессы
набухания полимерных
материалом, используемых в
стоматологии.
Растворение
высокомолекулярных веществ
принято рассматривать как
процесс, аналогичный смешению двух жидкостей, в котором имеет
2 Механизм возникновения заряда в
3. коллоидных частицах. Строение ДЭС.
Мицелла, гранула, ядро.
Электрический потенциал и влияние на него электролитов.
Электрический заряд на границе
раздела фаз может возникать или в
результате избирательной
адсорбции одного из ионов
растворенного электролита, или
 значение
как
энергетическое
значение
как
энергетическое
взаимодействие между
молекулами растворяемого
вещества и растворителя
(энергетический фактор), так и
действие фактора,
обусловливающего равномерное
распределение молекул
растворенного вещества в
растворе (энтропийный фактор). Благодаря аномально большим
значениям энтропии, при
растворении многих
высокополимеров энтропийный фактор играет решающую роль,
особенно при растворении полимеров с неполярными
молекулами, когда растворение
сопровождается поглощением тепла (Н > 0).
Особенностью растворения ВМС
- является то, что растворению
полимера предшествует его
набухание. При набухании ВМС поглощает низкомолекулярный растворительпри этом объём и масса увеличиваются.
Набухание проходит в несколько
этапов:
Проникновение
низкомолекулярного
растворителя в
полимер.(Сольватация)
Процесс экзотермический
H<0 S=0 G<0
Распределение
макромолекул по всему
объёму растворителя. S>0
H=0
Образование гомогенного
раствора в результате
распределения всех
молекул. S>0 H=0 G<0
Набухание
вследствие диссоциации
поверхностных молекул вещества
дисперсной фазы. В результате этих
процессов на границе раздела фаз
возникает ДЭС. ДЭС состоит из достаточно прочто связанных с
поверхностью дисперсной фазы ПОИ
и эквивалентного количества
противоположно заряженных ионов
- противоионов, находящихся в дисперсионной среде.
Расположение противоионов в
дисперсионной среде определяется
2 противоположными факторами:
тепловое движение стремится
распределить ионы равномерно по всему объему жидкой фазы, а силы
электростатического притяжения
стремятся удержать их вблизи поверхности раздела фаз.
В результате действия этих 2
факторов устанавливается
диффузионное распределение
противоионов с уменьшающейся
концентрацией по мере удаления от
межфазной поверхности. ПОИ
вместе со связанными
противоионами образуют
адсорбционный слой, толщина которого невелика. Оставшаяся
часть противоионов образует
диффузионный слой. ПОИ создают
на дисперсной фазе элект.заряд. Противополжный по знаку заряд
сосредоточен в дисперсионной
среде. Разность потенциалов между дисперсной фазой и дисперсионной
средой -
электротермодинамический
потенциал - опре-ся св-ми дан.сист. Скачок потенциала на поверхности
скольжения тесно связан с
электрокинетическими явлениями и
называется электрокинетическим
характеризуется степенью потенциалом (часть
набухания, величина которой электротермодинамического). Его
определяется количеством значение определяетяс толщиной
жидкости в граммах поглощаемой дифф.слоя. При увеличении
на данной стадии набухания и при концентрации Э в дисперсионной
д а н н ой температуре одним среде, сжатии дифф.слоя он умен-ся
граммом высокополимера:
a =(m2-m1)/ m1 где m1 масса
полимера до набухания; m2 - его
масса после набухания.
Степень и скорость набухания полимеров зависит от ряда факторов: температуры, давления, величины pH среды, присутствия
по абсол.значению. При наличии
многозарядных противоионов с
ростом концентрации Э дзета-
потенциал умен-ся, может изменить
знак и происходит перезарядка коллоидных частиц.
Электрокинетический потенциал
зависит от темп-ры. Увеличение - с
веществ, в особенности повышением темп-ры (толщина
электролитов, степени дифф.слоя увел-ся). Уменьшение - с
измельченности полимера ростом темпе-ры адсорбция и «возраста» полимера. уменьшается вследствие десорбции
Скорость набухания с ПОИ. Этот процесс приводит к
повышением температуры растет, уменьшению
а степень предельного электротермодинамического
набухания уменьшается, если потенциала и электрокинетического
процесс набухания потенциала.
сопровождается выделением Строение мицелл. Состоит из тепла. электронейтрального агрегата и
С ростом внешнего давления ионогенной части. Масса
степень набухания всегда сосредоточена в агрегате. Ионы,
повышается, что вытекает из определяющие заряд агрегата -
принципа Ле-Шателье, если ПОИ. Агрегат и ПОИ образуют ядро.
учитывать, что суммарный объем С заряженной поверхностью ядра
системы из растворителя и устойчиво связано некоторое число
растворяемого вещества пр и ионов противоположного знака -
набухании уменьшается.
Влияние pH среды на набухание хорошо изучено для белков и целлюлозы: минимум набухания лежит в области изоэлектрической точки (например для желатины при pH=4,7), по ту и другую сторону, от которой степень набухания возрастает и, достигнув
противоионов. ПОИ и связанные
противоионы образуют
адсорбционный слой. Агрегат +
адсорбционный слой =
гранула.Заряд гранулы равен сумме зарядов противо- и ПОИ.
максимумов, вновь начинает
уменьшаться.
Такое влияние pH на набухание
связано с тем, что в
изоэлектрической точке заряд макромолекул белков минимален, а вместе с этим минимальна и степень гидратации белковых и он ов .
Влияние электролитов также хорошо изучено для белков и целлюлозы. На процесс набухания оказывают влияние, главным образом, анионы, причем влияние последних своеобразно. Одни из них усиливают набухание, другие ослабляют. Это дало возможность все анионы расположить в закономерный ряд, получивший
н азван и е лиотропного ряда
набухания, или ряда Гофмейстера (по имени ученого, впервые открывшего это явление в 1891 г.):
Роданид > иодид > бромид > нитрат > хлорат.
Хлорид > ацетат > цитрат > тартрат > сульфат.
В первом ряду все анионы
усиливают набухание в
нисходящем порядке, т. е. максимальное усиление (для желатины вплоть до перехода набухания в полное растворение даже при комнатной температуре) дают роданид CNS- и иодид I -, а
наименьшее - хлорат CIO3. Во
втором ряду первый анион -
хлорид CI- занимает переходное
положение, а последующие
анионы не только не усиливают набухания, а наоборот, все более тормозят этот процесс, причем максимальное в этом смысле влияние оказывает сульфат -
ионSO42-.
Пластификаторы применяют для
повышения пластичности и
 расширения
интервала
расширения
интервала
высокоэластичного состояния
полимеров. Взаимодействуя с
пластификатором, полимеры
набухают, что связано с
образованием
мономолекулярного с л оя
пластификатора в окр у г цепи
полимера. Это так называемая наружная пластификация, которая не изменяет жесткости цепи
молекул. Повышение
пластичности достигается за счёт
уменьшения си л
межмолекулярного
взаимодействия в полимере.
4. Вязкость ВМС. Относительная, 2
приведенная, характеристическая
вязкости растворов. Уравнения
Штаудингера и Марка-Куна-
Хаувинка и использование их для
расчета молекулярной массы полимеров.
Вязкость растворов ВМС зависит
от концентрации вещества в
растворе. В отличие от других
растворов незначительная концентрация ВМС порой приводит к значительному
увеличению вязкости раствора.
Вязкость растворов ВМС зависит
от условий определения, в частности, от давления. Это
объясняется тем, что одни и те же макромолекулы могут находиться
в различных конформационных
состояниях: от линейных до
глобул, поэтому вязкость
растворов ВМС может быть
неодинакова в различных
направлениях. Вязкость
4.
макромолекул с выпрямленными
хаотично расположенными
звеньями выше, чем вязкость
макромолекул, которые имеют форму клубка.
Если вязкий полимер или его
раствор продавить через
капилляр, то молекулы будет
выпрямляться и располагаться
ориентированно, а вязкость будет снижаться.
Вязкость растворов ВМС зависит
также от свойств и температуры растворителя.
Для растворов ВМС
различают относительную,
удельную,
приведенную и характеристическ ую вязкости.
Относительная вязкость -
отношение вязкости раствора hр к
вязкости растворителя h0:
h о т н = h р / h 0 = tр / t0
tр время истечения раствора
ВМС, t0 - время истечения
растворителя(эти величины
определяются с помощью вискозиметра).
Удельная вязкость - показывает,
насколько увеличилась вязкость
раствора ВМС по сравнению с
вязкостью растворителя:
hуд = (hр - h0)/ h0 = (tр - t0)/ t0 =hотн -
1 (15.4)
Приведенная вязкость -
отношение удельной вязкости к
концентрации:
hпр = hуд/с (15.5)
Обычно приведенная вязкость
линейно зависит от концентрации
(рис.15.2).При экстраполяции
прямой до пересечения с осью
ординат получают величину /h/,
которую
 называют
характеристической
называют
характеристической
вязкостью:
/h/ = lim hуд/с (15.6)
Характеристическую вязкость
определяют на основании
вискозиметрических измерений,
используя значение
относительной, удельной и приведенной вязкостей.
Характеристическая вязкость для
данной пары веществ является
величиной условной, но
постоянной, она не зависит от концентрации растворителя и
состояния макромолекул, кроме того, она связана с молекулярной массой макромолекул.
/h/ = kМа, lg/h/ = lg k +
аlg М (15.7)
М - средняя молекулярная масса ВМС, а, k - коэффициенты.
Уравнение 15.7 - уравнение Марка-Куна-Хаувинка.
Для растворов полимеров с
короткими и жесткими цепями а =
1 и уравнение 15.7 упрощается:
/h/ = kМ, lg /h/
= lg k + lgМ (15.8)
Коэффициент a зависит от формы молекул.
Значение коэффициентов
определяют экспериментально,
это позволяет по значению
характеристической вязкости
рассчитать молекулярную массу
макромолекул. Зная массу, можно
определить средний
размер r макромолекул:
М = 4/3pr3NАr (15.9)
 Уравнение
Штаудингера:
hуд/с
=
Уравнение
Штаудингера:
hуд/с
=
Kм*M
5. Осмотическое давление
растворов биополимеров.
Уравнение
Галлера. Полиэлектролиты. Изоэлектрическая точка.
Онкотическое
давление плазмы крови.
Осмотическое давление растворов ВМС определяется теоретическим
уравнением Вант-Гоффа: п=cRT где с- концентрация раствора.
Для практического же подсчёта
осмотического давления раствора
ВМС Галлер предложил уравнение: п=(RT/M)*c+Bc2 где с-концентрация раствора ВМС ; M - молярная масса
ВМС ; B - коэффициент
учитывающий гибкость и форму молекулы в растворе.
Полиэлектролиты - это
мицеллярные и молекулярные
коллоидные электролиты
диссоциированные в растворах на макро- и микро- ионы.
Изоэлектрическая точка (ИЭТ) -
Характеристика состояния раствора
амфотерного электролита (амфолита
) -соед., способного присоединять
или отщеплять протоны,
превращаясь либо в положительно,
либо в отрицательно
заряженные ионы, - при котором суммарный электрический заряд амфолита равен нулю.
Онкотическим давлением плазмы
крови называется часть
осмотрического давления крови,
создаваемое растворенными в ней белками ВМС.
6. Мембранное равновесие Доннана.
2
5.
2
 Мембранным
равновесием
Мембранным
равновесием
Доннана называют равновесие, устанавливающееся в системе
растворов, разделенных
мембраной, непроницаемой хотя
бы для одного вида
присутствующих в системе ионов.
Низкомолекулярные ионы и
высокомолекулярные заряженные частицы,
распределяются неравномерно по обе стороны мембраны.Это
явление получило назв. эффекта
Гиббса-Доннана. Рассмотрим
6.
с1истему, состоящую из клетки ([R-
] [Na+j1) и наружного раствора
(межклеточной жидкости)
([Na+]II[Cl-]II). Внутри клетки
находится внутриклеточная
жидкость, содержащая только
соли бел-ка RNa с концентрацией
с1, где R - анион, имеющий
коллоидные размеры. Такой
анион не проходит через
мембрану - недиализуемый ион. Мембрана отделяет раствор RNa
от межклеточной жидкости, содержащей раствор NaCl с
концентрацией с2. Для ионов Na+
и С1- мембрана проницаема.
Пусть до начала опыта система
характеризуется распределением
ионов, которое соответствует
схеме:
где с1 и с2 - начальные
концентрация ионов внутри
клетки (слева от мембраны) и
снаружи (справа от мембраны).
Двойной чертой обозначена мембрана, а индексами I и II обозначены левый (I - внутри
клетки) и правый (II - между
клетками) растворы. Если
исходное соотношение
 концентраций
с1
<
с2,
то
в
концентраций
с1
<
с2,
то
в
соответствии с законами
диффузии внутрь клетки б+удут
переходить ионы С1- и Na .
Допустим, что перешло х моль
NaCl. Тогда при равновесии:
При равновесии
электрохимические потенциалы
каждого из общих ионов
растворов I и II
7. Устойчивость растворов
биополимеров. Высаливание, застудневание, коацервация.
Высаливание, как метод получения высокоэффективных лекарственных
веществ, используемых и стоматологии.
Факторы устойчивости растворов
полимеров. Растворы полимеров в
хорошо растворяющих их жидкостях
образуются самопроизвольно и
агрегативно устойчивы. Нарушить
устойчивость растворов полимеров
можно путем ухудшения их растворимости - введением
электролитов или нерастворителей
(жидкостей, плохо растворяющих данный полимер). Так, например,
для белков и полисахаридов
нерастворителями являются этанол, ацетон. Высаливание. Под влиянием
электролитов и нерастворителей
происходит процесс выделения ВМС
из раствора,
называемый высаливанием. Внешне такой процесс сходен с коагуляцией,
поскольку ВМС выделяется в виде
хлопьев, волокон, творожистых ос а д ков .
Однако если для коагуляции
2 Понятие об аэрозолях. Особенномти
7. их оптических, молекулярно
кинетических и электрических
свойств. Лечебное действие аэрозолей при заболеваниях полости рта.
Аэрозоли представляют собой
свободно-дисперсные системы с
газообразной дисперсионной средой и дисперсной фазой,
состоящей из твердых или
жидких частиц. Аэрозоли образуются при взрывах, дроблении и распылении
веществ, а также в процессах конденсации при охлаждении пересыщенных паров воды и органических жидкостей.
Аэрозоли можно получить и с
помощью химических реакций,
протекающих в газовой фазе.
По агрегатному состоянию частиц
аэрозоли классифицируют
на туманы (ж/г) - дисперсная
фаза состоит из капелек
жидкости, дымы (т/г) - аэрозоли с
твердыми частицами
конденсационного
происхождения, пыли (т/г) -
твердые частицы, образованные путем диспергирования.
 гидрофобных
золей
под
действием
гидрофобных
золей
под
действием
электролита требуются
незначительные количества
электролита и процесс коагуляции часто необратим, то на разрушение
водного раствора ВМС затрачивается большая
концентрация электролита и
наблюдается неподчинение правилу
Шульце-Гарди. Высаливание
является обратимымпроцессом -
разведение системы растворителем
приводит к восстановлению
истинного раствора. В основе
механизма высаливания ВМС лежит
процесс дегидратации. Ионы введенного электролита (или
молекулы «нерастворителя») как бы
«отнимают» большую часть
растворителя от макромолекул
полимера, делая их гидрофобными.
Поэтому высаливающее действие
ионов определяется их
способностью к гидратации.
Слабогидратирующиеся ионы могут
вообще не вызывать данного эффекта.
Концентрацию электролита, при
которой наступает быстрое
осаждение полимера,
называютпорогом
высаливания ВМС. Величина порога
высаливания измеряют уже не в
миллимолях (как при коагуляции) а в молях на литр.
Обычно более сильный
высаливающий эффект вызывают анионы, которые располагаются в
лиотропный ряд: SO42- > CH3COO- > Cl-
> NO3- > Вг- > I- > CNS-. Ряд для
катионов имеет вид Li+ > Na+ > К >
Rb+ > Cs+, что соответствует их способности к гидратируемости.
Возможны системы смешанного
типа, когда на твердых частицах
конденсируется влага. Так возникает «смог» - туман,
образовавшийся на частичках ды м а .
Электрические свойства
аэрозолей чрезвычайно сильно
отличаются от электрических
свойств систем с жидкой средой,
что объясняется резким различием плотностей и
диэлектрических свойств газов и
жидкостей. В газовой среде
отсутствуют электролитическая
диссоциация и ДЭС. Однако частицы в аэрозолях имеют
электрические заряды, которые
возникают при случайных
столкновениях частиц друг с
другом или с какой-нибудь поверхностью.
Аэрозоли обладают
способностью рассеивать свет. В них наблюдается конус Фарадея- Тиндаля. ИЗ-за большей разницы
в показателях преломления
дисперсной фазы и
дисперсионной среды
интенсивность светорассеяния у
аэрозолей больше чем у лиозолей.
Молекулярно-кинетические
свойства подчиняются
закономерностям лиозолей. Из-за
малой вязкости и плотности
газовой дисперсионной среды
интенсивность броуновского
движения, скорость диффузии и
седиментации значительно больше чем в лиозолях.
Аэрозоли нашли широкое
применение в медицине и
фармации. Стерильные аэрозоли
в специальных упаковках типа
баллонов применяют для
стерилизации операционного
 Высаливание
полиамфолитов
в
Высаливание
полиамфолитов
в
значительно мере зависит от рН
среды и облегчается вблизи их ИЭТ (см. §30.5).
Высаливание ВМС имеет большое
практическое значение. Его
применяют для фракционирования
белков, полисахаридов и других
веществ. Так, возможность
фракционирования обусловлено тем, что, применяя соли в разной концентрации, можно высаливать
различные фракции: при малой
концентрации выпадают наиболее
крупные и наименее заряженные частицы.
Коацервация. В концентрированных
растворах ВМС, особенно в
растворах белков, могут возникать
ассоциаты из молекул, которые
затем становятся зародышами новой
фазы. Выделение
новообразовавшейся фазы в виде
мельчайших капель
называют коацервацией. В
результате слияния отдельных
мелких капелек может произойти
расслоение на коацерват -
концентрированный раствор
полимера и разбавленный истинный
раствор. Предположительно при
коацервации происходит частичная дегидратация и слияние гидратных
оболочек молекул без их
непосредственного объединения,
поэтому внутри коацервата, где
концентрация молекул полимера
значительно выше, чем в
окружающем растворе, возникают
определенные контакты, как
следствие,
наблюдается самоорганизация с
образованием определенной
поля, ран и ожогов;
ингаляционные аэрозоли,
содержащие антибиотики и
другие лекарственные вещества,
- для лечения дыхательных путей; аэрозоли локального
применения используют вместо
перевязочных средств; аэрозоли
в виде клея - в хирургической практике для склеивания ран, кожи, бронхов, сосудов и т.д.
 структуры.
Процессу
коацервации
структуры.
Процессу
коацервации
способствует не только высокая
концентрация, но и факторы,
вызывающие самопроизвольную агрегацию: низкая температура, изменение рН среды, введение
низкомолекулярных электролитов и
«нерастворителей», воздействие
полей. Интересно, что
представления о коацерватах, как о зародышах простейших форм жизни
в мировом океане, легло в основу
теории А.И. Опарина (1922) о
происхождении жизни на Земле.
Практическая важность коацервации
возросла в связи с развитием
технологии микрокапсулирования. В ряде методов микрокапсулирования оболочка микрокапсул образуется из
адсорбированных капелек
коацервата полимера, которые сливаются в сплошную пленку и
специальной обработкой
переводятся в твердое состояние.
Застудневание в рез. огр. набухания
ВМС или частичного испарения растворителя из раствора ВМС
образуются студни. Таким образом студень можно рассматривать как
ограниченно набухший полимер или
концентрированный раствор полимера.
8. Реакции полимеризации,
лежащие и основе получения
стоматологических полимеров и
сополимеров (полиэтилена,
дивинилового каучука, полистирола и поливинилхлоридакрилатов).
??????????????????????????????????
?????????
2 Полимеры в стоматологии. Базисные
8. пластмассы на основе акриловой и
метакриловой кислот.
В стоматологии синтетические полимеры используют в качестве
пломбировочных материалов,
защитных покрытий, для
изготовления зубных протезов.
Стеклоиономерный цемент для
пломбирования зубов и трещин в
эмали. Он представляет собой
смесь полиакрилловой кислоты со стеклом специальных складов..
Частицы стекла, вплавлены в
полимерную матрицу, образуют композицию более прочную, чем портландцемент.
Постепенно в стоматологических
клиниках мира появляется новая группа полимерных материалов,
твердеющих без применения
химических инициаторов. В новых
композициях твердения
осуществляют фотохимические под
действием ультрафиолетового излучения кварцевой лампы.
Базисные пластмассы
изготавливаются на основе
акриловой и метакриловй кислот.
Ведущую роль акриловые
материалы заслужили своими главными свойствами: низкой
токсичностью, и удобством
переработки. Наилучшим способом
получения базисных пластмасс
является сополимеризация в
особенности привитая сополимеризация.
Базисные пластмассы различают холодного(быстротвердеющие) и горячего отверждения. В качестве материалов могут использоваться материалы типа гель, пластмассы
типа порошок-жидкость,
термопластичные литьевые
пластмассы. Однако в основном
выпускаются пластмассы типа порошок-жидкость.
Изготовление стом. конструкций из полимер-мономерных композиций горячего отверждения протекает по
 схеме:
полимер(порошок
сополимер
схеме:
полимер(порошок
сополимер
метилметакрилата с небольшим количеством этилметакрилта) + инициатор(перекись бензоила)+
мономер(жидкость
метилметакрилат, сшивающие
д об а в ки
этиленгликоль)+ингибитор(гидрохин
он)+нагрев=полимеризат+теплота полимеризации.
Основные представители: этакрил, акреол, фторакс, акронил.
9. Акриловая кислота, эфиры
акриловой и метакриловой
кислот, продукты их
полимеризации широко
используемые в
стоматологической практике.
Акриловая кислота:СН2=СН-СООН.
Эфиры: МЕТИЛАКРИЛАТ (метиловый
эфир акриловой к-ты)
СН2=СНСООСН3, мол. м. 86,09;
бесцв. подвижная жидкость с резким запахом; т. пл. < -75 °С, т. кип. 80,5 °С.
Прианяется для изтовления пластичных масс.
ЭТИЛАКРИЛАТ (этиловый эфир
акриловой к-ты) СН2 = СНСООС2Н
Метакриловая
кислота:CH2=C(CH3)COOH
Эфиры: МЕТИЛМЕТАКРИЛАТ -
CH2=C(CH3)-COOCH3, бесцветная
жидкость, tкип 101 .С. Применяется
главным образом для получения
оптически прозрачного полимера - полиметилметакрилата (см. также Стекло органическое).
2 Тетрафторэтилен как составная часть
9. фторопластов. Их применение в
стоматологии.
Тетрафторэтилен — химическое соединение углерода и фтора с
химической формулой C2F4, один из
представителей фторолефинов —
непредельных фторорганических соединений.
Тетрафторэтилен, CF2 = CF2, газ без
цвета и запаха, не растворяется в
воде, растворяется в органических
растворителях; tкип -76,3 °С. Обладает
всеми свойствами, характерными
для фторолефинов, легко
полимеризуется и сополимеризуется со многими мономерами, например
с винилиденфторидом, гексафторпропиленом,
трифторхлорэтиленом, этиленом.
Из тетрафторэтилена получают
политетрафторэтилен.Фторопласты
характеризуются широким
диапазоном механических свойств,
низким коэффициентом трения,
низкими значениями износа; стойки к действию различных агрессивных сред при комнатной и повышенной
 температуре,
атмосферо-
температуре,
атмосферо-
,коррозионно-
и радиационностойки, слабо газопроницаемы.
К базисным пластмассам
содержащим тетрафторэтилен
относят «Фторакс» -
фторсодержащий акриловый
сополимер, обладающий повышенной прочностью,
химической стойкостью, пластмасса полупрозрачна. Порошком фторакса
является привитой сополимер
метилметакрилата к фторкаучуку и фтористого винилдена, полученный
суспензионным методом в
соотношении 1:2. Жидкость -
метилметакрилат, содержащий
сшивагент диметакриловый эфир
дифенилолпропана. Фторакс,
используемая при изготовлении
базисов, как полных протезов
верхней и нижней челюстей, так и частичных протезов.
1 Акриловая, итаконовая, 3
0. малеиновая кислоты, как 0.
составляющее компоненты
стеклоиономерных цементов.
Жидкость стеклоиономерного
цемента обычно представляет собой 47,5% (40-55%) водный раствор сополимера акриловой и итаконовой или акриловой и малеиновой кислот. Вода при этом является не только растворителем, а необходимым компонентом цемента, играющим важную роль в процессе его отверждения. Она является средой, в которой происходит ионообмен.
ch 2
Акриловая: ch2=ch-cooh Итакон.:
hooc-ch2-c-cooh
Малеиновая: hooc-ch=ch-cooh
Для полимеризации в качестве
органической составляющей
используются именно эти три ненасыщенные кислоты акриловая, итаконовая, малеиновая. Полимеры этих кислот содержат максимальное количество карбоксильных групп, за
 счет
которых
происходит
сшивка
счет
которых
происходит
сшивка
цепочек полимера и адгезия к
твердым тканям зуба.
Полиитаконовая и полималеиновая кислоты содержат в 2 раза больше
карбоксильных групп, чем
полиакриловая. Итаконовая кислота снижает вязкость жидкости и ингибирует загустевание вследствие межмол окулярных водородных связей. Добавление 5 % оптически активного изомера винной кислоты значительно увеличивает время обработки и способствует быстрому схватыванию материала, ускоряя экстракцию ионов из стеклянных частиц. Механизм действия винной кислоты заключается в — том, что
он а является сильным
комплексообразователем, временно извлекает в течение первого периода отверждения цемента ионы
металла из межмолекулярных
связей, Такая реакция обратима и на последних стадиях ионы металла
с н ов а способны создавать
поперечные связи.
С химической точки зрения затвердевание стекло и оном ерного цемента обусловлено образованием сложной совмещенной матрицы,
состоящей из силикатной и
полиакрилатной матриц. Поскольку различные ионы выделяются из
стекла неравномерно, процесс
застывания осуществляется поэтапно.
Отвердение цемента проходит в
три последовательные стадии:
1. Растворение или гидратация
компонентов, сопровождающаяся
выделением
(выщелачиванием),ионов.
2. Загустевание (или первичное
гелеобразованне, начальное, нестабильное отвердевание).
3. Отвердевание (или дегидратация,
созревание, окончательное
отвердевание).
1 Механизм радикальной 3
полимеризации.
 1.
РАДИКАЛЬНАЯ
ПОЛИМЕРИЗАЦИЯ,
п
1.
1.
РАДИКАЛЬНАЯ
ПОЛИМЕРИЗАЦИЯ,
п
1.
олимеризация, в к-рой активные
центры роста представляют собой своб. радикалы.
Радикальнаяполимеризация возмож
на для большинства виниловых,
винилиденовых, диеновых
мономеров, а также для нек-рых
напряженных циклич. соединений.
Нек-рые ненасыщ. мономеры не способны полимеризоваться по
радикальному механизму
вследствие стерич. затруднений
(напр., 1,2-дизаме-
щенные виниловые мономеры) или
в случае вырожденной передачи
цепи (см. ниже),
напр. пропилен, аллильныемономер ы.
Радикальная полимеризация-один
из осн. пром. методов, к-рым
получают более половины
производимых в мире полимеров, в т.
ч.полиэтилен (высокого давления), п
олистирол, сополимеры этилена и стирола с разл.
полярными мономерами, поливинил хлорид,полиакрилаты и полиметакр
илаты, ряд синтетич. каучуков и
водорастворимых
карбоцепных полиэлектролитов.
Кинетич. схема
радикальной полимеризации включ
ает четыре элементарные
стадии: инициирование, рост,
передачу и обрыв цепи. На
стадии инициирования образуются
первичные радикалы мономера в
результате непосредств. энергетич.
воздействия (тепло, УФ
либоионизирующее излучение; о
двух последних
 см.
Фотополимеризация,
Радиацион
см.
Фотополимеризация,
Радиацион
ная полимеризация)или чаще при взаимод. мономера с радикалами, возникающими при гомолитич.
распаде специально вводимых в-в-
инициаторов радикальных
(напр., пероксидов,
гидропероксидов, азосоединений).
Для увеличения
скорости инициирования при низких
т-рах
к пероксидам добавляют восстанови
тели, напр. соли переходных
металлов или амины (т. наз. окис- лит.-восстановит. инициаторы).
Стадия инициирования включает по
меньшей мере два последоват.
элементарных акта - генерирование
радикалов R• (р-ция 1, а) и их
взаимод. с мономером (р-ция 1, б):
(I-инициатор, М-мономер, М•1-
первичный мономерный радикал,
k1 и k'1 - константы
скоростей соответствующих р-ций).
Осн. стадия полимеризации-р-ция
роста цепи, при многократном
повторении к-рой образуется
макромол. цепь, - описывается ур-
нием:
Передача цепи -р-ция, приводящая к
переносу активного центра от
растущего макрорадикала на любую
др. молекулу (р-ритель,мономер,
инициатор, полимер), выступающую
в роли агента передачи (А), с
образованием
"мертвой" макромолекулы (Мn) и
 новогоактивного
центра
(А•):
новогоактивного
центра
(А•):
(k4 - константа скорости передачи
цепи). Обычно р-ция передачи цепи
приводит к продолжению кинетич.
цепи, поскольку новый радикал
А• способен инициировать
радикальную полимеризацию со
скоростью, близкой к скорости р-ции роста.
1 Сополимеризация винилхлорида и
2. 1,3-бутадиена, метакрилата и 2-
ацетокси- 1,3-бутадиена,
приводящая к синтезу
стоматологических полимеров.
??????????????????????????????
1 Фенол и формальдегид - основа для
3. синтеза фенолформальдегидной
смолы. Производные фенола
(бисфенолы) - составная часть пломбировочных сополимеров.
Гидрохинон как ингибитор процесса
сополимеризации базисных пластмасс.
3
2.
3 Облицовочные полимеры для 3. несъемных протезов.
 Фенолформальдегидная
смола
-
Фенолформальдегидная
смола
-
вещество получаемое при
нагревании смеси формальдегида
(формалина) и фенола. Впервые такая химическая реакция была
проведена немецким учёным Адольфом Байером в 1872 г. В
процессе химического
взаимодействия формальдегида и фенола образовывался полимер и
молекула воды
Формальдегид: ch2o фенол: c6h5oh
Выпускаемые в 80-х годах эпоксидные преполимеры
представляли собой продукты
сочетания эпихлор-гидрина (ЭХГ) с
бисфенолом А (ДФП)
Гидрохинон:
Входит в состав жидкости базисных пластмасс как ингибитор процесса
сополимеризации при
транспортировке мономерной жидкости.
В качестве облицовочных
материалов используют акриловые
полимеры. Для облицовки
металлических каркасов несъемных
протезов используют пластмассу Синма-М (акриловая пластмасса
горячего отверждения в виде
порошка и жидкости). Порошок -
суспензионный сопривитой
фторсодержащий сополимер, жидкость - смесь акриловых
мономеров и олигомеров. Наличие
олигомеров увеличивает время
жизнеспособности массы в
пластичном состоянии (до 30 мин).
Пластмассу можно использовать для облицовки протезов след.методами:
моделированием облицовки непосредственно на каркасе
протеза; паковкой пластмассы в форму. В комплект пластмассы
входят порошки «Дентин» и
«Эмаль». «Дентин» и жидкость - 3:1(объемное) или 2:1(весовое).
Оставляют для набухания в течение 6 мин в закрытом сосуде(в процессе перемешивают 1-2 раза). Наносят на
каркас небол.порциями, придавая облицовке форму нужного зуба.
Толщина слоя не превышает 3 мм,
т.к.если больше то трещины. В
пневмополимеризаторе
стоматологическом Синма-М
полимеризуется в течение 10 мин
при темп-ре 120 и давлении 4-5 атм.
2 полимеризация для коррекции проводится при темп-ре 100 для
предотвращения образования щели между Ме и пластмассой.
 1
Альдегиды
как
аппреты
для
1
Альдегиды
как
аппреты
для
4. улучшения качества полимеров.
реакции окисления, полимеризации,
альдольной конденсации
альдегидов. Получение фенол- формальдегидной смолы.
??????????
3 Химический состав
4. стоматологических цементов.
Цемент — порошкообразное
вяжущее, как правило, минеральное
вещество, способное при
замешивании с водой образовывать
пластичную массу. После затвердевания становится камнеобразным.
Цинк-фосфатные цементы
выпускаются в виде порошка и жидкости.
Порошок состоит в основном из
оксида цинка с добавлением 10%
оксида магния и небольшого
количества пигмента. Его прокаливают при высокой
температуре (>1000° С), чтобы
снизить реакционную способность.
Жидкость представляет собой
водный раствор ортофосфорной
кислоты, содержащий от 30 до 55% воды. В жидкость входят также 2-3%
солей алюминия и 0-9% солей
цинка. Алюминий необходим для реакции образования цемента, а
цинк является замедлителем реакции между порошком и
жидкостью, что обеспечивает
достаточное время для работы.
Образовавшийся аморфный фосфат
цинка связывает вместе
непрореагировавший оксид цинка и другие компоненты цемента.
Цинк-силикатнофосфатные цементы:
Цементный порошок представляет собой смесь, состоящую из 10-20% оксида цинка и силикатного стекла,
смешанных механическим способом
или сплавленных и повторно
измельченных.
Силикатное стекло содержит 12-25%
фторидов. Некоторые материалы
считают «бактерицидными», так как
в них присутствуют в небольших
количествах соединения серебра.
Жидкость содержит от 2 до 5% солей алюминия и цинка в водном 45-50% растворе ортофосфорной кислоты.
Затвердевший цемент состоит из
непрореагировавших частиц стекла
и оксида цинка, связанных вместе
матрицей из алюмосиликат- фосфатного геля.
Цинк-поликарбоксилатные цементы:
Порошок представляет собой оксид
цинка, в некоторых случаях с
содержанием от 1 до 5% оксида
магния. В цементах некоторых
марок может присутствовать от 10
до 40% оксида алюминия или
другого упрочняющего наполнителя.
Для улучшения механических
свойств и в качестве
выщелачиваемого фтористого
соединения в состав цемента может
быть включено также несколько
процентов фторида олова или другого фторида.
Жидкость представляет 40% водный раствор полиакриловой кислоты или
сополимера акриловой кислоты с
другими органическими кислотами, например итаконовой.
Молекулярный вес полимера
обычно составляет от 30 до 50 тыс., чем и объясняется вязкий характер раствора.
Порошок акриловых цементов
представляет собой тонко
измельченный полимер
метилметакрилата или сополимер, содержащий перекись бензоила в
качестве инициатора. В состав
порошка могут входить также минеральный наполнитель и пигменты.
Жидкость состоит из мономера
метилметакрилата, содержащего
аминный ускоритель. Мономер размягчает частицы полимера и
одновременно полимеризуется под воздействием свободных радикалов,
образующихся при взаимодействии
перекиси бензоила и аминного
ускорителя. Затвердевшая масса
состоит из новой полимерной
матрицы, объединяющей
нерастворенные, но набухшие гранулы первичного полимера.
Жидкость добавляется в порошок
при минимальном перемешивании
шпателем с целью избежания
попадания воздуха. Смесь должна
быть использована сразу, так как рабочее время очень короткое.
Диметакрилатные цементы
разработаны на основе
диметакрилатов и представляют собой сочетание ароматического
диметакрилата с другими
мономерами. Поставляются в виде
двух вязких жидкостей, двух паст или в виде порошка и жидкости.
Диметакрилатный цемент применяется для фиксации
предварительно протравленных
цельнолитых протезов и ортодонтических дуг.
В порошок диметакрилатного
цемента входит тонко измельченное
боросиликатное или кварцевое
стекло, содержащее органическую
перекись бензоила в качестве
инициатора. При смешивании с
жидкостью происходит полимеризация смеси с
образованием структуры
композиционной пластмассы с
большим количеством поперечных связей. Жидкость состоит из смеси
ароматического диметакрилата,
разбавленной
алкилдиметакрилатом с низкой
вязкостью. В качестве катализатора
используется амин. Некоторые
диметакрилатные цементы
содержат фосфатный мономер для улучшения адгезии.
Материалы, состоящие из двух паст
содержат смесь диметакрилата и других мономеров с различными
количествами наполнителя в
зависимости от марки, а также инициаторы химического или
светового отверждения, подобные
тем, которые применяются в
композиционных пломбировочных материалах.
Порошок в стеклоиономерных
цементах состоит из тонко
измельченного стекла (фторсиликата
кальция и алюминия) с размером
частиц около 40 мкм для
пломбировочных материалов и менее 25 мкм для фиксации. Содержание фтора в порошке
составляет от 10% до 16% от веса.
Для увеличения прочности в цемент
Кетак-Сильвер (Германия),
например, введен порошок серебра. Жидкость представляет собой смесь
50% водного раствора сополимера полиакрил-итаконовой или другой
поликарбоновой кислоты и 5%
винную кислоту. В некоторых
материалах сополимер добавляется
к порошку, а раствор содержит
только винную кислоту; в других все ингредиенты содержатся в порошке,
а жидкость представляет собой
 дистиллированную
воду.
При
дистиллированную
воду.
При
замешивании полиакриловая и
винная кислоты взаимодействуют со стеклом, реагируя с ионами кальция
и алюминия, которые, образуя поперечные связи, превращают
поликислотные молекулы в гель. Винная кислота служит для того, чтобы увеличить рабочее время.
Цинкоксидэвгеноловый цемент (без
наполнителя) — простая
комбинация оксида цинка и
эвгенола — включает порошок и жидкость.
Порошок представляет собой
фактически чистый оксид цинка, не
содержащий мышьяка. Возможно
присутствие в небольших
количествах наполнителей, например кремнезема. Для
ускорения твердения возможно
присутствие примерно 1% ацетата или сульфата цинка.
Жидкость состоит из очищенного эвгенола или гвоздичного масла
(85% эвгенола). Возможно
присутствие спирта или уксусной
кислоты (не выше 1%) для ускорения
схватывания, а также небольших
количеств воды для реакции
твердения. Между оксидом цинка и
эвгенолом в присутствии воды
происходит химическая реакция с образованием эвгенолята цинка.
1 Синтез полипептидов, белков.
5. Аминокислоты - как структурные
компоненты. Строение пептидной связи.
Короткие белки могут быть
синтезированы химическим путём с помощью группы методов, которые используют органический синтез —
например, химическое
лигирование[20]. Большинство
3 Стоматологические герметики и
5. адгезивы.
 методов
химического
синтеза
методов
химического
синтеза
проходят в направлении от C-конца к
N-концу, в противоположность
биосинтезу. Таким образом можно
синтезировать
короткий иммунногенный пептид (эпитоп), служащий для получения
антител путём инъекции в животных,
или получения гибридо́м; химический синтез также
используется для получения
ингибиторов некоторых
ферментов[21]. Химический синтез
позволяет вводить искусственные, то
есть не встречающиеся в обычных
белках аминокислоты — например,
присоединятьфлюоресцентные
метки к боковым цепям
аминокислот. Однако химические
методы синтеза неэффективны при
длине белков более 300
аминокислот; кроме того,
искусственные белки могут иметь
неправильную третичную структуру,
и у аминокислот искусственных
белков отсутствуют
посттрансляционные модификации.
Белки синтезируются живыми организмами из аминокислот на
основе информации,
закодированной в генах. Каждый
белок состоит из уникальной
последовательности аминокислот,
которая определяется нуклеотидной
последовательностью гена,
кодирующего данный
белок. Генетический
код составляется из трёхбуквенных
«слов», называемых кодонами;
каждый кодон отвечает за
присоединение к белку одной
аминокислоты: например, сочетание АУГ соответствует метионину.
Поскольку ДНК состоит из четырёх
 типов
нуклеотидов,
то
общее
число
типов
нуклеотидов,
то
общее
число
возможных кодонов равно 64; а так
как в белках используется 20
аминокислот, то многие
аминокислоты определяются более
чем одним кодоном. Гены,
кодирующие белки,
сначала транскрибируются в
последовательность нуклеотидов
матричной РНК (мРНК) белками РНК- полимеразами.
Аминокислоты да ну их в
опу!(Аффтор жжёт)
Пептидная связь
Пептидная (амидная) связь — это
вид химической связи, которая
возникает вследствие
взаимодействия -аминогруппы
одной аминокислоты и -
карбоксигруппы другой
аминокислоты. Амидная связь
очень прочная, и в нормальных
клеточных условиях (37 °C,
нейтральный ph)
самопроизвольно не
разрывается. Пептидная связь
разрушается при действии на неё
специальных протеолитических
ферментов (протеаз, пептидгидролаз).
 1
Синтез
нуклеозидов,
как
пример
1
Синтез
нуклеозидов,
как
пример
6. реакции поликонденсации.
Я думаю всё, что нужно в этом
вопросе это вот такая картинка) Т.К.
вопрос практический, вроде..)
Всякие штуки соединяются с
выделением водыВот вам и
поликонденсация..)
3
6.
1 Олигосахариды. Дисахариды: 3 37.Химические реакции, лежащие в
7. мальтоза, лактоза, целлобиоза, 7. основе получения полимерных
сахароза. быстротвердеющих материалов
для реставрации съемных протезов
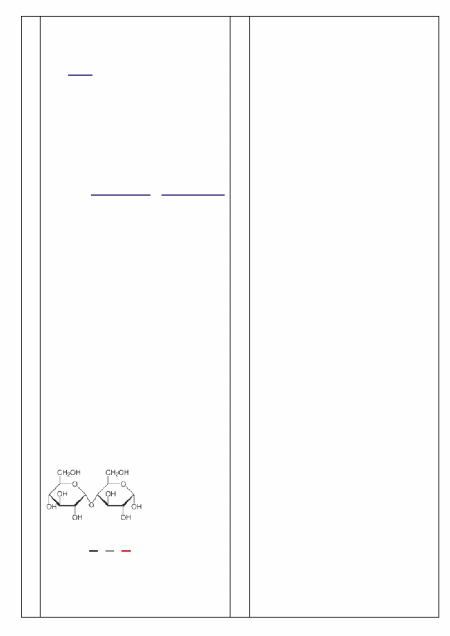 Олигосахариды
представляют
собой
Олигосахариды
представляют
собой
углеводы, состоящие из
нескольких моносахаридных остатко
в (от греч. ὀί — немногий).
Олигосахариды, состоящие из
одинаковых моносахаридных
остатков, называют
гомополисахаридами, а из разных — гетерополисахаридами.
Наиболее распространёнными из
олигосахаридов
являются дисахариды и трисахариды
. По химической природе
дисахариды — это О-
гликозиды (ацетали), в которых вторая молекула моносахарида
выполняет роль агликона. В
зависимости от строения
дисахариды делятся на две группы:
восстанавливающие и
невосстанавливающие.
Мальтоза (от англ. malt —
солод) — солодовый сахар, 4-О-
-D-глюкопиранозил-D-глюкоза,
природный дисахарид, состоящий
из двух остатков глюкозы;
содержится в больших
количествах в проросших зёрнах
(солоде) ячменя, ржи и других
зерновых; обнаружен также
в томатах, в пыльце
и нектаре ряда растений
Одной из таких реакций является
реакция полимеризации.
Полимеризационным называют
процесс , при котором
макромолекулы образуются путем последовательного присоединения одного или нескольких мономеров
к растущему активному центру. В
стомат. практике наиболее
распространен радикальный способ инициирования полимеризации.
Такие реакция называется цепной и
состоит их трех последовательных
стадий: инициирования, роста и обрыва цепи.
Инициирование- это превращение
большой доли мономера в
активные частицы способные
присоединять к себе новые молекулы мономера.
реакция присоединения: полная полимеризация, не содержащая побочных продуктов.
реакция поликонденсации:
реакция синтеза полимера. При котором происходит хим.
взаимодействие с выделением
побочных низкомолекулярных в-в.
Лактоза (от лат. lactis —
молоко) C12H22O11 —
углевод группы дисахаридов,
содержится в молоке и молочных
продуктах. Молекула лактозы
состоит из остатков
молекул глюкозы и галактозы.
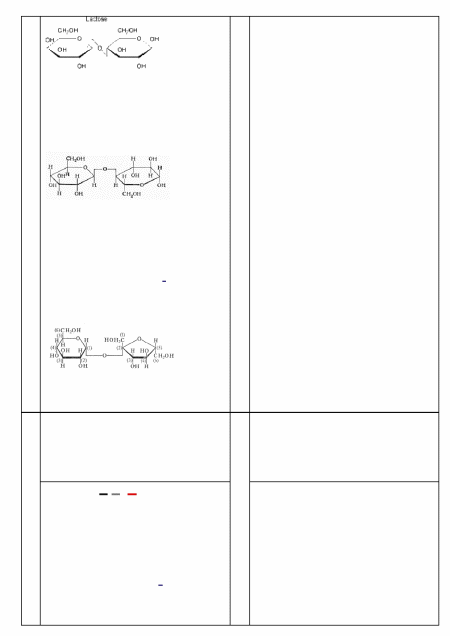 Целлобиоза
—
4-(-глюкозидо)-
Целлобиоза
—
4-(-глюкозидо)-
глюкоза, дисахаридов, состоящий
из двух остатков глюкозы,
соединённых -глюкозидной
связью; основная структурная единица целлюлозы.
Сахароза C12H22O11,
или свекловичный
сахар, тростниковый сахар, в
быту просто сахар —
дисахарид из
группыолигосахаридов,
состоящий из
двух моносахаридов — - глюкозы и -фруктозы.
1 Гомополисахариды: крахмал,
8. гликоген, целлюлоза. Первичная
структура, гидролиз. Амилоза,
амилопектин. Понятие о гетерополисахаридах.
(C6H10O5)n —
полисахариды амилозы и амилоп
ектина, мономером которых является альфа-глюкоза. Крахмал, синтезируемый
разными растениями в
хлоропластах, под
действием света при фотосинтез
е, несколько различается по
структуре зёрен, степени полимеризации молекул,
3
8.
38.Современные базисные
материалы, применяемые в стоматологии. Альгинатные слепочные материалы.
Альгинатные оттискные материалы.
Базисными называются материалы,
применяемые для изготовления базисов съемных пластиночных протезов. На сегодняшний день
существует широкий выбор
базисных материалов, Один из вариантов: нейлоновые гибкие
протезы «Валпласт». Нейлоновые
протезы отличаются высокой
эстетичностью. Они изготовлены из
 строению
полимерных
цепей
и
строению
полимерных
цепей
и
физико-химическим свойствам.
Целлюлоза (фр. cellulose от лат.
полупрозрачного материала
естественного цвета десны, а для их
фиксации используются кламера,
незаметные для глаза. Протезы
суперэластичны и отличаются
повышенной прочностью, поэтому
они не сломаются не только в
повседневной жизни, при обычной эксплуатации, но и в экстремальных
ситуациях. Изготовление протезов
происходит таким образом, что они
имеют точную посадку и
cellula — «[1к]летка, клетушка») —
(C6H10O5)n , белое твердое
вещество, нерастворимое в воде,
молекула имеет линейное
(полимерное) строение,
структурная единица — остаток
-глюкозы
[С6Н7О2(OH)3]n. Полисахарид,
главная составная
часть клеточных
оболочек всех высших растений.
Гликоген —
(C6H10O5)n, полисахарид,
образованный
остатками глюкозы; основной запасной углеводчеловека и
животных. Гликоген (также иногда
называемый
животным крахмалом, несмотря
на неточность этого термина)
является основной формой
хранения глюкозы в животных
клетках. Откладывается в виде гранул в цитоплазме во многих
типах клеток (главным
образом печени и мышц).
Гликоген образует
энергетический резерв, который может быть быстро мобилизован
при необходимости восполнить внезапный недостаток глюкозы.
стабильную фиксацию. Материал
обладает великолепной точностью и однородностью.
Эти протезы не вызывают
аллергической реакции у
пациентов, чувствительных к
акрилу, винилу, латексу и
металлам. Это еще одно очень
важное достоинство нейлоновых протезов.
Материал на основе полиуретана «ДЕНТАЛУР».
Протезы из безмономерного
материала на основе полиуретана
сочетают в себе преимущества акриловых и гибких протезов.
Преимущества перед
стандартными (акриловыми)
протезами: нетоксичность,
гипоаллергенность, эластичность,
высокая прочность, отсутствие запаха и отсутствие усадки при
полимеризации
Такие протезы имеют
преимущества и перед гибкими
протезами: допустимость починки, приварки зубов при перебазировке,
простота полировки, надежность крепления искусственных зубов,
меньшая стоимость Материал
 абсолютно
негигроскопичен
(не
абсолютно
негигроскопичен
(не
впитывает влагу с флорой полости
рта) поэтому в нем не живут
микроорганизмы
Альгинатные слепочные
В желудочном тракте человека и
животного крахмал
поддаётся гидролизу и
превращается в глюкозу, которая усваивается организмом.
Промежуточными продуктами
гидролиза крахмала
являются декстрины. В
промышленности превращение
крахмала в глюкозу (процесс
осахаривания) происходит путём
кипячения его на протяжении
нескольких часов с разбавленной серной кислотой (каталитическое
влияние серной кислоты на
осахаривание крахмала было
обнаружено
в 1811 г. К. С. Кирхгофом). Чтобы
из полученного раствора
удалитьсерную кислоту в него
добавляют мел, получая из
серной кислоты
нерастворимый сульфат кальция.
Последний отфильтровывают, и вещество выпаривают.
Получается густая сладкая
масса — крахмальная патока,
которая содержит кроме глюкозы
значительное количество
остальных продуктов гидролиза крахмала.
материалы
льгинатные слепочные материалы легки в работе.
Альгинаты позволяют получить
достаточно точные гипсовые модели.
Данные модели могут применяться
ка к:
Документальные модели,
показывающие состояние прикуса
до, во время и после ортодонтического и
ортопедического лечения.
Диагностические модели, на которых можно более точно
поставить диагноз и определить план лечения..
Вспомогательные, окклюзионные
модели антогонистов при изготовлении различных
ортопедических конструкций.
Рабочие модели при изготовлении штампованно-паяных конструкций,
съемных пластиночных протезов,
ортодонтических аппаратов,
индивидуальных слепочных ложек.
Альгинатный оттискной материал
В настоящее время в
ортопедической стоматологии для снятия оттисков при изготовлении
зубных протезов широко
используются альгитные оттискные
материалы. Уникальным
природным сырьем для их
производства являются бурые
морские водоросли. Натриевая соль альгиновой кислоты и соли
поливалентных металлов (Са)
составляют основу всех
 альгинатных
оттискных
альгинатных
оттискных
материалов.
Альгинатные оттискные материалы серии «Белопринт»: «Белопринт» и
«Белопринт Хроматик» - это
сложная композиция на основе
альгинатов с различной
молекулярной массой, что позволяет получать оттиски
высокой степени прочности и
эластичности, точно передающие рельеф мягких и твердых тканей
полости рта. Порошок «Белопринт»
в процессе дозировки и
замешивания не образует «пыли»,
быстро смешивается с водой, что
обеспечивает стоматологу удобную работу с материалом.
В состав порошка входят
нетоксичные, биосовместимые
материалы. Он не содержит
консервантов и дезинфектантов,
поэтому безопасен как для
пациентов, так и для стоматологов,
не оказывает раздражающего
воздействия на ткани полости рта.
Св-ва альгинатов: вязкость, точность
передачи деталей, стабильность
размеров, эластичность
1
9.
3 Современные силиконовые
9. материалы, применяемые в
стоматологии.
В настоящее время широко
распространены такие силиконы, как: А-силиконы и К-силиконы. К-силиконы. В их основе лежит
реакция поликонденсации: реакция
синтеза полимера. При котором
происходит хим. взаимодействие с
выделением побочных
низкомолекулярных в-в.
 Представители:
«Стомафлекс»,
Представители:
«Стомафлекс»,
«Ксантопрен»
Св-ва: очень точное
вопроизведение мелких деталей,
размерная стабильность,
механически прочны, гидрофобны,
нейтральны по вкусу и запаху,
Хорошая адгезия к оттискной ложке
и отличная - между слоями
А-силиконы. В их основе лежит
реакция присоединения: полная полимеризация, не содержащая побочных продуктов.
Представители: « 3 М Экспресс»,
«Экзафлекс»
Св-ва: точное воспроизведение
мелких деталей, размерная
стабильность, механически прочны,
гидрофильны, тиксотропны,
Отличное послойное соединение,
Не имеют вкуса и запаха,
Оптимальная совместимость с кожей и слизистой оболочкой.
2
0.
4 Биополимеры, используемые для
0. профилактики и лечения болезней
полости рта. Антимикробные и противовирусные препараты.
Эффективность стоматологической
помощи во многом зависит от
качества применяемых
материалов, в том числе и
биополимерных. В стоматологии
синтетические биополимеры
используют в качестве
пломбировочных материалов,
защитных покрытий, для
изготовления зубных протезов. Достаточно распространен так
называемый стеклоиономерный
цемент для пломбирования
передних зубов и трещин в эмали.
Он представляет собой смесь полиакрилловой кислоты со
стеклом специальных складов,
изготовленным из измельченной
смеси кварца, глинозема, криолита,
плавикового шпата и фосфата аммония или из смеси кварца,
глинозема и карбоната кальция.
Частицы стекла, вплавлены в
полимерную матрицу, образуют
композицию более прочную, чем портландцемент.
Постепенно в стоматологических клиниках мира появляется новая
группа биополимерных
материалов, твердеющих без
применения химических
инициаторов, которые часто не
соответствуют токсикологическим
требованиям. В новых композициях
твердения осуществляют
фотохимические под действием
ультрафиолетового излучения
кварцевой лампы
Антибактериальные препараты. Их
применение в практике
стоматолога обусловлено
безусловной важностью инфекции
как фактора, принимающего участие в развитии основных
стоматологических заболеваний.
В настоящее время
антибактериальную терапию
используют для профилактики
кариеса, профилактики и лечения заболеваний пародонта, слизистой
оболочки рта (СОР), для
предотвращения осложнений,
возникающих при лечении
деструктивных форм периодонтита,
развития транзиторной
бактериемии при хирургических
манипуляциях, как компонент
деконтаминационных мероприятий.
Препараты для антибактериальной
терапии должны отвечать ряду
 требований:
требований:
