
- •Билет №20 «Волновая функция.Уравнение Шредингера.Стационарное состояние»
- •Билет№21 «Частица в одномерной прямоугольной потенциальной яме.Прохождение частицы через потенциальный барьер»
- •Билет№22 «Атом водорода.Потенциалы возбуждения и ионизации.Квантовые числа.Вырожденные состояния»
- •Билет №23 «Ширина спектральных линий.Мультиплетность спектров.Спин электрона.Магнетон Бора»
- •Билет №24 «Спин орбитальное взаимодействие.Эффект Зеемана.Принцип Паули.Расположение элементов в системе Меделеева»
- •Билет №25 «Ионная и ковалентная связи атомов в молекуле.Энергия диссоциации.Полная энергия молекулы.Вращательные ,колебательно-вращательные полосы»
- •Билет №7 «Дифракция от круглого сечения,круглого диска ,щели»
- •Билет №26 «Вынужденное излучение .Мазеры. Лазеры. Накачка метастабильных уровней. Свойства лазерного излучения»
- •1. Лазерное излучение когерентно и практически монохроматично. 2. Лазерное излучение большой мощности имеет огромную температуру.
- •Билет №27 «Фазовое пространство.Функция распределения.Понятие о квантовой статистике Бозе-Эйнштейна и Ферми-Дирика»
- •Билет №28 «Колебания кристаллической решетки.Теория Дебая теплоемкости кристаллов.Энергия нулевых колебаний.»
- •Билет №29 «Квантовая теория свободных электронов в металле.Уровень Ферми.Запрещенные зоны.Валентная зона.Зона проводимости»
- •Билет №3 «Фотометрические величины.Интенсивность,световой поток,поверхностная яркость,освещенность»
- •Билет №4 «Принцип Гюйгенса.Когерентные волны.Интерференция света.Оптическая разность хода»
- •Билет №5 «Полосы равного наклона и равной толщины.Кольца Ньютона.Инерферометры Майкельсона и Фабри-Перо»
- •Билет №6 «Дифракция Фраунгофера и дифракция Френеля.Принцип Гюйгенса-Френеля.Зоны Френеля»
- •Билет №7 «Дифракция от круглого сечения,круглого диска ,щели»
- •Билет №7 «Дифракция от круглого сечения,круглого диска ,щели»
- •Билет №40 «Реакция деления ядра.Цепная реакция деления»
- •Билет №30 «Электропроводность металлов.Сверхпроводимсоть.Температурные зависимости проводимости»
- •Билет №31 «Дырочня проводимость.ПРимесная проводимость.Зпрещенные зоны.Валентная зона.Зона проводимости»
- •Билет №32 «Работа выхода.Термоэлектронная эмиссия.Контактная разность потенциалов»
- •Билет №33 «Контактные явления в полупроводниках»
- •Билет №34 «Термоэлектрические явления»
- •1. Явление Зеебека. В замкнутой цепи, состоящей из последовательно соединенных разнородных проводников, контакты между которыми имеют различную температуру, возникает электрический ток.
- •Билет №35 «Основные свойства атомного ядра»
- •Билет №36 «Масса и энергия связи.Дефект массы.Деление тяжелых и синтез легких ядер»
- •Билет №37 «Ядерные силы.Модели ядра.Мезоны»
- •Билет №38 «Радиоактивность.Постоянная распада.Альфа,бета и гамма-излучения»
Билет №24 «Спин орбитальное взаимодействие.Эффект Зеемана.Принцип Паули.Расположение элементов в системе Меделеева»
Спин-орбитальное взаимодействие — в квантовой физике взаимодействие между движущейся частицей и её собственным магнитным моментом, известным как спин. Наиболее часто встречающимся примером такого взаимодействия является взаимодействие электрона, находящегося на одной из орбит в атоме, с собственным спином. Такое взаимодействие, в частности, приводит к возникновению так называемой тонкой структуры энергетического спектра электрона и расщеплению спектроскопических линий атома.
Если тождественные частицы имеют одинаковые квантовые числа, то их волновая функция симметрична относительно перестановки частиц. Отсюда следует, что два одинаковых фермиона, входящих в одну систему, не могут находиться в одинаковых состояниях, так как для фермионов волновая функция должна быть антисимметричной. Обобщая опытные данные, В. Паули сформулировал принцип, согласно которому системы фермионов встречаются в природе только в состояниях, описываемых антисимметричными волновыми функциями (квантово-механическая формулировка принципа Паули).
Д. И. Менделеев ввел понятие порядкового номера Z химического элемента, равного числу протонов в ядре и соответственно общему числу электронов в электронной оболочке атома. Расположив химические элементы по мере возрастания порядковых номеров, он получил периодичность в изменении химических свойств элементов. Однако для известных в то время 64 химических элементов некоторые клетки таблицы оказались незаполненными, так как соответствующие им элементы (например, Ga, Se, Ос) тогда еще не были известны. Д. И. Менделеев, таким образом, не только правильно расположил известные элементы, но и предсказал существование новых, еще не открытых элементов и их основные свойства. Кроме того, Д. И. Менделееву удалось уточнить атомные веса некоторых элементов. Например, атомные веса Be и U, вычисленные на основе таблицы Менделеева, оказались правильными, а полученные ранее экспериментально — ошибочными.
Билет №25 «Ионная и ковалентная связи атомов в молекуле.Энергия диссоциации.Полная энергия молекулы.Вращательные ,колебательно-вращательные полосы»
Молекула — наименьшая частица вещества, состоящая из одинаковых или различных атомов, соединенных между собой химическими связями, и являющаяся носителем его основных химических и физических свойств. Химические связи обусловлены взаимодействием внешних, валентных электронов атомов. Наиболее часто в молекулах встречается два типа связи: ионная и ковалентная
Ионная связь (например, в молекулах NaCl, KBr) осуществляется электростатическим взаимодействием атомов при переходе электрона одного атома к другому, т. е. при образовании положительного и отрицательного ионов. Ковалентная связь (например, в молекулах H2, С2, СО) осуществляется при обобществлении валентных электронов двумя соседними атомами (спины валентных электронов должны быть антипараллельны). Ковалентная связь объясняется на основе принципа неразличимости тождественных частиц (см. § 226), например электронов в молекуле водорода. Неразличимость частиц приводит к специфическому взаимодействию между ними, называемому обменным взаимодействием. Это чисто квантовый эффект, не имеющий классического объяснения, но его можно себе представить так, что электрон каждого из атомов молекулы водорода проводит некоторое время у ядра другого атома и, следовательно, осуществляется связь обоих атомов, образующих молекулу. При сближении двух водородных атомов до расстояний порядка боровского радиуса возникает их взаимное притяжение и образуется устойчивая молекула водорода.
Энергия изолированной молекулы
![]()
где Еэл — энергия движения электронов относительно ядер, Екол — энергия колебаний ядер (в результате которых периодически изменяется относительное положение ядер), Евращ — энергия вращения ядер (в результате которых периодически изменяется ориентация молекулы в пространстве).
С
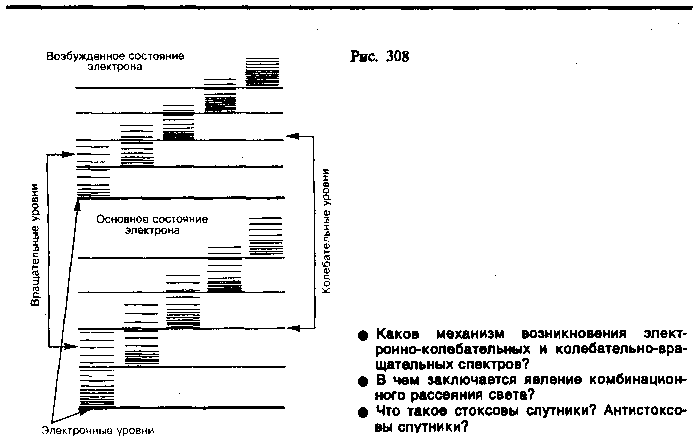 троение
молекул и свойства их энергетических
уровней проявляются в
молекулярных спектрах
— спектрах излучения (поглощения),
возникающих при квантовых переходах
между уровнями энергии молекул. Спектр
излучения молекулы определяется
структурой ее энергетических уровней
и соответствующими правилами отбора
(так, например, изменение квантовых
чисел, соответствующих как колебательному,
так и вращательному движению, должно
быть равно ± 1).
троение
молекул и свойства их энергетических
уровней проявляются в
молекулярных спектрах
— спектрах излучения (поглощения),
возникающих при квантовых переходах
между уровнями энергии молекул. Спектр
излучения молекулы определяется
структурой ее энергетических уровней
и соответствующими правилами отбора
(так, например, изменение квантовых
чисел, соответствующих как колебательному,
так и вращательному движению, должно
быть равно ± 1).
Итак, при разных типах переходов между уровнями возникают различные типы молекулярных спектров. Частоты спектральных линий, испускаемых молекулами, могут соответствовать переходам с одного электронного уровня на другой (электронные спектры) или с одного колебательного (вращательного) уровня на другой (колебательные (вращательные) спектры). Кроме того, возможны и переходы с одними значениями Eкол и Eвращ на уровни, имеющие другие значения всех трех компонентов, в результате чего возникают электронно-колебательные и колебательно-вращательные спектры. Поэтому спектр молекул довольно сложный.
Энергия, требуемая для диссоциации одной молекулы в свободном состоянии (в идеальном газе) при 0K, наз. энергией диссоциации. Энергия диссоциации характеризует прочность химической связи и измеряется методом электронного удара, калориметрически, из исследования термодинамич. равновесий, а также с помощью спектроскопич. и кинетич. методов.
