
- •24. Металлическая связь
- •[Природа
- •[История
- •]Свойства
- •]В воде [Механизм Гротгуса
- •]В нуклеиновых кислотах и белках
- •]В полимерах
- •25. Гибридизация
- •Особенности молекул, содержащих σ-связи
- •28. Механизм образования связи
- •Валентность атомов. Перекрывание атомных орбиталей
- •Гибридизация атомных орбиталей. Геометрическая форма частиц
- •Гибридизация атомных орбиталей. Геометрическая форма частиц
- •Геометрическая форма молекул и реакционная способность веществ
- •]Определение
- •]Связь с термодинамической устойчивостью системы
- •]Применение в химии []Связь с химическим потенциалом
- •]Историческая справка
- •30. Энергетические эффекты химических реакций
- •31. Превращение энергии при химических реакциях
- •]Определение
- •]Связь с термодинамической устойчивостью системы
- •]Применение в химии ]Связь с химическим потенциалом
- •Направленность химических процессов
- •[Определение
- •]Связь с термодинамической устойчивостью системы
- •]Применение в химии ]Связь с химическим потенциалом
- •]Энергия Гиббса и направление протекания реакции
- •]Историческая справка
- •35. []Скорость химической реакции
- •]Порядок химической реакции
- •]Реакция нулевого порядка
- •[]Реакция первого порядка
- •]Реакция второго порядка
- •]Молекулярность реакции
- •]Катализ
- •]Катализ в биохимии
- •]Равновесие
- •Способы выражения константы равновесия
- •]Стандартная константа равновесия
- •]Константа равновесия реакций в гетерогенных системах
- •]Константа равновесия и изменение энергии Гиббса
- •39. Гомогенные и гетерогенные реакции
- •Закон действующих масс
- •]Закон действующих масс в химической кинетике
- •]Закон действующих масс в химической термодинамике
- •]Методы расчета константы равновесия
- •[Править]Энтропийный расчёт изменения энергии Гиббса и константы равновесия реакции
28. Механизм образования связи
Ковалентная связь может быть образована путем обобществления электронов двух нейтральных атомов (обменный, или равноценный механизм образования связи). Например, для связи Н−Н: Н· + ·Н → Н−Н или Н · · Н
Такая же ковалентная связь Н-Н возникает при обобществлении электронной пары гидрид-иона Н− катионом водорода Н+ (донорно-акцепторный, иликоординационный механизм образования связи): Н+ + (:Н)− → Н−Н или Н · · Н
Катион Н+ - акцептор, а анион Н− - донор электронной пары.
Аналогичным образом при образовании ковалентной связи между атомом азота молекулы аммиака NH3 и катионом водорода H+ атом азота - донор, а катион водорода - акцептор электронной пары. В образующемся катионе аммония NH4+ все четыре связи N−H равноценны (одинаковы), и уже нельзя указать тот атом водорода, который был акцептором при образовании ковалентной связи.
Степень окисления азота и в молекуле аммиака, и в катионе аммония одинакова и равна −III.
Валентность атомов. Перекрывание атомных орбиталей
Основываясь на электронных формулах двух и многоатомных частиц (молекул, ионов), можно определить валентность каждого атома. С точки зрения строения молекул валентность атома в сложной частице - это число общих электронных пар у этого атома в данной частице (по одной на каждую связь), то есть число σ-связей, которые этот атом образовал с другими атомами при формировании сложной частицы.
Например, в молекуле HCl валентность атома водорода H и атома хлора Cl равна 1.
В молекуле аммиака NH3 валентность атома азота N равна 3, а в катионе аммония NH4+ валентность атома азота N равна 4 (при валентности каждого из атомов водорода H, равной 1).
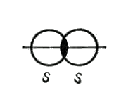
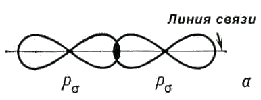
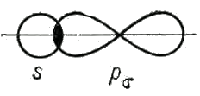
Ковалентная связь между атомами образуется при перекрывании атомных орбиталей, например 1s-орбиталей при образовании связи H−H, 2p-орбиталей при образовании связи F−F, 1s-орбитали атома H и 3p-орбитали атома Cl при образовании связи H−Cl.
При образовании химических связей всегда происходит сдвиг электронной плотности в направлении перекрывания, а это приводит к изменению формы орбиталей по сравнению с их состоянием в свободном атоме.
Гибридизация атомных орбиталей. Геометрическая форма частиц
Перекрывание атомных орбиталей при формировании двухатомных молекул АВ (А и В - атомы одного или разных элементов) ведет к линейной геометрической форме молекул (Н−Н, F−F, H−Cl).
Образование химических связей в многоатомных молекулах ведет к изменению формы и расположения орбиталей в пространстве у того атома, который образует две или более связей (атом А в частицах AВn), поскольку, в многоатомных частицах происходит гибридизация орбиталей центрального атома А (по теории, разработанной Л. Полингом в 1931 г.).
Типы гибридизации атомных орбиталей центрального атома определяют геометрическую форму частиц (молекул, ионов) AВn.
Гибридизация атомных орбиталей. Геометрическая форма частиц
Гибридизация |
Геометрическая форма |
Угол между связями |
sp |
Линейная |
180° |
sp2 |
Треугольная |
120° |
sp3 |
Тетраэдрическая |
109,5° |
sp3d |
Тригонально-бипирамидальная |
90°, 120° |
sp3d2 |
Октаэдрическая |
90° |
Для предсказания типа гибридизации атомных орбиталей пользуются алгоритмом, представляющим образование связи по донорно-акцепторному механизму.
Для молекулы или сложного иона AВn прежде всего определяют центральный атом и его степень окисления, затем устанавливают сокращенную электронную формулу центрального атома в данной степени окисления ("условного иона").
На схеме незавершенных подуровней условного иона показывают образование соответствующего числа связей А−В. Отсюда определяется тип гибридизации атомных орбиталей центрального атома А.
Если у атома А в молекуле (сложном ионе) AВn имеется неподеленная пара электронов, ее тоже следует учитывать при определении типа гибридизации. Эта неподеленная пара электронов считается направленной к "недостающему" атому-партнеру по химической связи.
Например, это имеет место в тетраэдрических молекулах аммиака NH3 и воды H2O. Такие тетраэдры называют незавершенными; кроме того, электростатическое отталкивание атомов водорода от неподеленной пары атома азота N или двух неподеленных пар атома кислорода O несколько искажает тетраэдрическую форму частицы и уменьшает углы между связями H−N−H и H−O−H.
Типы гибридизации sp3d (тригональная бипирамида) и sp3d2 (октаэдр) встречаются у атома серы S в молекулах SF4 и SF6 (при образовании связей S−F используются также 3d-орбитали, на которых в свободном атоме серы S электроны отсутствуют).
