
- •1 Вопрос. Параметры идеального газа.
- •2 Вопрос. Законы идеального газа.
- •3 Вопрос. Уравнение Клапейрона-Менделеева.
- •4 Вопрос. Изо-процессы с точки зрения уравнение Клапейрона-Менделеева.
- •5 Вопрос. Закон Максвелла о распределения молекул газа по скоростям и энергиям теплового движения.
- •6 Вопрос. Барометрическая формула. Распределение Больцмана.
- •7 Вопрос. Внутреннее трение вязкости.
- •8 Вопрос. Число степеней свободы. Внутренняя энергия.
- •9 Вопрос. Первое начало термодинамики.
- •10 Вопрос. Работа газа.
- •11 Вопрос. Теплоемкость.
- •12 Вопрос. Изобарный процесс.
- •13 Вопрос. Изохорный процесс.
- •14 Вопрос. Изотермический процесс.
- •15 Вопрос. Адиабатный процесс.
- •16 Вопрос. Круговой процесс (цикл).
- •17 Вопрос. Энтропия.
- •18 Вопрос. Второе начало термодинамики.
- •19 Вопрос. Цикл Карно.
- •Вопрос 20. Силы и потенциальная энергия межмолекулярного взаимодействия.
- •Вопрос 21. Уравнение Ван-дер-Ваальса.
- •Вопрос 22.Изотерма Ван-дер-Ваальса.
- •Вопрос 23. Внутренняя энергия реального газа.
- •Вопрос 24. Свойство жидкости.
- •Вопрос 25. Смачивание.
- •Вопрос 26. Давление от искривлённой поверхностью жидкости.
- •27 Вопрос. Капиллярное явлений.
- •28 Вопрос. Твердые тела.
- •Вопрос 29. Теплоемкость твердых тел.
- •Вопрос 30. Испарение, сублимация, плавление и кристаллизация.
- •Вопрос 31. Фазовые переходы 1 и 2 рода.
- •Вопрос 32. Диаграмма состояния. Тройная точка.
15 Вопрос. Адиабатный процесс.
Это процесс без теплообмена с окружающей средой то есть Q=0


Графически адиабатный процесс для наглядности изображают с изотермическим процессом.
Адиабатный
процесс подчиняется уравнение Пуассона.
 ,
, ,
,
 .
Где
.
Где
 показатель адиабаты. Вычислим работу
совершаемую газом в адиабатном процессе
показатель адиабаты. Вычислим работу
совершаемую газом в адиабатном процессе
 если газ расширяется, от объема
если газ расширяется, от объема
 то
его температура уменьшается от
то
его температура уменьшается от

 применяя для работы уравнение Пуассона
формулу можно преобразовать в виде
применяя для работы уравнение Пуассона
формулу можно преобразовать в виде
 .
.
Рассмотренные
процессы имеют общею особенность они
происходят при постоянной теплоемкости
в изохорном и изобарном это
 в изотермическом теплоемкость =
в изотермическом теплоемкость =
 бесконечность в адиабатном =0. Процесс
в котором теплоемкость остается
постоянном называется политропным
исходя из первого начало термодинамики
при условии постоянства С=const
можно вывести уравнение политропы
бесконечность в адиабатном =0. Процесс
в котором теплоемкость остается
постоянном называется политропным
исходя из первого начало термодинамики
при условии постоянства С=const
можно вывести уравнение политропы
 где
n показатель политропы.
При С=0 то
где
n показатель политропы.
При С=0 то
 .
При
.
При
 то
то
 .
При
.
При
 .
При
.
При
 .
.
16 Вопрос. Круговой процесс (цикл).
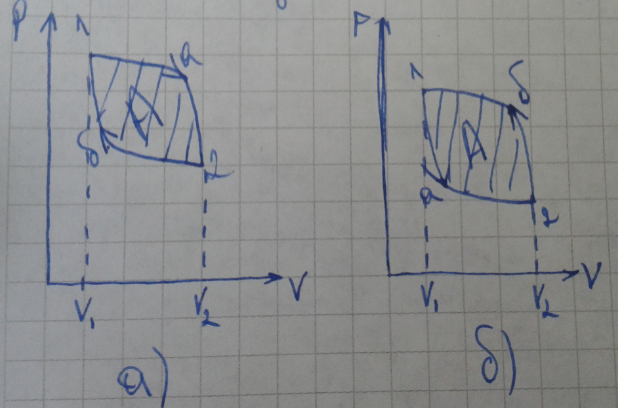 Циклом
называется система, пройдя через ряд
состояний, возвращается в исходную.
Циклом
называется система, пройдя через ряд
состояний, возвращается в исходную.
Цикл
на диаграмме изображается замкнутой
кривой. Цикл можно разбить на процессы
расширения и сжатия 2-1. Работа расширения
положительна
 работа сжатия отрицательная
работа сжатия отрицательная
 .
Работа совершаемая газом за цикл
определяется площадью заштрихованной
фигурой. Если работа за цикл положительная
(рис а)
.
Работа совершаемая газом за цикл
определяется площадью заштрихованной
фигурой. Если работа за цикл положительная
(рис а)
 то такой цикл называется прямым (протекает
по часовой стрелке). Если работа за цикл
отрицательная (рис б)
то такой цикл называется прямым (протекает
по часовой стрелке). Если работа за цикл
отрицательная (рис б)
 то такой цикл называется обратным
(протекает против часовой стрелки).
Прямой цикл используется в тепловых
двигателях это периодически действующие
двигатели совершающие работу за счёт
полученной извне теплоты. Обратный цикл
используется в холодильных машинах, в
которых за счет работы внешних сил
теплота переносится к телу с более
высокой температурой. В результате
кругового процесса система возвращается
в исходное состояние, следовательно
то такой цикл называется обратным
(протекает против часовой стрелки).
Прямой цикл используется в тепловых
двигателях это периодически действующие
двигатели совершающие работу за счёт
полученной извне теплоты. Обратный цикл
используется в холодильных машинах, в
которых за счет работы внешних сил
теплота переносится к телу с более
высокой температурой. В результате
кругового процесса система возвращается
в исходное состояние, следовательно
 .
Первое начало термодинамики для цикла
имеет вид
.
Первое начало термодинамики для цикла
имеет вид
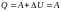 в результате кругового процесса система
может как получать теплоту
в результате кругового процесса система
может как получать теплоту
 ,
так и отдавать
,
так и отдавать
 .
.
 цикл
характеризуется термическим коэффициентом
полезного действия
цикл
характеризуется термическим коэффициентом
полезного действия
 .
Термодинамический процесс называется
обратимым если он может происходить
как в прямом так и в обратном направлении.
.
Термодинамический процесс называется
обратимым если он может происходить
как в прямом так и в обратном направлении.
17 Вопрос. Энтропия.
Для
выяснения физического содержания этого
понятия рассматривают отношение теплоты
Q полученной телом в
изотермическом процессе к температуре
К теплоотдающего тела называемая
приведенным количеством теплоты
 .
Приведенное количество теплоты
сообщаемое телу в любом обратимом
круговом процессе
.
Приведенное количество теплоты
сообщаемое телу в любом обратимом
круговом процессе
 из равенства 0 интеграла следует что
под интегральное выражение есть полный
дифференциал некоторой функции которая
определяется только состоянием системы
и не зависит от пути которым система
пришла в это состояние обозначается
она
из равенства 0 интеграла следует что
под интегральное выражение есть полный
дифференциал некоторой функции которая
определяется только состоянием системы
и не зависит от пути которым система
пришла в это состояние обозначается
она
 функция состояния
функция состояния
 называется
энтропией. Для обратимых процессов
изменение энтропии
называется
энтропией. Для обратимых процессов
изменение энтропии
 для
необратимых энтропия возрастает
для
необратимых энтропия возрастает
 .
Последние выражения относится только
к замкнутым системам если система
обменивается теплотой с внешней средой
то ее энтропия может вести себя любым
образом. Изменение энтропии можно
представить в ввиду неравенства
Клаузиуса. Если система совершает
переход из состояния 1 в состояние 2 то
изменение энтропии
.
Последние выражения относится только
к замкнутым системам если система
обменивается теплотой с внешней средой
то ее энтропия может вести себя любым
образом. Изменение энтропии можно
представить в ввиду неравенства
Клаузиуса. Если система совершает
переход из состояния 1 в состояние 2 то
изменение энтропии
 .
Физический смысл имеет не сома энтропия
а разность.
.
Физический смысл имеет не сома энтропия
а разность.
Найдем
изменение энтропии в разных процессах
идеального газа так как
 тогда изменение энтропии
тогда изменение энтропии

или
 то
есть изменение энтропии при переходе
идеального газа из состояния 1 в состояние
2 не зависит от вида процесса. Для
адиабатного процесса Q=0
тогда
то
есть изменение энтропии при переходе
идеального газа из состояния 1 в состояние
2 не зависит от вида процесса. Для
адиабатного процесса Q=0
тогда
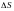 =0
а значит энтропия для данного процесса
величина постоянная. Адиабатный процесс
называют изоэнтропийным. Из последнего
выражения следует что при изотермическом
процессе (Т1=Т2)
=0
а значит энтропия для данного процесса
величина постоянная. Адиабатный процесс
называют изоэнтропийным. Из последнего
выражения следует что при изотермическом
процессе (Т1=Т2)
 .
Для изохорного процесса (V2=V1)
.
Для изохорного процесса (V2=V1)
 .
.
