
- •1 Вопрос. Параметры идеального газа.
- •2 Вопрос. Законы идеального газа.
- •3 Вопрос. Уравнение Клапейрона-Менделеева.
- •4 Вопрос. Изо-процессы с точки зрения уравнение Клапейрона-Менделеева.
- •5 Вопрос. Закон Максвелла о распределения молекул газа по скоростям и энергиям теплового движения.
- •6 Вопрос. Барометрическая формула. Распределение Больцмана.
- •7 Вопрос. Внутреннее трение вязкости.
- •8 Вопрос. Число степеней свободы. Внутренняя энергия.
- •9 Вопрос. Первое начало термодинамики.
- •10 Вопрос. Работа газа.
- •11 Вопрос. Теплоемкость.
- •12 Вопрос. Изобарный процесс.
- •13 Вопрос. Изохорный процесс.
- •14 Вопрос. Изотермический процесс.
- •15 Вопрос. Адиабатный процесс.
- •16 Вопрос. Круговой процесс (цикл).
- •17 Вопрос. Энтропия.
- •18 Вопрос. Второе начало термодинамики.
- •19 Вопрос. Цикл Карно.
- •Вопрос 20. Силы и потенциальная энергия межмолекулярного взаимодействия.
- •Вопрос 21. Уравнение Ван-дер-Ваальса.
- •Вопрос 22.Изотерма Ван-дер-Ваальса.
- •Вопрос 23. Внутренняя энергия реального газа.
- •Вопрос 24. Свойство жидкости.
- •Вопрос 25. Смачивание.
- •Вопрос 26. Давление от искривлённой поверхностью жидкости.
- •27 Вопрос. Капиллярное явлений.
- •28 Вопрос. Твердые тела.
- •Вопрос 29. Теплоемкость твердых тел.
- •Вопрос 30. Испарение, сублимация, плавление и кристаллизация.
- •Вопрос 31. Фазовые переходы 1 и 2 рода.
- •Вопрос 32. Диаграмма состояния. Тройная точка.
10 Вопрос. Работа газа.
Рассмотрим газ, находящийся под поршнем.
Е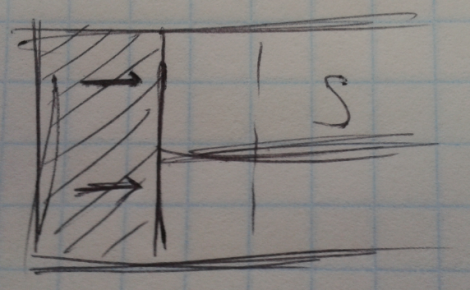 сли
газ расширяясь передвигает поршень на
малое расстояние то он производен над
ним работу
сли
газ расширяясь передвигает поршень на
малое расстояние то он производен над
ним работу
 ,
,
Р – давление, S – площадь поршня.

 .
.
Полную работу, совершаемую газом, при изменении его от V1 до V2 найдем проинтегрировав

Данное выражение справедливо при любых изменениях объёмов жидких, газообразных. Работу совершённого газа также можно изобразить графически.

То есть работа совершённая газом определяется площадью заштрихованной фигуры.
11 Вопрос. Теплоемкость.
Различают удельную и молярную теплоемкость.

Удельная теплоемкость показывает какое количество теплоты необходимо для нагревания одного килограмма вещества на один кельвин.


Различают также теплоемкости при постоянном объеме и при постоянном давлении когда процессе нагревания эти параметры остаются переменными (P=const V=const)
Первое начало термодинамики для одного моля газа с учетом молярной теплоемкости.
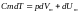
Если газ нагревают при постоянном объеме то работа внешних сил равна 0 и сообщаемая газу теплота идет только на увеличение внутренней энергии.
 Согласно
формуле
Согласно
формуле

Молярная теплоемкость при изохорном процессе.
Если газ нагревается при постоянном давлении то первое начало термодинамики в виде.

Учитывая
что
 не
зависит от вида процесса определяется
лишь температурой и всегда равна
не
зависит от вида процесса определяется
лишь температурой и всегда равна
 .
А также дифференцировав уравнение
Клаперона-Менделеева
получим
.
А также дифференцировав уравнение
Клаперона-Менделеева
получим
 данное выражение называется уравнением
Майера и показывает что
данное выражение называется уравнением
Майера и показывает что
 на газовую постоянную (для молярной
теплоёмкости). Это объясняется тем
на газовую постоянную (для молярной
теплоёмкости). Это объясняется тем
что
при нагревании газа P=const
требуется дополнительное количество
теплоты на совершение работы, так как
постоянство давления обеспечивается
увеличением объема. Выражение для
 можно представить в виде
можно представить в виде
 .
Удельные теплоемкости.
.
Удельные теплоемкости. .
.
Отношение
 называется показателем а
адиабаты.
называется показателем а
адиабаты.
12 Вопрос. Изобарный процесс.
Изобарный процесс подчиняется закону Гей-Люссака. См вопрос №2
При изобарном процессе газом совершается работа на увеличение объема.

Используя уравнение Клаперона-Менделеева для выбранных двух произвольных состояний
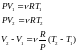 .
.

В
изобарном процессе газу сообщается
количество теплоты
 .
.
 первое
начало термодинамики.
первое
начало термодинамики.
13 Вопрос. Изохорный процесс.
Подчиняется закону Гей-Люссака. (См вопрос №2) и .
При
изохорном процессе газ не совершает
роботы над внешними силами.
 .
Первое начало термодинамики для данного
процесса имеет вид
.
Первое начало термодинамики для данного
процесса имеет вид
 то есть вся теплота сообщаемая газу
идет на увеличение его внутренней
энергии
то есть вся теплота сообщаемая газу
идет на увеличение его внутренней
энергии
 .
Для произвольной массы газа
.
Для произвольной массы газа
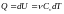 .
.
14 Вопрос. Изотермический процесс.
Процесс при постоянной температуре и подчиняющийся закону Бойля-Мариотта PV=const. Так как при T=const внутренняя энергия газа не изменяется dU=0 то все количество теплоты сообщаемое газу идет на совершение им работы против внешних сил
то
есть Q=A.
 Так как при изотермическом процессе
меняется не только объем ни и давление
то выражение можно проинтегрировать
по изменению давления
Так как при изотермическом процессе
меняется не только объем ни и давление
то выражение можно проинтегрировать
по изменению давления
 .
.
Для того чтобы при расширении газа температура не понижалась газу в течении процесса необходимо подводить количество теплоты эквивалентную внешней работе.
