
- •1.Основные законы химии. Закон эквивалентов закон Авагадро. Закон дальтона.
- •1)Закон кратных отношений.
- •Закон эквивалентов
- •Для расчета эквивалента кислоты надо молярную массу разделить на основность.
- •2.Химическая кинетика. Состояние систем. Основные понятия. Функция состояния первый закон термодинамики.
- •3.Термодинамика. Закон Гесса. Следствия закона Гесса. Водородный показатель. Ионное произведение воды.
- •4.Зависимость теплового эффекта реакции от температуры. Уравнение Кирхгофа. Расчет h при различных температурах.
- •5.Второе начало термодинамики. Статическая интерпретация энтропии. Уравнение Больцмана
- •6. Расчет изменения энтропии при нагревании. Расчет константы равновесия по закону действующих масс.
- •7. Изменение энергии Гиббса как критерий самопроизвольного течения процесса
- •9,10. Расчет константы равновесия по закону действующих масс. Химическое равновесие….
- •9. Химическое равновесие. Расчет константы равновесия по термодинамическим данным : ∆h, ∆s, ∆g
- •17. Реакция второго порядка
- •18.Влияние температуры на равновесие. Изобара Ван Гоффа.
- •Разделим переменные и проинтегрируем уравнения изобары Ван Гоффа
- •19. Теория переходного состояния. Энергия активации реакции.
- •20. Расчет эдс гальванических элементов, оставленных из электродов 1 и 2 рода.
- •21.Расчет ph растворов кислот и оснований
- •22.Условие смещение химического равновесия. Принцип Ле-Шателье
- •23.Образование растворов. Способы выражения концентрации растворов
- •24.Коррозия. Протекторная защита металлов от коррозии.
- •25.Электрохимия. Электродов 1 рода. Уравнения Нернста для электродов 1 рода.
- •26.Образование растворов. Способы выражения концентрации растворов
- •27.Растворы электролитов. Теория электролитической диссоциации Аррениуса. Равновесие в растворах электролитов. Сильные и слабые электролиты.
- •28.Электролиз. Правила разряда ионов при электролизе. Процессы, протекающие на катоде и аноде при электролизе.
- •29.Растворы неэлектролитов. Закон Генри. Закон Рауля
- •30.Химическая кинетика. Молекулярность и порядок реакции. Графическое определение порядка реакции.
- •31. Коррозия. Виды коррозии. Механизм электрохимической коррозии.
- •34.Электролиз. Законы Фарадея. Катодное нанесение покрытий и анодное растворение металла
- •35.Гальванический элемент Якоби-Даниэля. Расчет эдс гальванических элементов, составленных из электродов 1 рода
- •36.Газовые электроды. Расчет эдс водородного электрода
34.Электролиз. Законы Фарадея. Катодное нанесение покрытий и анодное растворение металла
Первый закон электролиза Фарадея: масса вещества, осаждённого на электроде при электролизе, прямо пропорциональна количеству электричества, переданного на этот электрод. Под количеством электричества имеется в виду электрический заряд, измеряемый, как правило, в кулонах.
Второй закон электролиза Фарадея: для данного количества электричества (электрического заряда) масса химического элемента, осаждённого на электроде, прямо пропорционально эквивалентной массе элемента. Эквивалентной массой вещества является его молярная масса, делённая на целое число, зависящее от химической реакции, в которой участвует вещество.
![]()
Где :
m — масса осаждённого на электроде вещества в граммах
Q — полный электрический заряд, прошедший через вещество
F = 96,485 C mol−1 — постоянная Фарадея
M — молярная масса вещества
z — валентное число ионов вещества (число электронов на один ион).
Для первого закона Фарадея M, F и z являются константами, так что чем больше величина Q, тем больше будет величина m.
Для второго закона Фарадея Q, F и z являются константами, так что чем больше величина M/z (эквивалентная масса), тем больше будет величина m.
Катодное нанесение покрытий и анодное растворение металла
35.Гальванический элемент Якоби-Даниэля. Расчет эдс гальванических элементов, составленных из электродов 1 рода
Цинк лучше растворяется в растворах своих солей то есть легче отдает ионы в раствор, чем медь, и поэтому он заряжается отрицательно. На поверхности цинка будет находиться избыток электронов. В то же время медь, обладая меньшей скоростью растворения, заряжается положительно, так как скорость перехода ионов из раствора на поверхность меди больше, чем скорость перехода ионов меди с пластинки в раствор. На поверхности пластинки в результате этого возникает недостаток электронов - пластинка заряжается положительно (рис.1). Если соединить эти пластинки проводником (например, медной проволокой), то избыточная часть электронов, имеющихся в цинке, будет переходить на медную пластинку это приводит к понижению заряда цинковой пластинки и нарушает равновесие двойного электрического слоя. Для восстановления равновесия двойного слоя с пластинки в раствор будет переходить определенное количество цинка. При переходе избыточных электронов с цинковой пластинки на медную положительный заряд последней будет уменьшаться. Для сохранения равновесия в двойном электрическом слое часть положительных ионов из раствора будет выделяться на медной пластинке.
Таким образом, разность в зарядах пластинки, обусловленная переходом электронов с цинковой пластинки на медную, будет восстанавливаться.
В результате возникает самопроизвольно протекающий процесс, сопровождающийся растворением цинковой пластинки и выделением на медной пластинке положительно заряженных ионов меди и их разрядкой. Это направленное течение электронов по проводнику и представляет электрический ток, который можно измерить при помощи соответствующих приборов.
Электрический ток, определяемый разностью потенциалов между электродами в таких обратимых условиях их работы, называется электродвижущей силой элемента.
На основании теоретических расчетов установлено, что величина электродного потенциала, возникающая на границе между металлом и раствором соли этого металла, то есть раствором, содержащим ионы этого металла, равна:
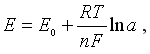
где Е0 - постоянная, характерная для данного металла; R - газовая постоянная, равная 8,32 Дж/град•моль; Т - абсолютная температура; n - степень окисления металла в данном соединении, то есть число электронов, которое теряет атом металла, превращаясь в ион; F - число Фарадея, равное 96500 Кл; α - активная молярная концентрация ионов металла в данном растворе.
Это уравнение выражает зависимость потенциала металла от концентрации его ионов в растворе и называется уравнением электродного потенциала, известным под названием уравнения Нернста.
ЭДС гальванического элемента, составленного из любой пары электродов, можно вычислить по разности потенциалов электродов, если пренебречь потенциалом, возникающим на границе раздела двух растворов (этот потенциал называется диффузионным); он по своей величине много меньше электродных потенциалов.
ЭДС принято выражать положительной величиной. Например, в медно-цинковом гальваническом элементе
Cu | CuSO4 || ZnSO4 | Zn
раствор раствор
цинк - отрицательный электрод, а медь - положительный. Нормальный потенциал цинка при 25° С равен -0,76 В. Нормальный потенциал меди при 25°С равен +0,34 В. ЭДС медно-цинкового гальванического элемента равна (+0,337) - (-0,763) = + 1,10 (В), то есть:
Eo = ECu - EZn = Eo
(Cu2+/Cu) - Eo (Zn2+/Zn) = +0.337 - (-0.763) = +1.100 В.
Если ЭДС элемента положительна, то реакция (так, как она записана в элементе) протекает самопроизвольно. Если ЭДС отрицательна, то самопроизвольно протекает обратная реакция.
