- •Вопрос 1
- •Вопрос 2
- •Вопрос 3.
- •Вопрос 4.
- •Вопрос 5
- •Вопрос 6
- •Вопрос 7
- •Вопрос 8
- •Вопрос 11.
- •Вопрос 15.
- •Вопрос 16
- •Вопрос 17
- •Вопрос 18
- •Вопрос 20
- •Вопрос 21
- •Вопрос 22
- •Вопрос 22. Атом водорода. Потенциалы возбуждения и ионизации. Квантовые числа. Вырожденные состояния.
- •Вторая часть билета!
- •Вопрос 23. Ширина спектральных линий. Мультиплетность спектров. Спин электрона. Магнетон Бора.
- •24.Спин орбитальное взаимодействие. Эффект Зеемана. Принцип Паули. Расположение элементов в системе Менделеева.
- •Вопрос 25. Ионная и ковалентная связи атомов в молекуле. Энергия диссоциации. Полная энергия молекулы. Вращательные, колебательно-вращательные полосы.
- •Вопрос 26. Вынужденное излучение. Мазеры. Лазеры. Накачка метастабильных уровней. Свойства лазерного излучения.
- •27. Фазовое пространство. Функция распределения. Понятие о квантовой статистике Бозе-Эйнштейна и Ферми-Дирака.
- •29.Квантовая теория свободных электронов в металле. Уровень Ферми. Запрещенные зоны. Валентная зона. Зона проводимости
- •30.Электропроводность металлов. Сверхпроводимость. Температурные зависимости проводимости.
- •31.Дырочная проводимость. Примесная проводимость. Запрещенные зоны. Валентная зона. Зона проводимости.
- •32.Работа выхода. Термоэлектронная эмиссия. Контактная разность потенциалов.
- •33). Контактные явления в полупроводниках
- •35). Основные свойства атомного ядра.
- •36). Масса и энергия связи. Дефект массы. Деление тяжелых и синтез легких ядер.
- •37.Ядерные силы. Модели ядра. Мезоны.
- •1.Капельная модель ядра.
- •2.Оболочечная модель ядра.
- •38.Радиоактивность. Постоянная распада. Альфа, бета и гамма излучения. Закон радиоактивного распада.
- •39. Альфа-распад. Бета-распад. Правила смещения.
- •40). Реакция деления ядра. Цепная реакция деления.
- •41 Космическое излучение. Типы взаимодействия элементарных частиц. Частицы и античастицы
- •42 Классификация элементарных частиц. Кварки.
Вопрос 18
 Согласно
модели атома Томсона атом представляет
собой непрерывно заряженный положительным
зарядом шар радиусом порядка 10
Согласно
модели атома Томсона атом представляет
собой непрерывно заряженный положительным
зарядом шар радиусом порядка 10![]() м
внетри которого около своих положений
равновесия колеблются электроны;
суммарный отрицательный заряд электронов
равен положительному заряду шара,
поэтому атом в целом нейтрален. Через
несколько лет было доказано, что
представление о непрерывно распределенном
внутри атома положительном заряде
ошибочно. Ядерная модель атома Резерфорда
согласно этой модели вокруг положительного
ядра имеющего заряд Ze (Z-
порядковый номер элемента в системе
Менделеева, е- элементарный заряд) размер
10
м
внетри которого около своих положений
равновесия колеблются электроны;
суммарный отрицательный заряд электронов
равен положительному заряду шара,
поэтому атом в целом нейтрален. Через
несколько лет было доказано, что
представление о непрерывно распределенном
внутри атома положительном заряде
ошибочно. Ядерная модель атома Резерфорда
согласно этой модели вокруг положительного
ядра имеющего заряд Ze (Z-
порядковый номер элемента в системе
Менделеева, е- элементарный заряд) размер
10![]() -10
-10![]() м и массу практически равную массе
атома, в области с линейными размерами
порядка 10
м о замкнутым орбитам движется электроны
образуя электронную оболочку атома.
Т.к атомы нейтральны, то заряд ядра равен
суммарному заряду электронов, т.е вокруг
ядра должно вращаться Z
электронов. Попытки построить модель
атома в рамках классической физики не
привели к успеху: модель Томсона была
опровергнута опытами Резерфорда, ядерная
же модель оказалась неустойчивой
электродинамически и противоречила
опытным данным.
м и массу практически равную массе
атома, в области с линейными размерами
порядка 10
м о замкнутым орбитам движется электроны
образуя электронную оболочку атома.
Т.к атомы нейтральны, то заряд ядра равен
суммарному заряду электронов, т.е вокруг
ядра должно вращаться Z
электронов. Попытки построить модель
атома в рамках классической физики не
привели к успеху: модель Томсона была
опровергнута опытами Резерфорда, ядерная
же модель оказалась неустойчивой
электродинамически и противоречила
опытным данным.
Постулаты Бора: 1 : в атоме существуют
стационарные состояния в которых он не
излучает энергии. Стационарным состоянием
атомасоответствуют стационарные орбиты,
по которым движутся электроны. Движение
электронов по стационарным орбитам не
сопровождается излучением электромагнитных
волн. В стационарном состоянии атома
электрон, двигаясь по круговой орбите
должен иметь дискретные квантовые
значения момента импульса удовлетворяющие
условию
![]() (n=1,2,3,…) где
(n=1,2,3,…) где
![]() -масса
электрона υ-его скорость по n-й
орбите радиуса
-масса
электрона υ-его скорость по n-й
орбите радиуса
![]()
Второй постулат Бора: при переходе
электрона с одной стационарной орбиты
на другую излучается один фотон с
энергией
![]() равной разности энергий соответствующих
стационарных состояний атома до и после
излучения.
При
равной разности энергий соответствующих
стационарных состояний атома до и после
излучения.
При
![]() происходит
излучение фотона наоборот- его поглощение.
Набор возможных дискретных частот
происходит
излучение фотона наоборот- его поглощение.
Набор возможных дискретных частот
![]() квантовых переходов определяет линейчатый
спектр атома.
квантовых переходов определяет линейчатый
спектр атома.
Состояния с одинаковой энергией называют вырожденными, а число различных состояний с каким-либо значением энергии называется кратностью вырождения соответствующего энергетического уровня.
Исходя из этих постулатов и используя планетарную модель строения атома, Н. Бор разработал количественную теорию атома водорода. Он рассчитал радиусы стационарных орбит электрона в атоме водорода и вычислил соответствующие им значения энергии.
Расчет
радиусов орбит.' Электрон
движется вокруг ядра в атоме водорода
по круговой орбите под действием
кулоновской силы, которая сообщает ему
центростремительное ускорение. По
второму закону Ньютона ![]()
Центростремительное
ускорение ![]() электрону
сообщает кулоновская сила притяжения
со стороны ядра
электрону
сообщает кулоновская сила притяжения
со стороны ядра ![]() Следовательно,
Следовательно,
![]() откуда
откуда ![]() (20.1)
(20.1)
Согласно
III постулату Бора: ![]() отсюда
отсюда
![]() (20.2)
(20.2)
Из
уравнений (20.1) и (20.2) получим ![]() Откуда
Откуда
![]() (20.3)
(20.3)
выражение
для радиусов разрешенных стационарных
орбит электрона в атоме водорода.
Здесь n —
номер орбиты, радиус которой r, ![]() —
электрическая постоянная, h —
постоянная Планка, m —
масса электрона, е —
заряд электрона.
—
электрическая постоянная, h —
постоянная Планка, m —
масса электрона, е —
заряд электрона.
Мы
видим, что радиусы
стационарных устойчивых орбит возрастают
пропорционально квадратам номеров
орбит (рис.
20.3): ![]() и
т.д. Если электрон в атоме водорода
находится на одной из стационарных
орбит, то атом обладает определенным
значением энергии, определяемой энергией
электрона:
и
т.д. Если электрон в атоме водорода
находится на одной из стационарных
орбит, то атом обладает определенным
значением энергии, определяемой энергией
электрона:![]() (Знак
"-" перед потенциальной энергией
означает, что за
(Знак
"-" перед потенциальной энергией
означает, что за ![]() принято
то значение, которое соответствует
принято
то значение, которое соответствует ![]() ).
Подставив в эту формулу значения
).
Подставив в эту формулу значения ![]() и r из
формул (20.2) и (20.3), получим:
и r из
формул (20.2) и (20.3), получим:
Таким
образом, энергия электрона, находящегося
на n-й
орбите,![]() (20.4)
(20.4)
Из
этой формулы видно, что значения энергии
атома водорода квантованы и, чем больше
n, тем больше энергия Wn.
![]() Сравнивая
это выражение с эмпирической формулой
Сравнивая
это выражение с эмпирической формулой![]() (20.5)
видим, что постоянная Ридберга
(20.5)
видим, что постоянная Ридберга ![]() следовательно,
в формуле (20.5) k —
номер орбиты, с которой происходит
переход электрона в атоме, n —
номер орбиты, на которую переходит
электрон.
следовательно,
в формуле (20.5) k —
номер орбиты, с которой происходит
переход электрона в атоме, n —
номер орбиты, на которую переходит
электрон.
Закономерности
Линейчатый
спектр атома представляет собой
совокупность большого числа линий,
разбросанных по всему спектру без
всякого видимого порядка. Однако
внимательное изучение спектров показало,
что расположение линий следует
определенным закономерностям. Эти
закономерности выступают на сравнительно
простых спектрах, характерных для
простых атомов.
В
1885 г. Иоганн Якоб Бальмер установил, что
частоты отдельных линий водорода
выражаются простой формулой: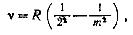 где
n означает частоту света, т. е. число
волн, испускаемых в единицу времени, R
— называемая постоянной Ридберга
величина, равная 3,28984•1015 с-1, и m — целое
число. Если задавать для т значения 3,
4, 5 и т. д., то получаются значения, очень
хорошо совпадающие с частотами
последовательных линий спектра водорода.
Совокупность этих линий составляет
серию Бальмера.
В
дальнейшем было обнаружено, что в спектре
водорода еще имеются многочисленные
спектральные линии, которые также
составляют серии, подобные серии
Бальмера.
Частоты
этих линий могут быть представлены
формулами
где
n означает частоту света, т. е. число
волн, испускаемых в единицу времени, R
— называемая постоянной Ридберга
величина, равная 3,28984•1015 с-1, и m — целое
число. Если задавать для т значения 3,
4, 5 и т. д., то получаются значения, очень
хорошо совпадающие с частотами
последовательных линий спектра водорода.
Совокупность этих линий составляет
серию Бальмера.
В
дальнейшем было обнаружено, что в спектре
водорода еще имеются многочисленные
спектральные линии, которые также
составляют серии, подобные серии
Бальмера.
Частоты
этих линий могут быть представлены
формулами
![]() (серия
Лаймана),
(серия
Лаймана),
![]() (серия
Пашена),
причем
R имеет то же самое числовое значение,
что и в формуле Бальмера. Таким образом,
все водородные серии можно объединить
одной формулой:
(серия
Пашена),
причем
R имеет то же самое числовое значение,
что и в формуле Бальмера. Таким образом,
все водородные серии можно объединить
одной формулой:![]() где
n и m — целые числа, причем m³n+1.
Спектры
других атомов значительно сложнее, и
распределение их линий в серии не так
просто. Оказалось, однако, что спектральные
линии всех атомов могут быть распределены
в серии. Крайне важно, что сериальные
закономерности для всех атомов могут
быть представлены в форме, подобной
формуле Бальмера, причем постоянная R
имеет почти одно и то же значение для
всех атомов.
Вопрос
19
где
n и m — целые числа, причем m³n+1.
Спектры
других атомов значительно сложнее, и
распределение их линий в серии не так
просто. Оказалось, однако, что спектральные
линии всех атомов могут быть распределены
в серии. Крайне важно, что сериальные
закономерности для всех атомов могут
быть представлены в форме, подобной
формуле Бальмера, причем постоянная R
имеет почти одно и то же значение для
всех атомов.
Вопрос
19
Де Броиль выдвинул гипотезу об универсальности корпускулярно-волнового дуализма. Утверждал что не только фотоны но и электроны и любые другие частицы материи наряду с корпускулярными обладают так же волновыми свойствами. Согласно де Бройлю, с каждым микрообъектом связываются, с одной стороны корпускулярные характеристики- энергия Е и импульс р а с другой волновые характеристики- частота ν и длина волны λ. Количественные соотношения, связывающие корпускулярные и волновые свойства частиц, такие же как для фотонов
![]() ,
,
![]() это соотношение постулировалось не
только для фотонов, но и для других
микрочастиц, и для таких которые обладают
массой покоя. λ=h/p Это соотношение
справедливо для любой частицы с импульсом
р. Американские физики Дэвиссон и Джермер
обнаружили что пучок электронов
рассеивающийся от естественной диф
решетки- кристалла никеля дает отчетливую
дифракционную картину. Диф максимумы
соответствовали формуле Вульфа-Бреггов,
а брэгговская длина волны оказалась
равной длине волны вычисленной по
формуле λ=h/p . В дальнейшем формула де
Бройля была подтверждена опытами
Тартаковского и Томсона наблюдавших
диф картину при прохождении пучка
быстрых электронов через металлическую
фольгу. Т.к диф картина исследовалась
для потока электронов, то необходимо
было доказать, что волновые свойства
присуши не только потоку большой
совокупности электронов, но и каждому
электрону в отдельности. Это удалось
доказать Фабриканту. Он показал, что
даже в случае слабого электронного
пучка, возникающая при длительной
экспозиции дифракционная картина не
отличается от дифракционных картин
получаемых при короткой экспозиции для
потоков электронов в десятки млн раз
больше интенсивных. Волновые свойства
частиц не являются свойством их
коллектива, а присущи каждой частице в
отдельности.. Согласно соотношению
неопределенностей Гейзенберга,
микрочастица не может иметь одновременно
и определенную координату и определенную
соответствующую проекцию импульса,
причем неопределенности этих величин
удовлетворяют условиям
это соотношение постулировалось не
только для фотонов, но и для других
микрочастиц, и для таких которые обладают
массой покоя. λ=h/p Это соотношение
справедливо для любой частицы с импульсом
р. Американские физики Дэвиссон и Джермер
обнаружили что пучок электронов
рассеивающийся от естественной диф
решетки- кристалла никеля дает отчетливую
дифракционную картину. Диф максимумы
соответствовали формуле Вульфа-Бреггов,
а брэгговская длина волны оказалась
равной длине волны вычисленной по
формуле λ=h/p . В дальнейшем формула де
Бройля была подтверждена опытами
Тартаковского и Томсона наблюдавших
диф картину при прохождении пучка
быстрых электронов через металлическую
фольгу. Т.к диф картина исследовалась
для потока электронов, то необходимо
было доказать, что волновые свойства
присуши не только потоку большой
совокупности электронов, но и каждому
электрону в отдельности. Это удалось
доказать Фабриканту. Он показал, что
даже в случае слабого электронного
пучка, возникающая при длительной
экспозиции дифракционная картина не
отличается от дифракционных картин
получаемых при короткой экспозиции для
потоков электронов в десятки млн раз
больше интенсивных. Волновые свойства
частиц не являются свойством их
коллектива, а присущи каждой частице в
отдельности.. Согласно соотношению
неопределенностей Гейзенберга,
микрочастица не может иметь одновременно
и определенную координату и определенную
соответствующую проекцию импульса,
причем неопределенности этих величин
удовлетворяют условиям
![]() ,
,
![]() ,
,
![]() ,
т.е произведение неопределенностей
к
,
т.е произведение неопределенностей
к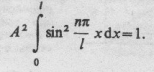 оординаты
и соответствующей ей проекции импульса
не может быть меньше величина порядка
h. Из соотношения неопределенностей
следует что если микрочастица находится
в состоянии с точечным значением
координат то в этом состоянии
соответствующая проекция ее импульса
оказывается совершенно неопределенной
и наоборот. Для микрочастицы не существует
состояний, в которых ее координаты и
импульс имели бы одновременно точные
значения.
оординаты
и соответствующей ей проекции импульса
не может быть меньше величина порядка
h. Из соотношения неопределенностей
следует что если микрочастица находится
в состоянии с точечным значением
координат то в этом состоянии
соответствующая проекция ее импульса
оказывается совершенно неопределенной
и наоборот. Для микрочастицы не существует
состояний, в которых ее координаты и
импульс имели бы одновременно точные
значения.