
- •Содержание
- •Лекция 4. Качественный анализ. Анализ анионов………………………………………………………….45
- •Контрольные задания по дисциплине "Экоаналитическая химия" Теоретические вопросы………………………………………………………………146
- •Лекция 1. Экологическая аналитическая химия и физико-химические методы анализа
- •Часть 1. Основы эколого-химического анализа и применяемые в контроле окружающей среды аналитические реакции
- •Тема 1. Теоретические основы эколого-аналитической химии
- •(A)Основные термины и определения
- •Наиболее распространенные физические и физико-химические методы анализа
- •Важнейшие области применения физических и физико-химических методов анализа в экологическом мониторинге
- •Методы разделения и концентрирования
- •Некоторые указания по выполнению аналитических операций и их важнейшие характеристики
- •Контрольные вопросы (для самоподготовки):
- •Литература
- •Лекция 2
- •Количество и концентрация вещества:
- •Приготовление и измерение различными способами
- •Статья II.Измерение объемов растворов 1
- •Описание мерной посуды и правила работы с ней
- •Мерные колбы
- •Статья III.Приготовление растворов из стандарт-титров
- •Статья IV.Пипетки
- •Статья V.Бюретки
- •3.1. Определения основных понятий
- •3.2. Аналитические признаки веществ и аналитические реакции
- •Бесцветный ярко сине-голубой
- •Бесцветный ярко красный
- •Окрашивание пламени соединениями некоторых элементов
- •3.3. Типы аналитических реакций и реагентов
- •3.4. Характеристики чувствительности аналитических реакций
- •3.5. Подготовка образца к анализу
- •3.5.1. Отбор средней пробы
- •3.5.2. Растворение пробы
- •3.6. Проведение анализа
- •Литература:
- •Лекция 4. Качественный анализ. Анализ анионов
- •4.1. Аналитические реакции. Аналитический признак.
- •Дробный и систематический анализы.
- •Практические работы Лабораторная работа №1 обнаружение индивидуальных анионов и анализ смесей анионов
- •Третья группа анионов
- •Дробный анализ смеси анионов
- •Лекция 5. Качественный анализ катионов
- •5.1. Аналитическая классификация катионов по группам [1]. Статья VI. Статья VII.Введение
- •5.2. Различные аналитические классификации катионов по группам
- •Рекомендуемая литература:
- •Количественный анализ
- •Классификация методов количественного анализа
- •Требования, предъявляемые к реакциям в количественном анализе
- •Статистическая обработка результатов количественного анализа
- •Повторить некорректно проведенный анализ — это непременное правило.
- •1.4.1. Правильность и воспроизводимость результатов.
- •1.4.2. Классификация ошибок количественного анализа.
- •Количественный химический анализ гравиметрический анализ (гравиметрия)
- •Загрязнение осадков
- •Основные операции гравиметрического анализа
- •Лекция 7. Обзор методов анализа. Электрохимические инструментальные методы анализа (рН-метрия и ионселективная потенциометрия). Обзор методов анализа.
- •1. Классификация и важнейшие характеристики методов анализа, применяемых в мониторинге ос
- •2. Электрохимические методы анализа
- •Лекция 8. Спектрально–оптические методы анализа
- •Лекция 9. Хроматографические методы анализа
- •5. Другие методы анализа
- •1.1. Приборы радиационной разведки и
- •1.2. Назначение и характеристики технических средств химической разведки и химического контроля
- •Газоанализатор типа «Колион»
- •Формулы перехода от одних выражений концентраций растворов к другим
- •Вопросы к зачету по разделу курса «Экоаналитическая химия» «Качественный анализ»
- •2. Какие Вы знаете операции качественного химического анализа?
- •3. Какие бывают классификации катионов (групповые реактивы)?
- •4. Какие s-элементы составляют I и II группы катионов и каковы их свойства?
- •5. Какие p-элементы входят в состав III, IV и V групп катионов и каковы их свойства?
- •6. Какие d-элементы входят в состав IV, Vи VI групп катионов и каковы их свойства?
- •Контрольные задания по дисциплине "Экоаналитическая химия" Теоретические вопросы
- •Вопросы по методам анализа. Химические методы количественного анализа Гравиметрия
- •Титриметрические методы
- •Экстракция
- •Спектроскопические методы
- •Хроматографические методы
- •Электрохимические методы
- •Расчетные задачи по различным типам равновесия и методам анализа
- •Задания по теме "Концентрация растворов"
- •Задача 2.
- •Задача 3.
- •Задача 4.
- •Задачи и тесты для контроля усвоения темы
- •Вариант 1
- •Вариант 2
- •Вариант 4
- •Вариант 5
- •Вопросы
- •127994, Москва, ул. Образцова, 9, стр. 9
Лекция 2
Количество и концентрация вещества:
Приготовление и измерение различными способами
Статья II.Измерение объемов растворов 1
Цель занятия: ознакомиться с мерной посудой, используемой в химическом анализе и приобрести некоторые первичные навыки работы с ней.
Задания:
1) зарисовать образцы мерной посуды в лабораторном журнале;
2) наполнить мерную колбу водой до метки (более сложный вариант – приготовление раствора из фиксанала);
3) отмерить 10,00 мл воды пипеткой Мора;
4) отмерить: 6,2 мл и 3,7 мл воды градуированными пипетками на 10 мл и 5 мл;
5) измерить объем одной капли, вытекающей из бюретки.
Посуда: мерные колбы, пипетки Мора и градуированные, резиновые груши, бюретки, воронки, мензурка, цилиндры и мерные пробирки; на столе преподавателя – микробюретка.
Описание мерной посуды и правила работы с ней
Для точного измерения объемов в химическом и, прежде всего, в титриметрическом анализе используются мерные колбы, пипетки и бюретки (рис. 1–3). Для не очень точных объемных измерений применяют цилиндры, мензурки и мерные пробирки.
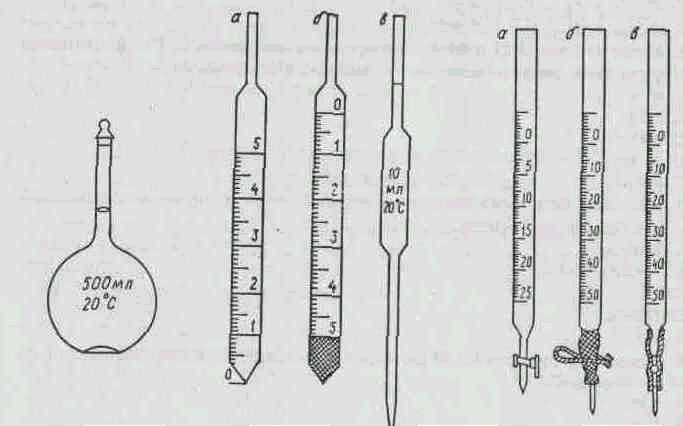
Рис. 1. Мерная колба Рис. 2. Пипетки: Рис. 3. Бюретки:
а, б – градуированные; а – с краном; б – с зажимом; в – пипетка Мора в – с шариковым затвором
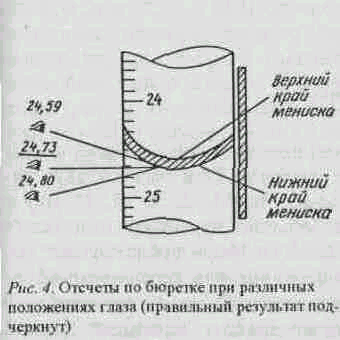
При измерении объемов следует помнить, что глаз экспериментатора должен находиться на одном уровне с мениском отмериваемой жидкости. При этом объем прозрачных жидкостей отмеривают по нижнему краю мениска, а интенсивно окрашенных (например раствора KMn04) – по верхнему (рис. 4).
Посуда, используемая в химическом анализе, должна быть химически чистой. Перед работой пипетки и бюретки тщательно моют моющими смесями, например хромовой смесью (раствор К2Сr207 в концентрированной H2S04), концентрированной азотной кислотой, спиртовым раствором щелочи или водным содовым раствором, заполняя ими бюретку с помощью воронки, а пипетку – с помощью груши. Затем их многократно ополаскивают сначала водопроводной водой, а затем дистиллированной. Убедившись в том, что вода смачивает внутренние стенки ровным слоем (если же на стенках собираются капли, то мытье повторяют), пипетку или бюретку 2–3 раза ополаскивают тем раствором, которым собираются заполнять бюретку или который должны отбирать пипеткой. Выполните задание 1.
Мерные колбы
Мерные колбы предназначены для приготовления стандартных растворов, а также для разбавления растворов до указанных объемов. Это плоскодонные колбы с длинным узким горлом, на котором нанесена круговая метка, а на широкой части указан номинальный объем раствора, который можно приготовить (или отмерить) с помощью данной колбы при определенной температуре (см. рис. 1).
Мерные колбы бывают различной вместимости: от 25 мл до 2 л.
Сухие навески (в том числе содержимое фиксаналов) вносят в мерную колбу через воронку, смывая затем остаток вещества с воронки (и ополаскивая ампулу фиксанала) дистиллированной водой. Доведение объема раствора до метки производят осторожно, а последние капли жидкости вблизи метки добавляют с помощью глазной пипетки. Если жидкость оказалась налита выше метки, то раствор первичного стандарта или приготовленный из фиксанала считается испорченным.
После доведения объема жидкости в колбе до метки (по нижнему краю мениска) колбу закрывают пробкой и тщательно перемешивают раствор в колбе, несколько раз переворачивая ее вверх дном. Более подробно этот процесс описан далее.
