
- •Содержание
- •Лекция 4. Качественный анализ. Анализ анионов………………………………………………………….45
- •Контрольные задания по дисциплине "Экоаналитическая химия" Теоретические вопросы………………………………………………………………146
- •Лекция 1. Экологическая аналитическая химия и физико-химические методы анализа
- •Часть 1. Основы эколого-химического анализа и применяемые в контроле окружающей среды аналитические реакции
- •Тема 1. Теоретические основы эколого-аналитической химии
- •(A)Основные термины и определения
- •Наиболее распространенные физические и физико-химические методы анализа
- •Важнейшие области применения физических и физико-химических методов анализа в экологическом мониторинге
- •Методы разделения и концентрирования
- •Некоторые указания по выполнению аналитических операций и их важнейшие характеристики
- •Контрольные вопросы (для самоподготовки):
- •Литература
- •Лекция 2
- •Количество и концентрация вещества:
- •Приготовление и измерение различными способами
- •Статья II.Измерение объемов растворов 1
- •Описание мерной посуды и правила работы с ней
- •Мерные колбы
- •Статья III.Приготовление растворов из стандарт-титров
- •Статья IV.Пипетки
- •Статья V.Бюретки
- •3.1. Определения основных понятий
- •3.2. Аналитические признаки веществ и аналитические реакции
- •Бесцветный ярко сине-голубой
- •Бесцветный ярко красный
- •Окрашивание пламени соединениями некоторых элементов
- •3.3. Типы аналитических реакций и реагентов
- •3.4. Характеристики чувствительности аналитических реакций
- •3.5. Подготовка образца к анализу
- •3.5.1. Отбор средней пробы
- •3.5.2. Растворение пробы
- •3.6. Проведение анализа
- •Литература:
- •Лекция 4. Качественный анализ. Анализ анионов
- •4.1. Аналитические реакции. Аналитический признак.
- •Дробный и систематический анализы.
- •Практические работы Лабораторная работа №1 обнаружение индивидуальных анионов и анализ смесей анионов
- •Третья группа анионов
- •Дробный анализ смеси анионов
- •Лекция 5. Качественный анализ катионов
- •5.1. Аналитическая классификация катионов по группам [1]. Статья VI. Статья VII.Введение
- •5.2. Различные аналитические классификации катионов по группам
- •Рекомендуемая литература:
- •Количественный анализ
- •Классификация методов количественного анализа
- •Требования, предъявляемые к реакциям в количественном анализе
- •Статистическая обработка результатов количественного анализа
- •Повторить некорректно проведенный анализ — это непременное правило.
- •1.4.1. Правильность и воспроизводимость результатов.
- •1.4.2. Классификация ошибок количественного анализа.
- •Количественный химический анализ гравиметрический анализ (гравиметрия)
- •Загрязнение осадков
- •Основные операции гравиметрического анализа
- •Лекция 7. Обзор методов анализа. Электрохимические инструментальные методы анализа (рН-метрия и ионселективная потенциометрия). Обзор методов анализа.
- •1. Классификация и важнейшие характеристики методов анализа, применяемых в мониторинге ос
- •2. Электрохимические методы анализа
- •Лекция 8. Спектрально–оптические методы анализа
- •Лекция 9. Хроматографические методы анализа
- •5. Другие методы анализа
- •1.1. Приборы радиационной разведки и
- •1.2. Назначение и характеристики технических средств химической разведки и химического контроля
- •Газоанализатор типа «Колион»
- •Формулы перехода от одних выражений концентраций растворов к другим
- •Вопросы к зачету по разделу курса «Экоаналитическая химия» «Качественный анализ»
- •2. Какие Вы знаете операции качественного химического анализа?
- •3. Какие бывают классификации катионов (групповые реактивы)?
- •4. Какие s-элементы составляют I и II группы катионов и каковы их свойства?
- •5. Какие p-элементы входят в состав III, IV и V групп катионов и каковы их свойства?
- •6. Какие d-элементы входят в состав IV, Vи VI групп катионов и каковы их свойства?
- •Контрольные задания по дисциплине "Экоаналитическая химия" Теоретические вопросы
- •Вопросы по методам анализа. Химические методы количественного анализа Гравиметрия
- •Титриметрические методы
- •Экстракция
- •Спектроскопические методы
- •Хроматографические методы
- •Электрохимические методы
- •Расчетные задачи по различным типам равновесия и методам анализа
- •Задания по теме "Концентрация растворов"
- •Задача 2.
- •Задача 3.
- •Задача 4.
- •Задачи и тесты для контроля усвоения темы
- •Вариант 1
- •Вариант 2
- •Вариант 4
- •Вариант 5
- •Вопросы
- •127994, Москва, ул. Образцова, 9, стр. 9
Количественный химический анализ гравиметрический анализ (гравиметрия)
Гравиметрический анализ — совокупность методов количественного анализа, основанных на выделении определяемого количества в виде какого-либо соединения и определения его массы.
Относительная погрешность этого анализа — от 0,1 % до 0,01 %.
В гравиметрическом анализе используются методы:
отгонки определяемого вещества в виде какого-либо летучего соединения;
осаждения из раствора в виде малорастворимого соединения.
Методы отгонки используют, например, для определения содержания кристаллизационной воды в кристаллогидратах, а также при анализе карбонатов, некоторых нитратов и других соединений, образующих летучие продукты реакции. Содержание определяемого компонента находят по разнице массы вещества до и к после термической обработки.
Чаще в гравиметрическом анализе используют методы осаждения. В этом случае гравиметрический анализ проводят по массе осадка, образовавшегося при взаимодействии определяемого компонента с раствором какого-либо реагента (осадителя).
Гравиметрический анализ с использованием осаждения включает несколько последовательных операций:
Осаждение определяемого компонента в виде малорастворимого соединения, называемого осаждаемой формой.
Отделение осадка от раствора фильтрованием.
Промывание осадка.
Нагревание осадка для удаления воды или его прокаливание для превращения осадка в подходящую для взвешивания химическую форму, называемую гравиметрической.
Взвешивание полученного осадка (гравиметрической формы).
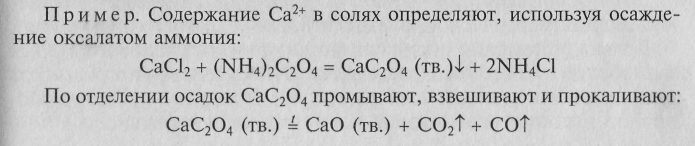
Образовавшийся (в примере) оксид кальция взвешивают и по его количеству рассчитывают содержание кальция в анализируемом веществе.
В гравиметрическом анализе различают осаждаемую и гравиметрическую формы вещества.
В приведенном примере СаС2О4 — осаждаемая форма, а СаО — гравиметрическая. Иногда гравиметрическая и осаждаемая формы являются одним и тем же соединением. Например, при определении Ва2+ их осаждают из раствора в виде Ва8О4. Этот осадок отделяют от раствора, промывают, прокаливают и взвешивают. При прокаливании удаляются вода и летучие примеси, но состав осадка не меняется, т. е. гравиметрической и осаждаемой формой является ВаSО4.
К веществам в осаждаемой и гравиметрической формах предъявляются разные требования, основные из которых следующие.
Для осаждаемой формы осадок а) должен быть практически нерастворим: после осаждения и промывания осадка его потери не должны превышать погрешности взвешивания на аналитических весах (приблизительно ±0,0002 г для обычно используемых в лаборатории). Расчеты показывают, что такие осадки соответствуют произведению растворимости ПР < 10-12. Для уменьшения растворимости обычно прибавляют избыток осадителя;
б) должен образоваться в форме, удобной для его отделения от раствора фильтрованием и промыванием, а также в чистом виде. Таким требованиям отвечают крупнокристаллические осадки. Они легко фильтруются, имеют меньшую общую поверхность, поэтому адсорбцией посторонних веществ можно пренебречь, и такие осадки легче отмыть при промывании. Если осадки получаются аморфными (скрытокристаллическими), то они должны быть однородными и скоагулированными;
в) легко и полностью превращаться в вещество гравиметрической формы.
Для вещества в гравиметрической форме осадок должен после сушки и прокаливания соответствовать определенной химической формуле;
быть химически устойчивым на воздухе, т.е. мало гигроскопичным, не поглощать диоксид углерода и другие газы, входящие в состав воздуха;
иметь, по возможности, большую молекулярную массу. Тогда относительная погрешность взвешивания уменьшается.
Эти требования определяют выбор соединений для осаждаемой и гравиметрической формы, а также условия их получения.
Гравиметрический анализ является одним из наиболее старых и наиболее точных методов анализа. Относительная погрешность анализа обычно не превышает нескольких десятых процента. Основной недостаток этого метода — его продолжительность.
Механизм образования осадка и условия осаждения
Для получения точных результатов в гравиметрическом анализе необходимо образование чистых крупнокристаллических осадков. Поэтому необходимо предусмотреть условия осаждения, при которых образуются крупные кристаллы.
Образование осадка начинается с формирования зародышей или центров кристаллизации. Если скорость образования центров кристаллизации небольшая по сравнению со скоростью роста кристаллов, то в растворе образуется небольшое число крупных кристаллов. Если скорость образования центров кристаллизации превышает скорость роста кристаллов, то в растворе образуется больше мелких кристаллов.
Для уменьшения числа центров кристаллизации необходимо уменьшить концентрацию определяемого вещества и увеличить перед началом осаждения его растворимость. С этой целью перед осаждением раствор разбавляют и нагревают. Для увеличения растворимости также вводят электролит — чаще всего соли аммония, или подкисляют раствор. Но существуют соединения (гидроксиды алюминия, железа и др.), растворимость осадков которых нельзя увеличить перед осаждением, не удается получить в виде крупнокристаллических образований, и они выпадают в виде мелкокристаллических или аморфных.
