
Температура появи первинного розплаву в основному визначається числом оксидів, що входять у суміш. У подвійній системі СаО-SiО2 в області, обмеженій С2S-С3S, з'являється розплав при 1900°С. Після додавання до цієї суміші А12О3 різко знижується температура появи первинного розплаву — до 1450°С.
Оскільки 96—98% загального складу клінкеру становлять чотири основних оксиди СаО, SiО2, Аl2О3, Fе2О3, найбільш істотною для клінкеру є чотирикомпонентна система СаО-А12О3-SiО2-Fі2О3. Установлено, що найбільш легкоплавка евтектика в ній утвориться при 1338°С. Такі оксиди, як МgО, К2О, Nа2О, сприяють подальшому зниженню температури утворення рідкої фази до 1280°С. Інші домішки вже не роблять істотного впливу, і незалежно від складу, спікання реальних цементних сумішей починається при 1260—1280°С.
Дослідженнями встановлено, що за флюсуючою дією, оксиди можна розташувати по убуванню їхньої сили дії в наступний ряд:
Fe2O3→Al2O3→MgО.
У реальних сумішах у період спікання спочатку розплав утвориться внаслідок появи легкоплавких евтектик між алюмінатами, алюмоферитами й другорядними складовими. До 1400°С відбувається повне розплавлювання алюмінатів і феритів, алюмоферитний розплав, що утворився розчиняє певну кількість С2S і вільного вапна. Кількість розплаву, що утвориться, залежить від вмісту в суміші А12O3, Fе2О3, МgО і лугів, співвідношення між А12O3 і Fе2O3 (тому що це співвідношення визначає, які мінерали утворяться: С3А, С4АF або С2F) , а також від температури розплаву. У зв'язку з тим, що в промислових печах температура спікання, як правило, не перевищує 1450°С, дослідження впливу більш високої температури на процес має вирішальне значення лише при одержанні плавлених цементів.
Кількість рідкої фази можна приблизно розрахувати, користуючись формулами, виведеними з аналізу чотирикомпонентної системи. При цьому, залежно від глиноземного модуля клінкеру, при температурі нижче 1400°С розрахунок ведуть за різними формулами, а вище 1400°С, коли в розплав переходить вся кількість А12О3 і Fе2О3, що міститься в клінкері.
Залежно від складу сировинної суміші кількість рідкої фази може коливатися від 15 до 30%, однак частіше становить 20-30%. Склад рідкої фази можна визначити за спеціальними графіками.
Кількість розплаву в суміші помітно збільшується при переході від евтектичної точки (1338оС) до температури, при якій розплавляється весь А12О3 і Fе2О3 (близько 1400°С). Подальше підвищення температури до 1450°С сприяє приросту розплаву лише на 1 — 2%. Однак для зниження в'язкості розплаву й створення тим найкращих умов для кристалізації необхідно довести температуру до 1450°С.
В'язкість розплаву є важливим технологічним фактором, який необхідно враховувати при виборі сполуки суміші. При введенні невеликої дози мінералізатора в період утворення рідкої фази в основному змінюється в'язкість розплаву, а не його кількість. На жаль, в'язкість клінкерних розплавів у цей час вивчена ще недостатньо.
Досить багато досліджень проведено лише в потрійній системі СаО-А12О3-SiО2 і для складів, що відповідають доменним шлакам. Про в'язкість у четверній системі СаО-А12O3-SiО2-Fe2O3 є неповні дані. Однак і вони дозволяють установити характер впливу тих або інших компонентів на зміну в'язкості. Установлено, що знижують в'язкість розплаву Fе2О3, МgО, МnО, а SiО2 і А12O3 підвищують її. Що стосується СаF2, то його вплив на в'язкість є досить складним. При введенні СаF2 у кількості до 1 % , в'язкість помітно знижується, при введенні більшої кількості СаF2 в'язкість різко збільшується, тому що розплав стає пересиченим стосовно СаF2. Це спричиняє кристалізацію й загальне згущування розплаву. За ступенем впливу на в'язкість клінкерних розплавів добавки можна розташувати в наступний ряд:
Na2O < Ca < Mg < Fe2O3 < Mn.
В'язкість розплавів промислових клінкерів коливається від 1 до 30—35 пз. Особливо висока в'язкість характерна для клінкерів, що мають високий глиноземистий модуль (рис. 4.7).
В'язкість розплаву, як і електропровідність, тісно пов'язана з його будовою. У цей час установлено, що розплави мають іонну будову. У таких розплавах катіони лужних і лужноземельних металів, що утворять іонний зв'язок з киснем, є іонами-модифікаторами. Вони досить рухливі. Катіони Si4+, А13+, Fе3+ утворюють із киснем переважно ковалентний зв'язок і втримуються в розплаві у вигляді стійких комплексних аніонів [Si4]4-, [Al4]5-, [FеО4]5- і т.п. Ці комплексні аніони й утворять каркас у розплаві. У розплаві при зміні температури можливі процеси ускладнення й роздрібнення іонів за рахунок взаємодії комплексних іонів між собою й з іонами-модифікаторами.
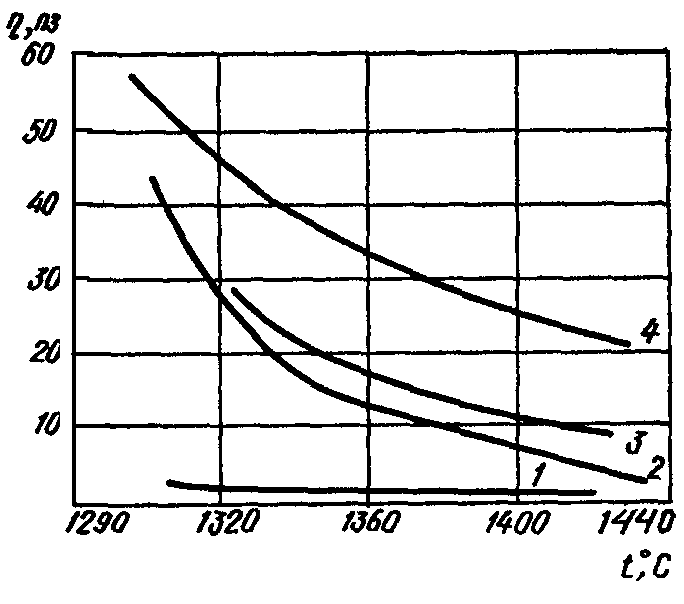
Рис. 4.7. В'язкість клінкерних розплавів:
1- р = 0,64; 2 – р =1,02; 3 – р =1,4; 4 – р =2.
Установлено, що в системі МеxОу-SiО2 ступінь полімеризації іонів [Si4]4- у розплаві визначається співвідношенням MeхОу : SiО2 — чим воно менше, тим більше ступінь полімеризації.
Якщо в'язкість розплаву в основному визначається рухливістю аніонів, то електропровідність — рухливістю іонів-модифікаторів. У розплавах, за складом близьких до евтектичних, при додаванні невеликих кількостей таких оксидів, як СаО, Fе2О3, К2O, МgО, електропровідність зростає. Найбільше збільшують електропровідність луги й МgО. При збільшенні кількості SiО2 і А12О3 електропровідність знижується. Отже, суміші, що мають високий глиноземистий модуль, менш реакційно-спроможні не тільки тому, що в них утруднена рухливість аніонів, але й унаслідок погіршення рухливості катіонів.
При появі рідкої фази в ній розчиняється С2S і СаО. Вони піддаються електролітичній дисоціації на іони, які поєднуються внаслідок нейтралізації, що відбувається безупинно, і утворять спочатку зародки, а потім і кристали С3S, які мають меншу розчинність в розплаві, ніж С2S і СаО. Кристали С3S, що утворюються при рідинному спіканні, мають більш правильну форму, чим ті, які утворилися при твердо-фазних реакціях.
В обертовій печі тривалість рідинного спікання становить 20—35 хв. Оскільки аліт утворюється в основному в рідкій фазі, у якій утримується багато інших елементів, у його кристалічну решітку впроваджуються іони А13+, Мg2+, К+, Na+. У кристали аліту іноді вкраплені зерна беліту й вільного вапна. Це або залишки мінералів, що ще не встигли прореагувати, або вторинні продукти, що виникли при розпаді С3S. Якщо в період, що передував спіканню, утворилися дрібні (до 20 мкм) кристали беліту, то кінетика утворення аліту, в основному, визначається швидкістю дифузії й в'язкістю розплаву. Якщо ж у системі є великі кристали беліту, то визначальним фактором є швидкість їхнього розчинення.
Кристалізація аліту може відбуватися як одностадійно, так і двостадійно. При одностадійній кристалізації розміри кристалів у клінкері порівняно однакові, а при двостадійній - неоднакові. Установлено, що двостадійна кристалізація має місце при низькій реакційній здатності складових цементних сумішей і більшому помелі.
Найбільш сприятливими для роботи печей є клінкери, що містять 23-28% рідкої фази. Вони мають дрібну рівномірну гранулометрію, сприяють утворенню стійкої обмазки. Клінкери, що містять 15-20% рідкої фази, вимагають більш високої температури випалу, важко утворюють обмазку, знижують продуктивність печей. Клінкери, що мають високий вміст рідкої фази, утворюють звари в печі.
Заключною стадією випалу є охолодження. На цій стадії відбувається фіксація в клінкері гідравлічно активних модифікацій клінкерних мінералів. З розплаву першими викристалізовуються С3S і C2S, а алюмінати й алюмоферити, як більш легкоплавкі, кристалізуються при більш низькій температурі. Режим охолодження впливає на структуру клінкеру, характер кристалізації й форму клінкерних мінералів, а також на вміст склоподібної фази.
При тому самому хімічному складі клінкер може мати різний фазовий склад. Залежність мінералогічного складу клінкеру від швидкості охолодження характеризується даними, наведеними в табл. 4.4.
Таблиця 4.4.
Залежність мінералогічного складу клінкеру від
швидкості охолодження
Мінерали |
Склад клінкеру при охолодженні, % |
|||
повільному |
швидкому |
середньому |
різкому |
|
C3S C2S C3A C4AF Скло |
59,8 18,5 12,8 6,1 - |
65,2 9,2 - - 22,4 |
65,2 14,2 8,0 6,1 3,8 |
70 5-4 - - 20,6 |
При незалежній кристалізації розплаву ступінь невідповідності мінералогічного складу клінкеру розрахунковому буде залежати від глиноземного модуля. Якщо р > 2, то кількість аліту в клінкері буде більше розрахункового, при р < 0,9 — менше розрахункового, а при р = 0,9—1,8 спостерігається відповідність розрахункового й фактичного вмісту мінералів.
На практиці умови охолодження бувають такими, що частина розплаву встигає кристалізуватися. Швидкість охолодження впливає не тільки на мінералогічну сполуку, але й на структуру клінкеру, При швидкому охолодженні утворяться дрібні кристали із чіткими гранями. Найбільш сприятливо рівномірний розподіл мінералів у масі клінкеру, причому бажано, щоб аліт кристалізувався у вигляді витягнутих у довжину кристаликів.
При повільному охолодженні клінкеру можуть виникнути такі небажані явища:
1) кристалізація MgО у вигляді періклазу, що може викликати нерівномірність зміни об'єму;
2) частковий перехід β-С2S в γ-С2S, що спричиняє зниження гідравлічної активності;
3) часткове розкладання аліту.
Цементи з клінкерів, що повільно охолоджуються, при високому р характеризуються помилковим схоплюванням і низькою початковою міцністю.
4.8. Вплив різних факторів на процеси утворення
Вплив хімічного й мінералогічного складу сировинної суміші. Між спікливістю клінкеру й такими його характеристиками, як коефіцієнт насичення КН і модулі n і р існує безпосередній зв'язок. Чим вище КН, тим гірше відбувається спікання клінкеру, тим більше в суміші залишається незасвоєного вапна. Спікливість також погіршується й зі збільшенням модулів бенкет. Однак якщо при спікливості для КН і п зберігається прямолінійна залежність (рис. 4.8), той вплив величини р на спікливість складніше.
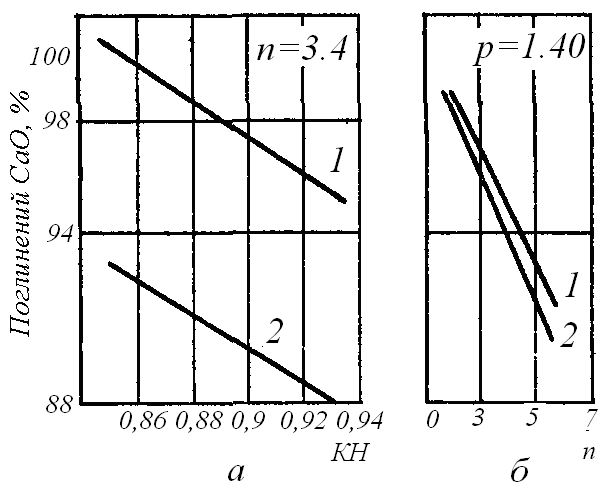
Рис. 4.8. Вплив коефіцієнта насичення (КН) і кремнеземистого модуля (n) на спікливість сировинних сумішей:
а) 1- р =1,02; 2 – р =3,3; б) 1- t =1400оС; 2 – t =1350оС.
Мінералогічний склад суміші також впливає на спікливість. Реакційна здатність сумішей у першу чергу залежить від реакційної здатності алюмосилікатного компонента. По активності в період протікання твердофазових реакцій, за даними Ю. М. Бутта й В. В. Тімашева, алюмосилікатні матеріали можуть бути розташовані в наступний (убутний) ряд:
монтмориллонит>галлуазит> біотит> каолініт> пирофиллит>
>мусковіт>вермикуліт.
При подальшому підвищенні температури реакційна здатність глинистих мінералів вирівнюється.
Значно меншою активністю, ніж глинисті мінерали, володіють кварц і польові шпати. Так, установлено, що якщо кварц подрібнити навіть до часток величиною менше 60 мкм, то й тоді його активність буде значно нижче активності каолініту.
З карбонатних компонентів найбільш реакційно-спроможною є крейда. Активність крупнокристалічних вапняків, за даними ряду дослідників, нижче, ніж дрібнокристалічних. Суміші, у які замість карбонатів уводиться Са(ОН)2, проявляють високу активність. Це пояснюється тим, що СаО, отриманий із Са(ОН)2, активніше СаО, що утворився з кальциту. Якщо до складу суміші ввести негашене вапно СаО, то його реакційна здатність падає, тому що під дією високих температур відбувається рекристалізація.
Але найбільш сприятливими для протікання реакцій клінкероутворення є мергелі, у яких тісний контакт між частками глини й вапняку обумовлює досить високу реакційну здатність сумішей.
Заміна глинистого компонента в шихті шлаками приводить до зниження активності. Особливо помітно знижується активність при введенні кислих шлаків, тому що вони містять складні алюмосилікати, які спочатку піддаються хімічному розпаду, а потім вступають у взаємодію з вапном. Тому ступінь засвоєння вапна у вапняково-шлакових сумішах при низьких температурах незначний. Максимум засвоєння вапна приходиться на інтервал температур 1300—1400°С. Основні шлаки трохи активніше кислих, тому що в них уже втримуються C2S, С3S2 і СS.
При швидкому випалі активність шихти на основі белітового шламу, що містить в основному двокальцієвий силікат, частково й у гідратованій формі, підвищується. При повільному випалі її активність падає у зв'язку з тим, що C2S встигає рекристалізуватися.
Вплив ступеню дисперсності вихідних компонентів.
Тонкість млива суміші впливає на процеси клінкероутвореня як на стадії реакцій у твердих фазах, так і на стадії рідкофазового спікання. Установлено, що в грубодисперсних сумішах значно частіше, ніж у тонкодисперсних, залишається незасвоєне вапно. Грубий помел позначається й на структурі клінкеру, у ньому спостерігаються групові скупчення мінералів, що чергуються. Припустима тонкість помелу сировини значною мірою визначається його мінералогічною природою, а виходить, і реакційною здатністю. Так, сировинні суміші на мергелях, белітових шламах і доменних шлаках вимагають меншої тонкості помелу, ніж на карбонатно-глиняній сировині.
Глинисті компоненти звичайно містять значну кількість часток розміром менше 5 мкм, тому особлива увага повинна приділятися помелу вапнякового компонента. Розміри зерен кальциту в суміші не повинні перевищувати 100 мкм, а при виробництві високомарочних цементів - 50-60 мкм. Породи, що містять значну кількість кварцу й халцедону, необхідно подрібнювати ще тонше (розмір їхніх зерен повинен бути в основному 30 мкм; а при випуску високоміцних цементів - 15 мкм).
У зв'язку з різною здатністю до розмелювання окремих компонентів шихти, у різних її фракціях утримується різна кількість тих або інших оксидів. У фракціях 0,5—15 мкм утримується підвищена кількість СаО й А12О3 і знижена кількість SiО2. SiО2, що важко розмелюється, зосереджує в більших фракціях. Якщо Fe2O3 уводиться з піритними недогарками, то його вміст у тонких фракціях знижується внаслідок труднощів здрібнювання, якщо ж застосовується залізна руда, то відбувається збагачення тонких фракцій оксидами заліза, що значно підвищує швидкість взаємодії компонентів у твердих фазах.
При визначенні доцільної тонкості помелу враховується не тільки спроможність до спікання, але й техніко-економічні показники.
Вплив домішок мінералізаторів і легуючих добавок. Активність і технологічні властивості цементів визначаються не тільки мінералогічним складом клінкеру, але й характером кристалізації мінералів, структурою клінкеру, розміром і формою кристалів, а також впливом на мінерали в процесі мінералоутворення різних мінералізаторів, каталізаторів, інгібіторів реакцій, стабілізаторів і речовин, що модифікують, які вносяться в суміш із компонентами сировини або із золою палива.
І в карбонатному компоненті, і в глинистій сировині, а також у коригувальних добавках (особливо в піритних недогарках, колошниковому пилу) утримуються сульфати. Вміст сірчаного ангідриду в сировинній суміші, розраховуючи на прожарену речовину, у середньому коливається від 0,22 до 2,23%. Сірка в сировині втримується, як правило, у вигляді гіпсу або піриту.
У порівнянні з карбонатом кальцію швидкість дисоціації сульфату кальцію максимальна при більш високих температурах (приблизно на 150—270°С вище). Тому повна заміна карбонатного компонента сульфатним спричиняє різке зниження реакційної здатності суміші, тобто падіння продуктивності обертової печі. Пірит, навпроти, дисоціює значно раніше. Він починає розкладатися при температурі 500°С. Оскільки в печі звичайно підтримується окисна атмосфера, то, в остаточному підсумку, продуктами розкладання як сульфату, так і сульфіду будуть СаО й SO3. У результаті зіткнення газової суміші із сировинною сумішшю в інтервалі температур 750—800°С утвориться вторинний сульфат кальцію, яким суміш усе більше збагачується. У присутності лугів значна частина сірчистого й сірчаного ангідриду йде на утворення термічно стійких лужних сульфатів К2SО4, Nа2SО4 або ЗК2SO4∙ Na2SО4, що, у свою чергу, затримує видалення лугів. Велика кількість сульфатів винесеться з пилом. Сульфати утворять комплексні сполуки типу силікосульфатів в інтервалі температур 1000—1250°С.
Установлено, що в певних кількостях сульфат кальцію сприятливо діє на реакції клінкероутворення. Він прискорює реакції силікатоутворення, знижує температуру утворення С3S до 1300—1350°С, стабілізує β-С2S. У присутності іона SO2 знижується в'язкість розплаву, збільшується кількість рідкої фази. Сульфат захищає зростаючі кристали C3S від ресорбції й розпаду, які відбуваються при тривалому перебуванні аліту в рідкій фазі. Однак перевищення граничного вмісту сульфату (більше 1-3%) може привести до випадання з рідкої фази сульфоалюмінату кальцію, що супроводжується виділенням надлишку СаО.
МgО, що часто вносять у шихту з вапняками або доменним шлаками, як уже вказувалося, негативно впливає на кінцеві властивості продукту, викликаючи нерівномірність зміни об'єму. У доломітизованих вапняках МgО міститься у вигляді карбонатів, а в шлаках - у вигляді магнезіальної шпінелі, монтичелліту, окерманіту, мервиніту й шлакового скла.
Донедавна вважалося, що МgО, який входить до складу силікатів і алюмосилікатів, у процесі клінкероутворення залишається зв'язаним. Однак дослідження останнього років показали, що вапно може витісняти магнезію з її сполук і лише 30-40% МgО залишається зв'язаним з кислотними оксидами.
Присутність у сировинній суміші силікатів магнію забезпечує одержання клінкеру з більше дрібною кристалізацією періклазу, тоді як карбонати приводять до утворення укрупнених кристалів. При використанні замість глинистого компонента доменних шлаків періклаз кристалізується також у вигляді рівномірно розподілених зерен розміром від 1 до 7 мкм.
Невелика кількість МgО в цементній суміші (до 2—3%) інтенсифікує процеси утворення мінералів у результаті збільшення кількості розплаву й зниження його в'язкості. Хоча в розплаві, що містить іони Мg2+, спостерігається деяке уповільнення переміщення іонів, що затримує утворення аліту, однак прискорення цієї реакції через зниження в'язкості перекриває це уповільнення. Вплив МgО на процеси утворення силікатів більш чітко проявляється в сумішах, що мають низький вміст рідкої фази.
Луги є небажаною домішкою в шихті. Вони впливають на властивості готового продукту, викликаючи деяке зниження міцності, прискорення тужавіння. Застосування цементу, що містить більше 1% лугів, і заповнювачів, що мають у своєму складі реакційно-спроможний кремнезем (опал, халцедон та інші), приводить до збільшення розширення бетону, зниження його морозостійкості, міцності й динамічного модуля пружності. На думку багатьох авторів, луги негативно впливають і на процеси утворення клінкеру, сповільнюють швидкість реакцій, негативно позначаються на стійкості футеровки. У сировині, що застосовується на більшості заводів, вміст лугів невеликий. Тільки декілька заводів випускають клінкер, що містить більше 1% лугів, у тому числі 5 заводів - більше 1,5%.
Вплив лугів на властивості цементу носить складний характер. Досить обґрунтованою є точка зору про те, що в цементному клінкері для загальнобудівельних цілей вміст лугів, у кількості 1,2%, а в клінкері для гідротехнічного бетону - 0,6%, є цілком припустимим. Вплив лугів на процеси утворення клінкеру залежить не тільки від сумарної їхньої кількості в сировині, але й від тонкості помелу, міцності кристалічної решітки лужних мінералів сировини й багатьох інших факторів.
Оскільки основна кількість лугів уводиться з алюмосилікатним компонентом сировини, кристалічні решітки мінералів — носіїв лугів — руйнуються при більше високій температурі, ніж глинисті мінерали. Це приводить до істотного вповільнення твердофазових реакцій утворення первинних силікатів, алюмінатів і алюмоферитів. За ступенем реакційної здатності до взаємодії із СаСО3 мінерали, що містять луги, можна розташувати в наступний (убутний) ряд: гідрослюда > слюда > польові шпати (лабрадор, альбіт, ортоклаз).
У шихтах, що містять ортоклаз, розпад його відбувається при температурах 900—950°С з утворенням лейциту й кремнезему. Останній вступає у взаємодію із СаО, утворюючи С2S.
З підвищенням температури в суміші утворяться алюмосилікати калію (К2О∙ А12О3 з 2SiО2, К2O∙ А12О3∙ SiО2) і К2О∙ А12О3, що, взаємодіючи із С3S і С3А, утворюють К2O∙23СаО∙12SiО2 і К2O∙8СаО∙ЗА12О3. Вивільнюваний К2O взаємодіє із сірчаним ангідридом, утворюючи К2SO4. Якщо сировинна суміш містить переважно Nа2О, у результаті утвориться досить стійкий Nа2О∙8СаО∙ЗА12О3 і видалення лугів зменшиться.
Уведення гіпсу в сировинну суміш, що містить луги, забезпечує більш інтенсивне протікання реакцій утворення клінкеру.
Сполука КС23S12 або, як вважають останнім часом, С2S, стабілізований К2О, менш активно взаємодіє в рідкій фазі із СаО, що гальмує утворення С3S. Аналогічно поводиться й NC23S12.
Пояснюється це тим, що іон Са2+ вступає в обмін із двома іонами Nа+, один із яких вбудовується в решітку мінералу, а інший у міжвузловий простір, ущільнюючи решітку С2S, що є причиною уповільненого засвоєння СаО. Крім того, іони Na+ витісняють Са2+ із кристалів С3S, причому в значно більшій кількості, ніж стехіометрична, тому що частина аліту при цьому розпадається. Про це свідчить поява в клінкері вільного вапна, а також утворення навколо кристалів аліту дрібних зерен беліту вторинного походження.
За даними ряду авторів, луги містяться практично у всіх клінкерних мінералах, особливо в белітові — К2О і в трикальцієвому алюмінаті — Nа2O.
Разом з тим, на окремих стадіях луги частково здійснюють позитивну дію на процеси мінералоутворення. Сульфати й карбонати калію й натрію, взаємодіючи з карбонатом кальцію, утворять подвійні солі Nа2Са(СO3)2 і К2Са(СO3)2, які мають низьку температуру плавлення (770—780)°С. Тому в суміші утворяться зони мікро-розплавів, які, розтікаючись по поверхні мінералів сировинної суміші, сприяють переносу окремих компонентів і тим самим прискорюють реакції в кілька разів. При 820— 825°С подвійний натрієво-кальцієвий карбонат розкладається з виділенням СаО, тобто практично прискорюється процес дисоціації СаСО3. Луги також інтенсифікують швидкість засвоєння вапна при температурах 900—1200°С. При температурах вище 1300°С луги, навпаки, гальмують цей процес, хоча невеликі кількості їх (0,2—0,3%) поліпшують кристалізацію С3S і С2S. Крім того, при дисоціації Nа2О в клінкерному розплаві утвориться іон-модифікатор Nа+, що знижує в'язкість розплаву на 0,2—0,5 пз.
Частина лугів, що утворилися при дисоціації лужних сполук, починаючи з температур 700—800°С видаляється й виноситься газовим потоком. З підвищенням температури цей процес посилюється, а після 1250—1270°С видалення різко зменшується внаслідок утворення рідкої фази.
Видалення лугів залежить не тільки від температури, але й від того, які мінерали є носіями лугів у сировині. Так, К2O видаляється значно активніше, ніж Na2О. Видалення К2O з гідрослюди становить до 65%, з ортоклазу — до 45, а видалення Nа2О з альбіту — лише 10%. Найбільшою стійкістю володіють сульфати. За ступенем видалення лугів мінерали, що входять до складу сировинної суміші, можна розташувати в наступний (убутний) ряд:
гідрослюди > хлориди > вториди > карбонати > гідрослюда>
> слюди > ортоклаз > альбіт > сульфати.
Уведення в сировинну суміш мінералізаторів, особливо фторидів і хлоридів у присутності водяних парів, збільшує видалення лугів. При цьому температура початку видалення знижується на 100—200°С, але й тоді К+ видаляється значно активніше, ніж Na+. Присутність у шихті гіпсу, навпаки, гальмує цей процес, тому що утворюються термічно стійкі лужні сульфати. Потрапляючи в зони з більш низькими температурами, луги конденсуються на поверхні сировинної суміші, на часточках пилу в газовому потоці й на поверхні теплообмінних пристроїв. Тому в печі відбувається багаторазова циркуляція лугів. Є дані про те, що кожний іон К+ до видалення з обертової печі піддається п'ятикратній сублімації й конденсації.
Кількість лугів, що залишилися в клінкері, залежить також і від способу виробництва, типу печі, ступеня використання вловленого пилу. При мокрому способі виробництва лугів видаляється більше, ніж при сухому. Найнижче видалення лугів спостерігається в печах із циклонними теплообмінниками (3-10%), значно більший - в обертовій печі із частковим поверненням пилу (27-33%) і в печах з конвеєрним кальцинатором (12-19%).
У цей час може бути рекомендовано кілька технологічних прийомів, що забезпечують зниження кількості лугів у клінкері:
- більш тонке здрібнювання компонента шихти, що містить луги;
- підвищення температури випалу;
- живлення печей при сухому способі виробництва більш дрібними гранулами;
- зменшення повернення вловленого пилу, що містить луги в піч;
- попереднє очищення пило-газового потоку до контактування його з матеріалом у запічних теплообмінних пристроях.
Хімічний аналіз більшості клінкерів свідчить про вміст у них невеликих кількостей фосфорного ангідриду, що вноситься із вапняним компонентом, а також з деякими відходами промисловості. Вплив фосфорного ангідриду на процеси утворення мінералів носить двоїстий характер. У розплаві фосфор утримується у вигляді аніона РО43-. Оскільки Р+5 має сильні комплексоутворюючі властивості, у розплаві утворяться й аніони типу -Р-О-Р- і -Р-О-Si-О-Р-, до яких можуть приєднуватися й катіони. Такого роду ланцюжки й радикали характеризуються зниженою швидкістю дифузії, що трохи знижує рухливість інших іонів у розплаві. З іншого боку, невелика частка іонного зв'язку в комплексі знижує в'язкість розплаву. Переважна дія одного із цих факторів залежить від концентрації фосфору, температури й природи супутніх іонів. У більшості випадків зниження в'язкості не компенсує зниження рухливості іонів і тому швидкість і повнота засвоєння СаО при спіканні знижуються.
Але вирішальними факторами в зниженні швидкості утворення аліту є стабілізація β-С2S фосфорним ангідридом, що зменшує швидкість розчинення беліту в розплаві, і частковий розпад аліту присутності іона Р5+. Кожний відсоток Р2О5 зменшує кількість C3S на 9,9%, збільшуючи вміст С2S на 10,9%. Якщо Р2О5 утримується 7%, трикальцієвий силікат зовсім не утвориться.
При невисокому вмісті Р2О5 у клінкері (0,1—0,5%) хід реакції утворення аліту не порушується, а, навпаки, Р2О5 навіть впливає на процес випалу, викликаючи зниження температури початку утворення мінералів, прискорюючи синтез аліту в діапазоні температур 1100—1400°С, поліпшуючи здатність клінкеру розмелюватися. Встановлена можливість одержання швидкотвердіючого й високоміцного цементу в присутності 0,2—0,3% Р2О5. Вважають, що збільшення вмісту Р2О5 до 0,7—1 % ще не приводить до негативного впливу.
При подальшому збільшенні кількості фосфорного ангідриду змінюються умови формування кристалів аліту й беліту, на поверхні кристалів аліту з'являються тріщини, на гранях утворюються облямівки із СаО й вторинного беліту. Реакційна здатність суміші знижується в результаті негативного впливу фосфорного ангідриду на кристалічну решітку СаО й SiО2. Крім того, частина вапна витрачається на утворення високоосновних фосфатів і силікофосфатів, які утворюють із двокальцієвим силікатом тверді розчини, стабілізують його в гідравлічно менш активній формі.
При одночасному введенні Р2О5 і фтору у шихту сполуки, що містять фтор, майже повністю усувають негативний вплив фосфатів, зв'язуючи фосфорний ангідрид у фторапатит, що нормалізує процес утворення мінералів і дозволяє одержати цемент при високих значеннях КН. Тому, на думку деяких авторів, у присутності фтористих мінералізаторів вміст Р2О5 може бути підвищено до 2,5—2,8%. У промисловості вже були випробувані такі відходи й продукти, як фторапатит, фосфогипс, шлаки фосфорного виробництва, які виявилися активними мінералізаторами, що сприяють кращій кристалізації клінкеру, зниженню витрати палива, підвищенню продуктивності печей.
ТiО2 утримується в клінкері в кількості 0,2—0,5%. Іон Тi4+ за своїми електричними властивостями досить близький до Si4+, тому він досить легко замінює останній у сполуках.
Енергія взаємодії в розплаві Ti–О більше, ніж Si—O, тому титан у катіонній формі можуть деполімеризувати деякі комплекси, викликаючи зменшення в'язкості розплаву. У присутності 0,1—0,5% ТiО2 процеси утворення мінералів у значній мірі інтенсифікуються. Позитивний вплив ТiО2 проявляється в прискоренні й зниженні температури дисоціації СаСО3, інтенсифікації твердофазових реакцій, зниженні температури й в'язкості рідкої фази, збільшенні розчинності в соляній кислоті глинозему, отриманого прожарюванням каолініту при температурах 900—1000°С (тобто підвищується його активність). ТiО2 у невеликих кількостях поліпшує кристалізацію клінкерних мінералів, підвищує їхні гідравлічні властивості, тобто є легуючим оксидом. Однак більші кількості ТiО2 погіршують процеси утворення мінералів; ТiО2 утворить із СаО гідравлічно інертні або малоактивні сполуки СаО∙ТiО2 і ЗCаО∙2ТiО2; знижується також активність беліту й аліту. Спостерігається саме розсипання «спеків», розрахованих на одержання аліту в присутності 3% ТiО2.
Оксиди марганцю спектральним аналізом виявляються в клінкерах більшості заводів. Особливо велика їхня кількість, що піддається хіміко-аналітичному визначенню, утримується в клінкерах тих заводів, які у якості сировинного компоненту застосовують доменні шлаки. Оксиди марганцю (1,5—2% і навіть до 3%), як і оксиди заліза, позитивно впливають на процеси утворення мінералів і прискорюють їх. Завдяки значному зниженню в'язкості клінкерного розплаву в присутності оксидів марганцю прискорюються твердо-фазові реакції (починаючи з 900°С). Марганець має більший, ніж залізо, негативний заряд і здатний заміщати залізо в його сполуках. При цьому утворяться тверді розчини в системі С4АF—С4АМ. Вважають, що гранична границя цих твердих розчинів характеризується формулою 4СаО·А12О3∙(0,4Fе2О3∙0,6Мn2О3). При використанні доменних шлаків у вигляді сировинного компонента найбільш сприятливим є вміст рівних кількостей Fе2О3 і Мn2O3 (близько 3%). При значному збільшенні Мn2О3 різко зменшується інтервал плавкості гартованого матеріалу, у той же час при використанні шихт, що легко спікаються, рекомендується вводити коригувальні добавки, що містять оксид марганцю, які викликають часткову кристалізацію розплаву. Марганець може стабілізувати β-2СаО∙SiО2, розчинність Мn2О3 в β-С2S доходить до 4%, а в С3S — усього до 0,5%. У присутності оксидів марганцю зменшується кількість вільного МgО, тому що частина його розчиняється в силікатах і алюмоферитах. При вмісті Мn2O3 більше 4%, у печі можуть утворитися свари й кільця. Знижується також і гідравлічна активність клінкеру.
Таким чином, у невеликих кількостях (до 1—2%) оксид марганцю є мінералізатором і легуючою добавкою, що поліпшує процеси утворення мінералів і структуру клінкеру. Перевищення вмісту Мn2O3 понад 3% небажане.
Сr2O3 у невеликих кількостях (до 0,2—0,5%) є мінералізатором по силі меншим, ніж плавиковий шпат. Він прискорює твердо-фазні реакції, знижує в'язкість розплаву, сприяє формуванню оптимальної кристалічної структури аліту, здійснює стабілізуючу дію на β-С2S, зменшує кількість вільної МgО в суміші. При вмісті 0,2—0,3% Сr2O3 у клінкері збільшується його гідравлічна активність. Однак у кількості 2—3% Сr2О3 робить гальмуючу дію на процес утворення аліту. Вважається, що граничний вміст Сr2O3 у С3S становить приблизно 2%. При більшому його вмісті відбувається розпад С3S на СаО й С2S або навіть СS.
ВаО в невеликих кількостях служить легуючою добавкою й мінералізатором. Карбонат барію вступає в реакцію із кремнеземом при температурах 735—775° С з утворенням двобарієвого, а вище 1050°С — трибарієвого силікату. Сульфат барію, навпаки, не приймає участі в реакціях утворення мінералів аж до повного розкладання СаСО3. Потім починається взаємодія ВаSO4 і С2S з утворенням твердого розчину. У присутності невеликих кількостей (0,5—0,9%) ВаО знижується в'язкість розплаву, що прискорює утворення С3S. Але при збільшенні дозування ВаО в'язкість підвищується, утвориться менше С3S. Активність ВаО як мінералізатора значно нижче активності таких оксидів, як Сr2О3, Мn2О3, ТiО2, Fе2О3. Більш активно діє ВаО в складі комплексного мінералізатора. Активність портландцементу помітно підвищується при оптимальній добавці ВаО. Крім того, цемент здобуває деякі спеціальні властивості - підвищену сульфатостійкість, вогнетривкість і опірність проникненню рентгенівських променів.
SrО, як і ВаО, у кількостях 0,1—0,3% трохи інтенсифікує процеси утворення мінералів, при більшому дозуванні спостерігається розпад С3S з утворенням вільного СаО й стронцій кальцієвого твердого розчину з основністю 2—2,3. Стронцій, як і барій, може утворювати двох- і тристронцієві силікати, які мають гідравлічні властивості, однак твердіють повільніше своїх кальцієвих аналогів.
Інші домішки. За даними спектрального аналізу, у сировині для портландцементу можна виявити цілий ряд елементів, які, однак, утримуються в таких кількостях, що не можуть утворювати самостійні фази, але все-таки впливають на процеси утворення мінералів і на тонку структуру цементних мінералів. Роль багатьох з них ще повністю не з'ясована, але про деякі уже є короткі відомості. Так, установлений позитивний вплив Li2O на процеси утворення силікатів кальцію, особливо при реакціях у твердих фазах.
Дисоціація СаСО3 прискорюється в присутності 0,1— 0,2% Li2О. Сполуки цинку також є активними мінералізаторами. Знижує в'язкість і збільшує кількість рідкої фази СuО. СdО прискорює процеси утворення мінералів, діючи як поверхнево-активна речовина. Борний ангідрид прискорює утворення С3А, є класичним стабілізатором β-С2S, але внаслідок цього гальмує утворення С3S. Багато оксидів (Мо3О3, V3О5, NiО, Lа2О3) у невеликих кількостях позитивно впливають на гідравлічну активність цементу. Особливий вплив роблять домішкові оксиди на кольори клінкеру.
Вивчення впливу окремих оксидів на процеси утворення клінкеру має в цей час велике практичне значення, тому що з кожним роком розширюється сировинна база за рахунок більш широкого застосування як сировинних компонентів відходів металургійної й хіміко-металургійної промисловості.
Вплив швидкості нагрівання на процеси утворення
клінкеру.
Швидкість випалу впливає на процеси утворення клінкеру. При швидкому випалі, який триває кілька хвилин, на зв'язування вапна сприятливо позначається одночасність реакцій розкладання карбонатів, розпаду каолінітового ядра з реакціями утворення силікатів. При цьому в реакціях беруть участь компоненти з порушеною кристалічною решіткою, що сприяє проходженню реакцій у твердій фазі. Іншою особливістю швидкого випалу є поява нерівновагих рідких фаз.
При повільному нагріванні сировини вапно частково встигає рекристалізуватися, що спричиняє гальмування реакцій утворення клінкеру у твердій фазі. У період спікання контролюючим фактором є швидкість розчинення СаО й С2S у розплаві. Рекристалізоване вапно й великі зрослі кристали С2S, які утворюються при повільному нагріванні, розчиняються повільніше. Отже, для прискорення реакцій у зоні спікання необхідно створювати такі умови, при яких би скорочувався час перебування матеріалу в зоні кальцинування.
На властивості й кристалізацію основних клінкерних мінералів дуже впливає довжина зони спікання і її близькість до обріза печі. У більше коротких печах, зона спікання яких не розтягнута, легше одержати високоміцний і швидкотвердіючий цемент, ніж у сучасних довгих печах, де зона спікання значно довше й теплове напруження вище, а оскільки швидкість просування матеріалу в печі не змінилася, тривалість перебування цементу в зоні спікання збільшилася. Тому в довгих печах рекомендується наближати зону спікання до обрізу печі, що підвищує якість цементу.
Рентгенографічні дослідження швидко і повільно обпалених клінкерів показують, що у швидко обпаленому клінкері концентрація дефектів у полікристалах аліту значно вище, ніж у повільно обпаленому, що є причиною більшої гідравлічної активності цементу на його основі.
Велике значення має також температура випалу. При високих температурах прискорюється процес синтезу аліту, різко знижується в'язкість рідкої фази, збільшується її кількість. Ці фактори повинні впливати на процеси одержання плавлених цементів. Установлено, що при 1600°С реакції утворення мінералів у сировинній суміші закінчуються за 5—10 хв, при 1700— 1800°С - за кілька секунд, а в інтервалі 1900—2000°С — за частки секунди. При цьому прискорюється також і ріст кристалів. Так, при температурі 1900—2000°С за кілька секунд розміри кристала аліту можуть досягти 2—3 мм, тоді як при звичайних температурах вони не перевищують 20—40 мкм. При температурах 1800—2000°С такі мінерали, як С3S і С3А є нестійкими, тому швидкість охолодження плавлених клінкерів повинна бути менше, ніж швидкість охолодження звичайних клінкерів, що забезпечує здійснення повторного синтезу цих мінералів.
Суттєвий вплив на процеси утворення клінкеру здійснює також і вид палива. При використанні твердого палива окремі фази цементного клінкеру не мають чітких обрисів, середній розмір кристалів аліту й беліту становить відповідно 65 і 55 мкм, тоді як випал тієї ж шихти на рідкому й газоподібному паливі приводить до чіткої кристалізації мінералів і значному (до 45—30 мкм) зменшенню розмірів кристалів.
Міцність цементу при цьому зростає на 60—80 кгс/см2 в усі строки твердіння.
