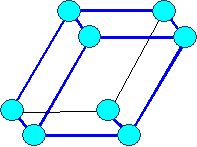
Описание кристаллического вещества
Для описания дальнего порядка вводится понятие кристаллической решетки. В положении термодинамического равновесия атомы, ионы, молекулы, образующие кристалл, располагаются в узлах кристаллической решетки. Кристаллы подразделяются на атомные (Al, Fe,..), ионные (Mg O, Na Cl) и молекулярные (СН4 твердая).
Структура кристалла воспроизводится транслированием элементарной решетки, которая называется решеткой БРАВЭ.
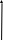


 z
b
z
b
а
a
с
у
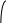
b g
X Рис. Элементарная ячейка
a, b, c - ребра ячейки (постоянные решетки), a, b, g - углы между ребрами.
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
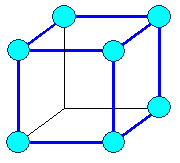
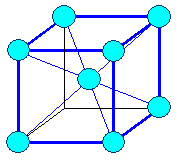
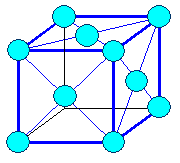
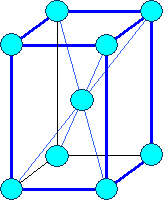
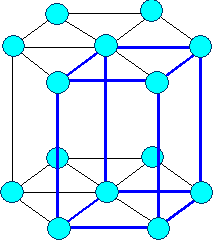
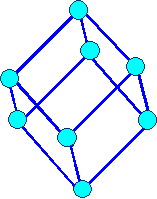
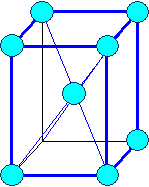
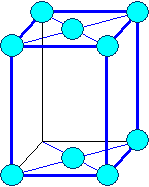
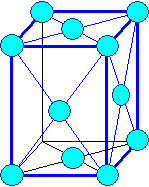
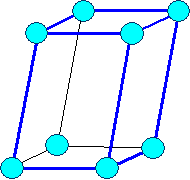
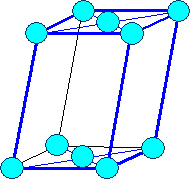
Элемeнты могут располагаться как в вершинах ячейки, так и в пересечении пространственных диагоналей (объемоцентрированная решетка) или в пересечениях диагоналей граней (гранецентрированная решетка).
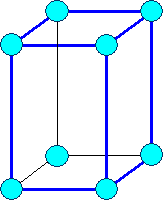
В соответствии с внутренней структурой кристаллы объединяются в 14 систем (сингоний), отличающихся соотношением длин ребер и углов.
Тип кристаллической решетки зависит:
- соотношения размеров катионов и анионов – координационного числа,
- внешних воздействий: температуры давления, деформации и т.п.