
- •8.1. Цілі і принципи
- •8.1.1. Вимоги до якості кінцевого продукту
- •Пари та рідини
- •8.1.3. Розділення як функція енергії
- •8.1.2. Співвідношення матеріального балансу
- •8.2. Регулювання якості продукту
- •8.2.1. Регулювання виходу основного продукту, споживання енергії і якості кінцевого продукту
- •8.2.2. Регулювання за збуренням
- •8.2.3. Зворотній зв'язок за якістю продукту
- •Виходу процесу в залежності від складу.
8.1.2. Співвідношення матеріального балансу
Як і в будь-якому іншому процесі, в дистиляції теж існує співвідношення між якістю і кількістю продукту, яке часто не враховують при проектуванні систем регулювання.
Загальний матеріальний баланс можна записати у вигляді
![]()
де F - масова або молярна витрата початкової сировини, a D і В - відповідно витрати дистиляту і залишкових продуктів. Один з цих трьох потоків може бути використаний для регулювання якості кінцевого продукту, інший - для визначення його кількості, а третій - для підведення балансу.
Подібним чином матеріальний баланс можна записати для будь-якого компоненту і:
![]()
де zі уі та Xі - масові або мольні долі компоненту і у відповідному потоці. При об'єднанні рівнянь (8.1) та (8.2) склад кінцевого продукту є пов'язаний співвідношеннями витрат

Розділення s визначається як відношення концентрацій легкої і важкої фракцій в кінцевому продукті, що поділене на таке ж відношення в залишковому продукті
![]()
Об'єднуючи рівняння (8.6) і (8.3), записані спочатку для легкої фракції /, а потім для важкої фракції h, можна знайти розв'язок рівняння для чотирьох варіантів складу, що входять в рівняння (8.6). Рішення припускає що в залишковому продукті не міститься компонентів легших за легку фракцію, а в дистиляті не міститься компонентів важчих за важку фракцію. Результат має вид квадратного кореня рівняння:

Нижні індекси ll та h позначають всі компоненти, які легші за легку фракцію і важчі за важку фракцію відповідно.
Приклад 8.1. Депропанізатор має наступний склад початкових і кінцевих продуктів в мольному представленні:
Вихідна сировина Дистилят Кінцевий
z у продукгх
Етан та більш легкі фракціїll 0,0097 0,030
Пропанl 0.310 0,950 0,002
Ізобутан h 0,088 0,020 0,120
Н-бутан та більш важкі фракції hh 0,593 - 0,878
Знайти D/F і розділення. Визначити вплив, що викличе збільшення D/F на 0,01 на значення уh


У роботі 1, с.43—45 отримано співвідношення між коефіцієнтом розділення s та середнім відношенням витрати пари до витрати вихідної сировини V/F в колоні
![]()
де![]() -
так званий характеристичний чинник
колони. Він є функцією відносної
леткості5
-
так званий характеристичний чинник
колони. Він є функцією відносної
леткості5![]() основних
компонентів, числа ступенів розділення
в колоні п
та
їх загального
к.к.д. Е
основних
компонентів, числа ступенів розділення
в колоні п
та
їх загального
к.к.д. Е
![]()
Область застосування цього співвідношення обмежують два основні чинники. Логарифмічна модель дійсна лише в області значень
![]()
Проте це обмеження не є серйозною перешкодою для застосування співвідношення (8.10), оскільки майже всі колони працюють саме в цій області.
Друге обмеження полягає в тому, що це співвідношення не містить члена, що враховував би склад вихідної сировини. Проте для виправлення цього недоліку можна ввести коректуючий коефіцієнт, що враховує, згідно рівняння (1.20), вплив складу на зміну ентропії. Було виведено співвідношення для розділення еквімолярних бінарних сумішей6, які мають ентропію змішування 5,76 R кДж / (кмоль • °С), де R = 8,3144 кДж / (кмоль • °С) - універсальна газова постійна. Нехай вихідна сировина, що подається в колону, є бінарною сумішшю, яка містить легку основну фракцію і всі більш легкі компоненти, а також важку основну фракцію і всі більш важкі компоненти. Тоді величина V/F при розрахунку за рівнянням (8.9) може бути скоректована співвідношенням Cz ентропії псевдобінарної суміші вихідної сировини до ентропії суміші з 50% легких та 50% важких компонентів:
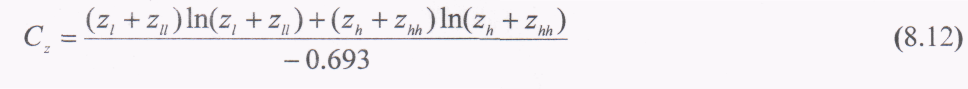
Л еткий
компонент - це такий компонент суміші,
який має найбільшу пружність парів при
даній температурі
в порівнянні з пружністю парів будь-якого
іншого компонента суміші. Леткий
компонент
має найменшу температуру кипіння. Важко
леткий компонент має найвищу температуру
кипіння.
Відносна
леткість компонентів визначається
відношенням пружності парів чистого
леткого компонента
(А) до пружності парів чистого компонента
(В), шо відібрані для порівняння при
однаковій
температурі
еткий
компонент - це такий компонент суміші,
який має найбільшу пружність парів при
даній температурі
в порівнянні з пружністю парів будь-якого
іншого компонента суміші. Леткий
компонент
має найменшу температуру кипіння. Важко
леткий компонент має найвищу температуру
кипіння.
Відносна
леткість компонентів визначається
відношенням пружності парів чистого
леткого компонента
(А) до пружності парів чистого компонента
(В), шо відібрані для порівняння при
однаковій
температурі
Еквімолярні бінарні суміші - суміші, що складаються із двох компонентів, при умові, що мольні концентрації цих компонентів у суміші однакові
Приклад 8.2. Знайти коефіцієнт для корекції співвідношення V/F. Склад початкової суміші вказаний в прикладі 8.1.

Рівняння (8.9) можна застосовувати навіть тоді, коли значення а і Е невідомі або неоднорідні по колоні. Для оцінки значення може бути використаний комплекс умов за даними колон, що працюють або тих, які точно змодельовані. За отриманим значенням можна знайти нові значення V/F при зміні умов.
Приклад 8.3. Колона в прикладі 8.1 має V/F = 1,60. Знайти можливе процентне зниження величини V/F, якщо вміст пропана в залишковому продукті зростає до 0,3%-
За рівнянням (8.9)
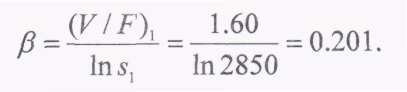
Новий коефіцієнт розділення рівний
![]()
і нове відношення V/F рівне
![]()
Це означає зниження значення V/F на 5,1%.
Енергія Q, необхідна для розділення, прямо пропорційна витраті пари V:
![]()
де Hv - прихована теплота пароутворення7 середньої суміші в колоні.
Одним з найбільш цінних застосувань цієї взаємозалежності енергії та розділення є прогноз економії енергії шляхом підвищення відносної леткості компонентів. Відносна леткість більшості сумішей зростає з пониженням температури і тиску. Якщо значення а відоме для різних умов, то рівняння (8.10) можна використовувати для оцінки відповідних змін V/F. Для перетворення V/F в Q/F при змінах Hv залежно від температури необхідно вводити коефіцієнт для корекції.
Прихована теплота пароутворення - це та кількість теплоти (енергії), яку поглинає одиниця маси чи об'єму рідини при переході від рідини до пари, чи навпаки виділяє, при переході від пари до сконденсованої рідини. Залежність від температури та тиску обернено пропорційна.
Приклад 8.4. Відносна леткість пропану та ізобутану в колоні, описаній в попередніх прикладах, рівна 2,01 при 49 °С та 2,33 при 26,7 °С. Теплота пароутворення при цих температурах складає 201,75 і 235,55 кДж/л відповідно. Визначити процентний вміст споживаної енергії при роботі з нижчою температурою. Вирішення:

тобто досягається зниження споживаної енергії на 25%. 8.1.4. Ентропійний аналіз
Аналіз ефективності роботи такого устаткування для перетворення енергії, як парогенератори і компресори, достатньо легкий. Зовсім не так все відбувається в процесах масообміну, в яких енергія використовується без відтворення. У цих процесах ентропійний вміст енергії йде на розділення суміші початкових продуктів і, отже, на зниження її ентропії.
Для ілюстрації виконаємо ентропійний аналіз роботи колони, що розділяє суміш, що складається на 50% з пропану і на 50% - з пропилену. Ці компоненти вибрані тому, що вони мають близькі температурні межі кипіння, через це розділення стає важким завданням, проте допускає широкий вибір джерел енергії, включаючи тепловий насос.
Розглянемо колону з 130 ідеальними тарілками, що розділяють початкову суміш на два продукти, кожен з яких має чистоту 99%. їх відносна леткість при температурі 26,7 °С складає 1,15, а прихована теплота паротворення в середньому рівна 8606 кДж/кмоль. Тоді
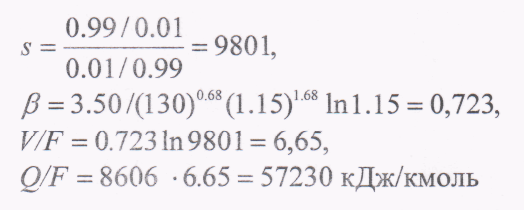
Колона нагрівається парою, що має температуру 100 °С, і охолоджується водою, температура якої, як показано на рис 8,3, рівна 21,11°С. Ентропія початкової сировини і кінцевих продуктів розраховувалася за рівнянням (1.20), а газова постійна R була прийнята рівною 8,3144 кДж/(кмоль • °С):
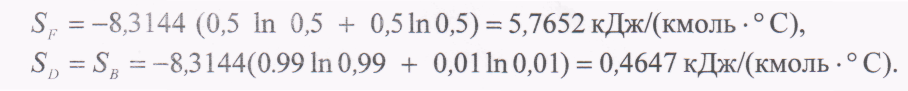
Зміна ентропії компонентів на 1 кмоль початкової сировини рівна
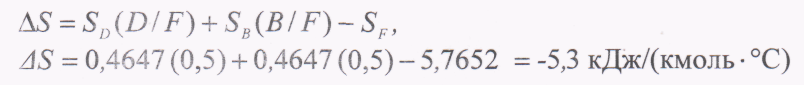
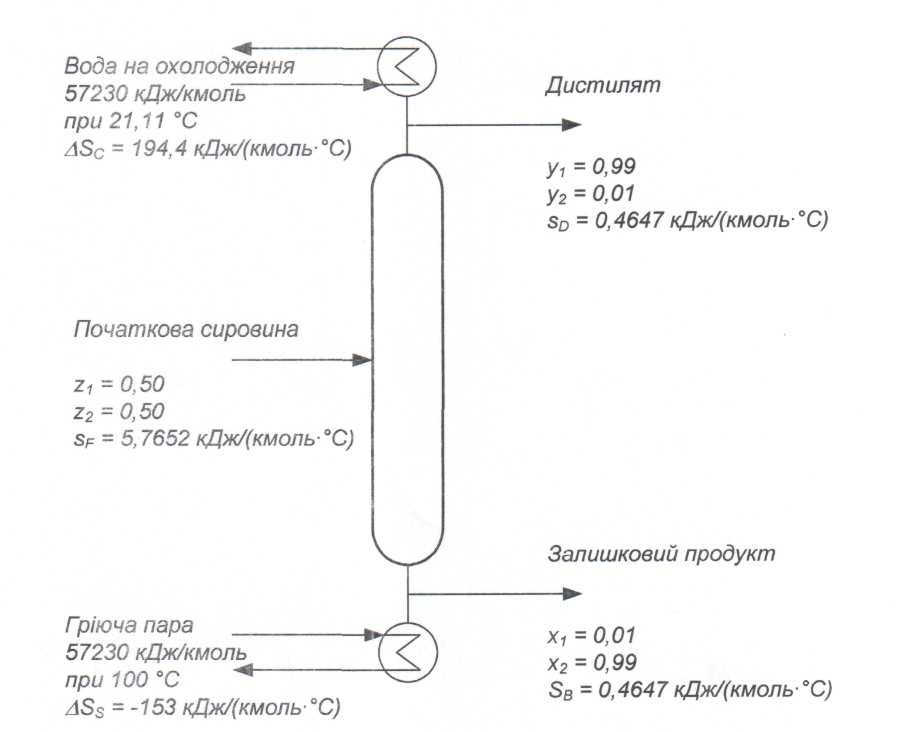
Рис. 8. 3. Чистий приріст ентропії оточуючого середовища в декілька разів більший за зниження ентропії компонентів, що розділяються.
В процесі перенесення 57230 кДж/кмоль початкової сировини при 100 °С ентропія гріючої пари, згідно рівняння (1.32), знижується на

Якщо вода, що подається для охолодження процесу, тече так швидко, що її температура підвищується незначно, то та ж залежність може бути використана для оцінки приросту ентропії
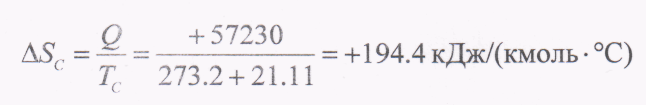
Чистий приріст ентропії системи нагріву і охолодження, що показана на рис. 8. З, становить 194,4 - 153,4 = 4 1 кДж/(кмоль • °С), порівняно із зниженням ентропії компонентів 5,3 кДж/(кмоль • °С), що розділяються.
Якби рідина, що подається для охолодження, використовувалась для повторного випаровування, то операція була б ефективнішою в тому сенсі, що приріст ентропії був би менший. Такі міркування правомірно застосувати до тих меж, поки різниця температур між нагрітою і холодною рідинами не наблизиться до різниці температур кипіння кінцевих продуктів. Різниця їх
температур кипіння складає 8,9°С. Збільшення ентропії при перенесенні 57 230 кДж/кг в умовах зміни температури від 30 до 21,11 °С становить

Отже, навіть в тих випадках, коли не враховується різниця температур на теплообмінних поверхнях або в середовищі, яке передає тепло, а також не розглядається перепад тиску в колоні, чистий приріст ентропії все ще має місце.
