Розділ 4 Системи регулювання процесів в компресорах
Значна частина енергії1, що споживається при очистці нафти і хімічній переробці, витрачається на приведення в дію компресорів, що забезпечують стислими газами реактори і забезпечують охолоджування або транспортування газоподібних продуктів. Оскільки на стиснення газів зазвичай витрачається механічна енергія, її економія має особливе значення. Єдиними компресорами, не споживаючими механічної енергії, є ежектори, що створюють розрідження або забезпечують невисоке стиснення пари. Вони, природно, також розглядаються в даному розділі, оскільки використовуються як компресори і працюють за рахунок енергії пари.
Термодинамічні принципи стиснення однакові для компресорів всіх типів, у тому числі і пароструминних ежекторів2. Тому в цьому розділі для аналізу характеристик компресорів окремих типів розглядається термодинаміка процесу стиснення. Потім розглядаються потреби технологічних процесів, в яких використовуються компресори, і обговорюється застосування систем регулювання витрати і тиску в компресорах.
Особлива увага приділена турбокомпресорам, оскільки вони знаходять широке застосування для стиснення великих об'ємів газів. Системи регулювання повинні спеціально розроблятися для кожної установки з метою зведення до мінімуму споживання енергії, а також захисту компресора і його приводу від несприятливих робочих умов. Ці системи можуть виявитися досить складними при великому числі компресорів або при великому числі потоків від одного багатоступінчатого компресора.
4.1. Термодинаміка процесу стиснення
Хоча політропне3 стиснення обговорювалося в розділі 1, розглянуті вище закони термодинаміки необхідно досліджувати детальніше, щоб оцінити вплив регулюючих дій на роботу компресора і процес стиснення. З метою визначення параметрів процесу і оцінки коефіцієнтів корисної дії спочатку розглядається стиснення ідеального газу . Отримані співвідношення застосовуються потім до реальних газів і газових сумішей.
1 Енергія (від грец. evspyoc - діяльний) — загальна кількісна міра руху і взаємодії всіх видів матерії. Енергія не виникає ні з чого і нікуди не зникає, вона може тільки переходити з одного вигляду в ініший (закон_збереження_енергії). Поняття енергії зв'язує всі явища природи в одне ціле, є загальною характеристикою стану фізичних тіл і фізичних полів.
Федорченко A.M.. Теоретична механіка (1975), Київ: Вища школа., 516 с.
Федорченко A.M.. Теоретична фізика. Квантова механіка, термодинаміка і статистична фізика. Т.2. (1993), Київ: Вища школа., 415 с.
2 Ежектор (англ. ejector, нім. Ejektor) — струминний насос для відсмоктування (при значному розрідженні) рідин, газів, пари або сипких мас за рахунок передачі кінетичноі_енергії від робочого середовища (що рухається) до відсмоктувального. Дія ежектора грунтується на розрідженні, що створюється у ньому струминою іншої рідини (пари, газу), котра швидко рухається.
Мала_гірнича_енциклопедія: В 3-х т. / За ред. B.C. Білецького. — Донецьк: «Донбас», 2004.
3 Політропний процес — термодинамічний процес, під час якого питома теплоємність газу залишається незмінною.
4 Ідеальний газ (рос. ідеальний газ; англ. ideal gas, нім. ideales Gas n) — це газ, в якому молекули можна вважати матеріальними_точками, а силами притягання й відштовхування між молекулами можна знехтувати. У природі такого газу не існує, але близькимиза властивостями до ідеального газу є реальні розріджені гази, тиск в яких не перевищує 200 атмосфер і які перебувають при не дуже низькій температурі, оскільки за таких умов відстань між молекулами набагато перевищує їх розміри.
Федорченко A.M.. Теоретична фізика. Квантова механіка, термодинаміка і статистична фізика. Т.2. (1993), Київ: Вища школа., 415 с. Ландау Л.Д., Лившиц Е.М.. Теоретическая физика. т. V. Статистическая физика. Часть 1. (1976), Москва: Наука..
_
4.1.1. Адіабатичне стиснення ідеального газу
У разі ізотермічного стиснення ідеального газу добуток тиску на об'єм однаковий в початковому і кінцевому станах
![]()
де р - абсолютний тиск, Q - об'ємна витрата, G - масова витрата, R - універсальна газова стала, Т - абсолютна температура, М - молекулярна маса газу. Проте в більшості компресорів ізотермічні умови5 не можна підтримувати через відсутність достатньої поверхні теплообміну: вірогідніше наближення до адіабатичних умов. Якщо процес стиснення є оборотним (політропним), то показник ступеня в рівнянні, що зв'язує об'єм і тиск зростає від одиниці (у ізотермічних умовах) до величини, рівної відношенню питомих теплоємностей газу:
![]()
![]() -
відношення питомої теплоємності при
постійному тиску до питомої
-
відношення питомої теплоємності при
постійному тиску до питомої
теплоємності6 при постійному об'ємі. Відношення абсолютних температур газів, що нагнітаються, і всмоктуваного пов'язане зі ступенем стиснення співвідношенням:
![]()
При![]() адіабатичному7
стисненні майже вся енергія, що
підводиться,
адіабатичному7
стисненні майже вся енергія, що
підводиться,
Q
витрачається на збільшення ентальпії рідини навіть в необоротному процесі. Нехай W - потужність, що підводиться до потоку, a G - масова витрата рідини. Тоді:

де С
-
питома теплоємність рідини і Т
-
її температура. Потужність, що підводиться,
можна
також представити як відношення добутку
масової витрати і «адіабатичного тиску»
на![]() -
параметр, зазвичай використовуваного
виготовлювачами
-
параметр, зазвичай використовуваного
виготовлювачами
компресорів:
де
адіабатичний ККД![]() ,
показує
,
показує![]() на
те, що не вся потужність9
перетвориться в тиск.
на
те, що не вся потужність9
перетвориться в тиск.
Якщо витрата виражається в кг/с і натиск в кДж/кг, то потужність матиме розмірність кВт.
5 Ізотермічні
умови-умови
за яких температура залишається сталою.
Ізотермічні
умови-умови
за яких температура залишається сталою.
6 Питома теплоємність (позначення - с) - характеристика речовини, яка вказує скільки теплоти необхідно щоб нагріти (або виділяється при охолодженні) 1 кг речовини на 1°С
7 Адіабатний процес (грец abiaficcwc; — неперехідний) — в термодинаміці зміна стану тіла без обміну теплом з навколиіінім середовищем. Його можна здійснити, проводячи стискання чи розширення тіла (наприклад, газу) дуже швидко.
8 Ентальпія (або теплова функція, від грец. enthalpo — «нагріваю») — термодинамічний_потенціал, що характеризує стан термодинамічної системи.
Ландау Л.Д., Лившиц Е.М.. Теоретическая физика. т. Ш. Квантовая механика. Нерелятивистская теория. (1974), Москва: Наука..
9 Потужність - робота, виконана за одиницю часу, або енергія, передана за одиницю часу.
Адіабатичний тиск можна розрахувати за підвищенням температури:

Ентальпія ідеального газу не залежить від тиску, і, отже, питома теплоємність в рівняннях (4.4) і (4.6) представляє питому теплоємність при постійному тиску Ср.
При підвищеннях температури, які зазвичай мають місце в процесі стиснення, Ср
можна
вважати постійною величиною, і в цьому
випадку рівняння (4.6) приймає вигляд:![]()
Використовуючи співвідношення
![]()
і
замінюючи відношення температур
відношенням тиску, згідно з рівнянням
(4.3), адіабатичний тиск можна виразити
через степінь стиснення р2
/р1
при
ККД, рівному
100%![]()
У табл. 4.1 (для звичайних газів) наведені значення молекулярної маси і функцій у і φ. Для парафінового ряду та їх сумішей існує достатньо характерна залежність між цими функціями і молекулярною масою. Криві, що ілюструють цю залежність, наведені на рис. 4.1.
Таблиця 4.1 Молекулярні маси і функції відношення питомих теплоємностей для звичайних газів
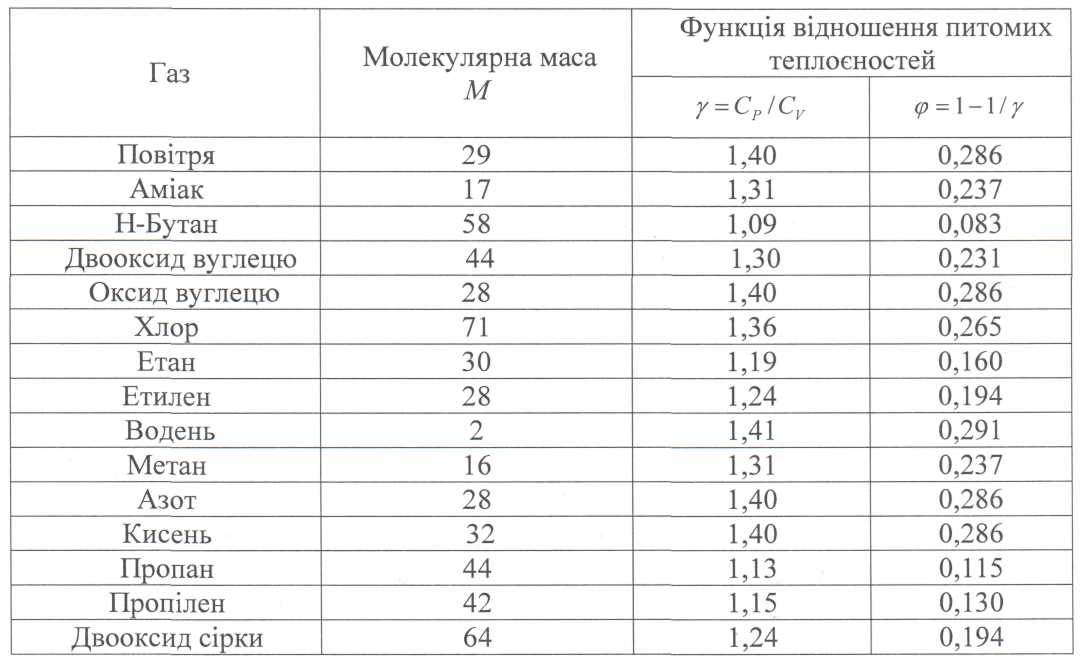
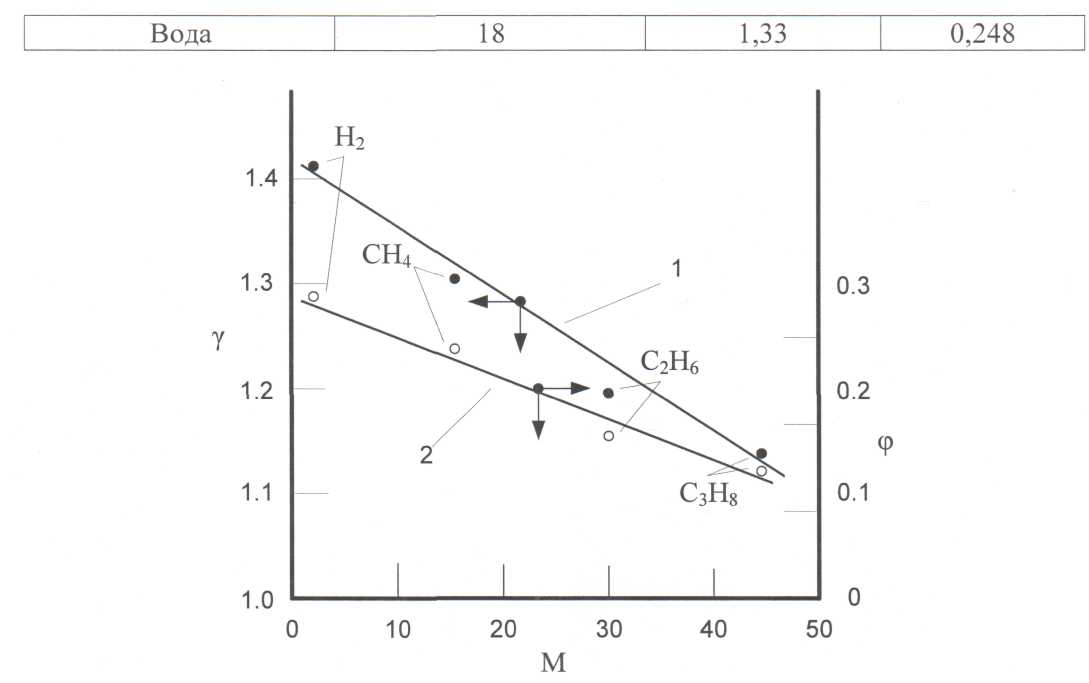
Рис.
4.1. Графік залежності функцій![]() від
молекулярної маси М
від
молекулярної маси М
— лінія точок залежності функції
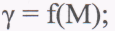
- лінія точок залежності функції