
1 Огляд наукової літератури
1.1 Циклічна система хіноліну
Хінолін (1 – аза нафталін або бензо[b]піридин) є одним з можливих азонафталінів (рис. 1.1). Безбарвна рідина з запахом піридину, яка на вологому повітрі жовтіє. tпл = -15 ºС; tкип = 237 ºС при 108,8/10 мм.рт.ст.; d204 = 1,09. Добре розчиняється в етанолі, хлороформі, діетиловому ефірі та бензолі, мало розчиняється в воді (0,7% при 20 ºС), гігроскопічний (захоплює до 22% води), перегоняється з водяним паром [1 – 5].
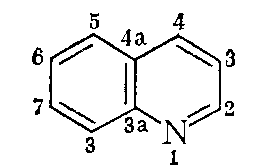
Рисунок 1.1 – Структура хіноліну
Біциклічна структура хіноліну, яка подібна до стуктури нафталіну, була запропонована Кьорнером.
Фізико – хімічні константи для хіноліну [5].
1.2 Хромато – мас – спектрометрія
Обігриваєма система вводу проби. Леткі рідини можна вводити через мембрану в невеликий обігріваємий резервуар, в якому підтримується тиск досліджуваної рідини близько 10-2 мм. рт. ст. За допомогою скляного капіляру резервуар з’єднують з іонним джерелом, тиск в якому складає приблизно 10-6 мм. рт. ст.
Іони, які утворюються як було описано раніше, можна далі розділити згідно відношенням їх маси до заряду (m/z) в магнітному та (або) електричному полях (використовуються таблиці). В мас – спектрометрі з одинарною фокусировкою заряджені частки спочатку прискорюються в сильному електричному полі з прискорюючою напругою V та потім поступають в магнітне поле В (в магнітний сектор приладу), де їх рух по дузі з радіусом r описується рівнянням [8].
m / z = B2 r2 / 2V (1.1)
Для реєстрації спектрів використовують класичні спектрометри та Фур’є – спектрометри (останні розглянуті в наступному підрозділі). Основні частини класичного спектрометру: джерело безперервного теплового випромінювання, монохроматор, неселективний приймач випромінювання.
2 Матеріали і методи дослідження
2.1 Синтез вихідних речовин
Вихідною речовиною для синтезу нових похідних L-цистеїну та ацетил цистеїну є 9-хлоракридин (рис. 2.1):

Рисунок 2.1 – Структура 9-хлоракридину
У свою чергу, вихідними речовинами для отримання 9-хлоракридину є N-фенілантранілові кислоти.
Реакція полягає в арилюванні антранілової кислоти відповідними заміщеними бромбензолу або хлорбензолу, що показано на рис. 2.2.

Рисунок 2.2 – Арилювання антранілової кислоти
2.3 Визначення чутливості досліджуваних сполук
Чутливість аналітичної реакції визначається певною можливістю виявити речовину (або йона в розчині).
Мінімальна концентрація розчину:
Сmin = m (речовини)/ V (розчину) (2.1)
Відкриваємий мінімум:
m = Сmin∙ Vmin ∙106 (мкг) (2.2)
Реакція тим чутливіша, чим менше її відкриваємий мінімум [27, 28].
Готуємо 0,1н розчин FeCl3∙6H2O.
Готуємо 0,02н розчин СuCl2∙6H2O;
Для визначення готуємо розчин, 5 см3 якого містить 0,01 г досліджуваної сполуки. Реакцію проводимо краплинним методом. Далі проводимо розведення доти, доки ще можливо виявити йони досліджуваної сполуки.
На предметне скло наносимо 2 краплини досліджуваої солуки та 1 краплину СuCl2∙6H2O (FeCl3∙6H2O). Очікуємо забарвлений яскраво – синій комплекс міді (ІІ) (яскраво – жовтий комплекс заліза (ІІ)).
При проведенні досліду очікуваного забарвлення не спостерігалось. Жодна з трьох основ не дала комплексу. Тому, слід зробити висновок про те, що дослідження цих сполук з позиції комплексоутворення є неперспективним, пояснення цього дав фізико – хімічний аналіз.
