
- •Минобрнауки россии
- •305040, Г. Курск, ул. 50 лет Октября, 94. Оглавление
- •Раздел 3. Квантовая физика и физика атома 5
- •Раздел 4. Ядерная физика и физика элементарных частиц 45
- •Раздел 3. Квантовая физика и физика атома
- •3.1. Корпускулярно-волновой дуализм свойств частиц. Волны де Бройля. Принцип неопределённостей Гейзенберга
- •3.1.1. Соотношение неопределенностей
- •Примеры решения задач
- •3.2. Уравнение Шрёдингера
- •3.3. Простейшие задачи квантовой механики
- •3.3.1. Прохождение частиц через потенциальный барьер
- •3.3.2. Движение частиц в одномерной яме с абсолютно непроницаемыми стенками
- •3.4. Спектр атома водорода. Правила отбора. Теория Бора для водородоподобных систем
- •3.5. Модель атома водорода Бора
- •3.6. Квантовомеханическая модель атома водорода
- •3.7. Векторная модель атома
- •Принцип запрета Паули
- •Если учесть наличие спина у электрона, то .
- •Раздел 4. Ядерная физика и физика элементарных частиц
- •4.1. Радиоактивность. Состав атомных ядер.
- •4.2. Превращение атомных ядер
- •4.2.1. Законы радиоактивного распада
- •4.2.2. Активность радиоактивного вещества
- •4.3. Ядерные реакции. Элементарные частицы
- •4.3.1. Искусственная радиоактивность, ядерные реакции
- •4.3.1. Законы сохранения в ядерных реакциях
- •4.3.2. Основные характеристики элементарных частиц
- •4.3.3. Изотопический спин
3.6. Квантовомеханическая модель атома водорода
Квантовая физика дает для атома водорода такое же решение для значений энергии атома, что и теория Бора, но она боле последовательна и описывает не только излучение атома водорода.
Стационарное уравнение Шредингера для атома водорода имеет вид:
![]()
Решения этого уравнения для любого положительного значения энергии соответствует пролету электрона около ядра и удалению в бесконечность, что не соответствует определению атома, как динамически устойчивой системы.
Решения, соответствующие дискретным отрицательным значениям энергии, равной
![]() ,
n
= 1,2,3,…
,
n
= 1,2,3,…
соответствуют электрону, связанному с ядром.
При
n
= 1 получим значения энергии в основном
состоянии атома водорода
![]() эВ.
эВ.
Так как электрон в атоме водорода движется в центрально-симметричном поле ядра, то оператор Лапласа и собственные волновые функции удобно записывать в сферической системе координат
![]() .
.
Собственные волновые функции содержат 3 целочисленных параметров n, l, mℓ , которые называются квантовыми числами.
Число n – главное квантовое число. Оно определяет уровни энергии электрона в атоме.
ℓ – азимутальное
или орбитальное квантовое число, оно
определяет модуль орбитального момента
импульса
![]() ).
).
mℓ – магнитное квантовое число, оно определяет проекцию орбитального момента импульса на некоторое направление z, определяемое внешним магнитным полем)
![]() .
.
n = 1, 2, 3,…. При данном n ℓ = 0, ±1, ±2, ±3, … ±(n – 1).
При данных n и ℓ mℓ = 0, 1, 2, …, ℓ.
Энергетическое состояние электрона определяется только квантовым числом n. Решения, удовлетворяющие стандартным условиям, получаются при значениях l , не превышающих n – 1
![]() - всего n
значений
- всего n
значений
При данном ℓ квантовое число m может принимать 2ℓ + 1 различных значений
![]() .
.
Состояния атома с одинаковой энергией (одинаковым квантовым числом n), отличающиеся числами l и m, называются вырожденными состояниями.
Число различных состояний называется кратностью вырождения.
Так
как для данного n
![]() ,
а m
может принимать
,
а m
может принимать
![]() ,
значение , то кратность вырождения
водородного атома:
,
значение , то кратность вырождения
водородного атома:
![]()
Таким
образом, каждому значению En
соответствует несколько собственных
функций
![]() ,
отличающихся числами ℓ
и mℓ..
,
отличающихся числами ℓ
и mℓ..
Состояние электрона с ℓ = 0 называют S – состоянием,
ℓ= 1 - p – состоянием,
ℓ = 2 - d, ℓ = 3 - f, ℓ = 4 - g, ℓ = 5 - h.
Так
как
![]() ,
то возможны следующие состояния:
,
то возможны следующие состояния:
1S
2S 2P
3S 3P 3d
4S 4P 4d 4f
В квантовой механике доказывается, что для орбитального вантового числа имеется правило отбора
![]()
Это значит, что возможны такие переходы, при которых ℓ изменяется на единицу.
Поэтому
для серии Лаймана
![]() )
)
Бальмера
![]()
При увеличении числа n дискретность энергетических уровней уменьшается и характер поведения частицы приближается к классическому. В этом состоит принцип соответствия:
При больших квантовых числах следствия, вытекающие из квантовой механики, должны совпадать с результатами классической теории.
Подобно
тому, как при
![]() релятивистская механика переходит в
ньтоновскую, при
релятивистская механика переходит в
ньтоновскую, при
![]() квантовая механика переходит к
классическому описанию (пренебрегаем
квантовая механика переходит к
классическому описанию (пренебрегаем
![]() ).
).
Собственные функции распадаются на два множителя:
![]() ,
,
![]() - вещественный,
- вещественный,
![]() - комплексный.
- комплексный.
Так
как координаты r,![]() независимы, то при подстановке в уравнение
Шредингера в сферических координатах
уравнение Шредингера разбивается на
две независимые части.
независимы, то при подстановке в уравнение
Шредингера в сферических координатах
уравнение Шредингера разбивается на
две независимые части.
Первое уравнение Шредингера для радиальной части
![]()
и для сферической части
![]()
Первое уравнение зависит только от вида потенциальной энергии, а следовательно определяется конкретной физической природой взаимодействия частиц (для нашего случая – кулоновского).
Второе уравнение не зависит от вида силового поля, поэтому его решение одинаково для всех центрально-симметричных полей.
Условие нормировки для этих уравнений имеет вид в сферических координатах:
![]()
![]() - телесный угол
- телесный угол
Из решения этих уравнений можно сделать следующие выводы:
1) Электрон может иметь в атоме водорода лишь дискретные значения энергия:
, n = 1, 2, 3,…
2) Состояние электрона в атоме характеризуется набором 4 квантовых чисел
а) главного квантового числа n, определяющего энергию электрона;
б) орбитальное квантовое числа ℓ, определяющего дискретное значение модуля орбитального момента импульса
![]()
Магнитного
квантового числа mℓ,
определяющего стационарные ориентации
орбитального момента импульса электрона
L
в пространстве, например, их проекции
на направление внешнего магнитного
поля
![]() .
.
![]()
Диапазону
значений ℓ соответствует
![]() значений mℓ..
значений mℓ..
Например, если ℓ = 2, то вектор орбитального момента импульса электрона в атоме может принимать в пространстве дискретных ориентаций .mℓ = 0, ±1, ±2.
г) спинового квантового числа s, определяющего ориентацию собственного момента импульса электрона (спина).
Собственный механический момент электрона определяется
![]() ,
где
,
где
![]() .
.
Проекция собственного механического момента равна
![]() .
.
Полный механический момент электрона складывается из спинового и орбитального моментов электрона
![]() ,
j
= ℓ + s,
ℓ + s-1,
│ℓ-s│,
,
j
= ℓ + s,
ℓ + s-1,
│ℓ-s│,
j – квантовое число полного момента импульса.
Проекция полного механического момента
![]()
В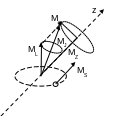 заимодействие
орбитального и магнитного момента (как
взаимодействие магнитных стрелок)
приводит к расщеплению энергетических
уровней, а следовательно, спектральных
линий. Оно называется спин-орбитальным
взаимодействием.
заимодействие
орбитального и магнитного момента (как
взаимодействие магнитных стрелок)
приводит к расщеплению энергетических
уровней, а следовательно, спектральных
линий. Оно называется спин-орбитальным
взаимодействием.
