
- •Бийский технологический институт (филиал) г.В. Багров, г.И. Севодина, о.Ю. Кравцова общая химическая технология
- •Содержание
- •Введение
- •Цель работы
- •Краткие теоретические сведения
- •Математическое описание процесса
- •Алгоритм решения
- •Задание
- •Контрольные вопросы
- •Лабораторная работа № 2. Исследование процесса восстановления двуокиси углерода углем
- •2.1 Цель работы
- •2.2 Краткие теоретические сведения
- •2.3 Описание кинетики процесса
- •2.4 Задание
- •2.5 Контрольные вопросы
- •Лабораторная работа № 3. Сравнение эффективности работы изотермических реакторов
- •3.1 Цель работы
- •3.2 Краткие теоретические сведения
- •3.3 Математическое описание изотермических реакторов
- •3.4 Задание
- •3.5 Контрольные вопросы
- •Лабораторная работа № 4. Исследование влияния условий проведения газофазной реакции на объем реактора
- •4.1 Цель работы
- •4.2 Краткие теоретические сведения
- •4.3 Математическое описание кинетики процесса
- •4.4 Задание
- •4.5 Контрольные вопросы
- •Лабораторная работа № 5. Расчет неизотермических реакторов
- •5.1 Цель работы
- •5.2 Краткие теоретические сведения
- •5.3 Задание
- •5.4 Контрольные вопросы
- •Лабораторная работа № 6. Реакторы с неидеальной структурой потока
- •6.1 Цель работы
- •6.2 Краткие теоретические сведения
- •6.3 Задание
- •6.4 Контрольные вопросы
- •Лабораторная работа № 7. Обогащение минерального сырья. Флотация
- •7.1 Цель работы
- •7.2 Краткие теоретические сведения
- •7.3 Описание лабораторной установки
- •7.4 Методика проведения работы
- •7.5 Обработка данных
- •7.6 Контрольные вопросы
- •Лабораторная работа № 8. Жесткость воды и еЕ определение. Методы снижения жесткости воды
- •8.1 Цель работы
- •8.2 Краткие теоретические сведения
- •8.3 Описание лабораторной установки
- •8.4 Определение жесткости воды
- •8.5 Обработка данных
- •8.6 Контрольные вопросы
- •Литература
- •А2 Программа № 2
- •А3 Программа № 3
- •А4 Программа № 4
- •А5 Программа № 5
- •А6 Программа № 6
- •А7 Программа № 7
- •А8 Программа № 8
- •А9 Программа № 9
Математическое описание процесса
Кинетическое уравнение описывает скорость изменения концентрации реагентов по мере протекания реакции окисления сернистого ангидрида. Оно позволяет определять необходимые для расчета реактора технологические параметры.
Кинетика данного процесса с достаточной степенью точности описывается уравнением Иванова-Борескова [8]:
 ,
(1.1)
,
(1.1)
где r – скорость реакции, с-1;
![]() ,
,
![]() –
начальные
концентрации SO2
и
О2
соответственно
доли;
–
начальные
концентрации SO2
и
О2
соответственно
доли;
Р – давление, атм.;
х – степень превращения, доли;
Кр – константа равновесия реакции, атм.-0,5;
k – константа скорости, с-1атм.-0,5.
В случае, когда исходная газовая смесь состоит из SO2 и воздуха, величина находится по формуле:
= 0,21(1- ). (1.2)
Значения Кр рассчитываются по уравнению:
![]() .
(1.3)
.
(1.3)
Величины констант скоростей для ванадиевого катализатора с размером гранул от 2 до 3 мм рассчитываются в зависимости от температуры по следующим формулам:
![]() при Т<673К;
(1.4)
при Т<673К;
(1.4)
![]() при 673 К < Т< 806 К;
(1.5)
при 673 К < Т< 806 К;
(1.5)
![]() =
1,361 при Т>806 К.
(1.6)
=
1,361 при Т>806 К.
(1.6)
Обозначив правую часть
уравнения (1.1) за f(x),
можем представить это уравнение для
нахождения условного времени пребывания
![]() при заданных х:
при заданных х:
![]() .
(1.7)
.
(1.7)
При расчете следует иметь в виду, что степень превращения не может превышать равновесную степень превращения для той температуры, при которой велся расчет. Значение хр может быть получено по соотношению:
 .
(1.8)
.
(1.8)
Алгоритм решения
Для определения условного времени пребывания при заданной степени превращения согласно уравнению (1.7) необходимо применить численные методы для вычисления определенного интеграла и метод решения трансцендентного уравнения (1.8). Программа решения задачи приведена в Приложении А.
Задание
1.5.1 Построение зависимостей
x=F(![]() )
и r=F(x)
)
и r=F(x)
Эти зависимости в случае
изотермического процесса позволяют
определить большинство технологических
параметров и размеры реактора, необходимые
для достижения заданной степени
превращения. В соответствии с номером
варианта принять заданное значение
начальной
концентрации сернистого ангидрида
![]()
![]() и при температуре Т=773 К
выполнить расчеты на компьютере. Предел
допустимой точности решения определяется
по равновесной степени превращения Хр,
которая также рассчитывается в программе
на основании уравнения (1.8). По
полученным данным строят график в
координатах "х -
"
или "r
-
".
На графике "х -
"
проводят линию, параллельную оси
,
соответствующую
значениям Хр.
Решение справедливо до значения
,
соответствующего пересечению этой
линии с кривой "х -
".
и при температуре Т=773 К
выполнить расчеты на компьютере. Предел
допустимой точности решения определяется
по равновесной степени превращения Хр,
которая также рассчитывается в программе
на основании уравнения (1.8). По
полученным данным строят график в
координатах "х -
"
или "r
-
".
На графике "х -
"
проводят линию, параллельную оси
,
соответствующую
значениям Хр.
Решение справедливо до значения
,
соответствующего пересечению этой
линии с кривой "х -
".
1.5.2 Построение линии оптимальных температур (ЛОТ)
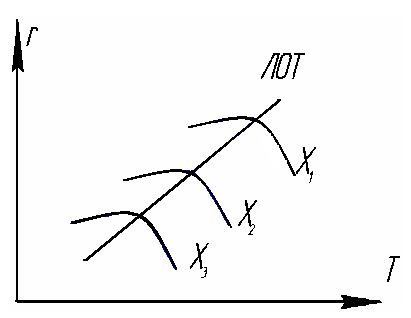
Для определения оптимальных условий работы промышленного реактора используется линия оптимальных температур (ЛОТ). Она может быть получена с помощью графика "х - " или "r - ". Для серии температур в интервале 693 К < Т < 893 К получают кривые r=F(t) (рисунок 1.3) по результатам расчета с помощью программы № 1. Далее рассматривают сечения полученного семейства кривых линиями =const. Исходя из этих сечений, строят график в координатах r=F(T) при =const (рисунок 1.4). Линия, соединяющая максимумы полученных кривых, называется линией оптимальных температур.
1.5.3 Построить профиль концентрации CА=f(l) по высоте трубчатого реактора при температуре Т=853 К и начальной концентрации , заданной в таблице 1.1, согласно номеру варианта.
Таблица 1.1 – Варианты заданий
Номер варианта |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
0,05 |
0,07 |
0,1 |
0,15 |
0,2 |
0,25 |
0,3 |
При этом заданы:
объем аппарата Vr = 3,14 10-3 м3;
диаметр аппарата d = 0,l м;
длина аппарата L = 0,4 м;
объемный расход газа v = 7,84 10-3 м3/с.
При расчетах воспользоваться программой № 2.

ростой
необратимой.___
