
- •1. Определение температуры воды
- •2. Определение запаха я вкуса воды
- •3. Определение плотности воды
- •4. Определение цветности воды
- •Настройки прибора
- •Определение рН исследуемой воды
- •Задачи я вопросы
- •Работа 4. Определение содержания ионов Сl- и s в воде
- •Реактивы
- •Продолжительность нагрева воды о перманганатом калия сильно сказывается на его окислявшем действии.
- •Вопросы
- •Работа 9. Определение содержания гидрокарбонатов и карбонатов в воде
- •Вопросы и задачи
- •Фотоколориметрический метод
- •Вопросы и задачи
- •Реактивы
- •Работа 13. Определение содержания фенолов в воде
- •Контрольные вопросы
Фотоколориметрический метод
Из исходного стандартного раствора с концентрацией ионов 0.02 мг/мл говорят рабочий стандартный раствор, для чего 1мл исходного раствора разбавляют дистиллированной водой в колбе на 100мл. Концентрация ионов в нём составляет 0.0002 мг/мл(0.2 мг/л). Затем в колбу емкостью 100мл наливают 50мл рабочего стандартного раствора. В другую (такую же) -50 мл отфильтрованной исследуемой воды. В каждую колбу прибавляют по 5 мл реактива Грисса.
Растворы перемешивают и нагревают на водяной бане при 50-60̊ С в течении 10минут. Затем охлаждают и колориметрируют на ФЭКе* (зеленый светофильтр № 5, кюветы с толщиной слоя 20 мм).
Определение оптической плотности исследуемой воды и рабочего стандартного раствора проводят по 3 раза. Результаты записывают в табл. 2.
РАСЧЁТ
Содержание ионов в исследуемой воде, мл/л:
 =
=![]()
Где С ст. – содержание ионов в рабочем стандартном растворе мл/г.
Д иссл. – оптическая плотность исследуемой воды.
Д ст. – оптическая плотность рабочего стандартного раствора
Результаты расчёта записывают в табл. 2.
Таблица 2
Оптическая плотность рабочего стандартного р-ра |
Оптическая плотность исследуемой воды |
Содержание ионов в исследуемой воде, мг/л |
|||||||
Д1 |
Д2 |
Д3 |
Д1 |
Д2 |
Д3 |
Х1 |
Х2 |
Х3 |
Хср |
*Фотоколориметрирование подробно рассмотрено в работах № 6,7.
Вопросы и задачи
Какие соединения азота образуются в воде? Каково их происхождение?
Как по содержанию азотсодержащих веществ в воде судят о времени загрязнения водоёма.
Какими методами определяют содержание ионов в воде? В чём сущность ускоренного метода?
В чём сущность фотоколориметрического метода определения содержания ионов в воде? Привести реакции образования азосоединения.
Содержание ионов
 в
воде 0.04 мг/л. Выразить эту величину в
эквивалентной форме.
в
воде 0.04 мг/л. Выразить эту величину в
эквивалентной форме.
РАБОТА 11. ОПРЕДЕЛЕНИЕ НИТРАТОВ В ВОДЕ
Соединения азота связанны с жизнедеятельностью водных организмов.
Главный источник азота в природных водах- белковые соединения растительного и животного происхождения. В результате биохимического расщепления белков выделяют аммиак, который под воздействием биохимических процессов переходит в другие формы азота.
Процесс биохимического окисления аммиака до нитратов называется нитрификацией.
Преобладание
в воде ионов ![]() указывает на окончание окисления
органических примесей и значительный
срок, прошедший с момента загрязнения
водоёмов.
указывает на окончание окисления
органических примесей и значительный
срок, прошедший с момента загрязнения
водоёмов.
Повышенное содержание нитратов в питьевой воде нежелательно, т.к. в организме они могут восстанавливаться до нитратов, которые, взаимодействуя с гемоглобином, уменьшают его способность переносить кислород.
Содержание ионов в воде определяют фотоколориметрированием или ускоренным методом.
В данной работе используют ускоренный метод, в котором определения проводят при помощи раствора дифениламина в серной кислоте.
Практическая часть
Реактивы
 (раствор)
(раствор)Исходный стандартный раствор KN
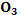
(p=1.84)
(8% раствор)
![]()
Из исходного стандартного раствора KN готовят растворы с разным содержанием ионов (стандартную шкалу). Для этого в мерные колбы емкостью 100мл вводят указанные в таблице количестве исходного раствора и дистилированой водой доводят до метки.
Номер колбы |
1 |
2 |
3 |
4 |
5 |
6 |
|
Объём исходного стандартного раствора |
1,0 |
5,0 |
10,0 |
20,0 |
50,0 |
100,0 |
|
Содержание ионов мг/л |
0,1 |
0,5 |
1,0 |
2,0 |
2,0 |
10,0 |
|
В шесть пронумерованных пробирок из каждой колбы пипеткой отбирают по 2 мл соответствующего раствора KN . В седьмую пробирку вводят пипеткой 2 мл отфильтрованной исследуемой воды. В каждую пробирку прибавляют по 0.1 мл 8% раствора NaCl тщательно взбалтывают и затем осторожно по стенке пробирки приливают цилиндром по 2 мл дифениламина в серной кислоте.
В всех пробирках на границе раздела двух растворов появляется полоска синего цвета. Полоску в пробирке с исследуемой водой сравнивают с соответствующими полосками в растворах стандартной шкалы.
Содержание ионов в исследуемой воде равно их концентрации в стандартном растворе, имеющим синюю полоску, идентичную по ширине и интенсивности окраски полоске в исследуемой воде.
Если
синяя полоска в исследуемой воде шире
(3-4 мм), чем в наиболее концентрированном
стандартном растворе (концентрация
ионов ![]() 10мг/л), то исследуемую воду разбавляют
в 2 или 5 раз и определение повторяют.
10мг/л), то исследуемую воду разбавляют
в 2 или 5 раз и определение повторяют.
