
- •Основы биохимии и токсикологии
- •Введение
- •Лабораторная работа №1 Лабораторнаяя работа 2 поляриметрическое определение сахаров
- •Лабораторная работа № 2
- •Тема: Определение Сахаров
- •Количественное определение содержания углеводов (по методу Шоорля)
- •1. Определение моносахаридов и дисахаридов
- •Определение глюкозы по методу Шоорля
- •2. Определение крахмала
- •Содержание различных форм углеводов в растениях
- •Тема: белки
- •Качественные реакции на белки
- •Реакции осаждения белков
- •Определение белков в листьях растений при помощи цветных реакций (по методу м. X. Чайлахяна)
- •Количественное определение белковых фракций
- •Лабораторная работа № 4 Тема: Определение Липидов Определение в липидах чисел - кислотного, омыления и эфирного
- •Полумакрометоды определения чисел - кислотного, омыления и эфирного
- •Рефрактометрический метод определения йодного числа
- •Раздел 2
- •4.1. Ксенобиотики
- •Контрольные вопросы
- •Строение мембраны
- •Функции мембран
- •Пути поступления веществ в клетку
- •Мембранотропные свойства ксенобиотиков
- •Лабораторная работа № 8 Определение нитратов в растительной продукции
- •Ход работы
- •Литература
Качественные реакции на белки
Качественные реакции на аминокислоты, пептиды и белки можно разделить на две группы:
1) цветные реакции, обусловленные аминокислотами и пептидами;
2) реакции осаждения, в основе которых лежат изменения физико-хнмических свойств белковых молекул.
Цветные реакции. Для качественного определения белков применяют следующие характерные реакции:
1. Биуретовая реакция на белки (реакция Пиотровского на пептидную связь). В разные пробирки наливают по 1-2 см3 раствора белка с равным объемом 4 %-ного раствора щелочи и постепенно, по стенке пробирки добавляют 1-2 капли 0,5 %-ного раствора медного купороса. Жидкость окрашивается в фиолетово-синий или фиолетово-красный цвет (биуретовая реакция) благодаря присутствию в молекуле белка пептидной связи (—СО—NH—). Реакцию дают все белки, а также продукты их гидролиза − пептоны и полипептиды, начиная с тетрапептидов.
2. Ксантопротеиновая реакция (Мульдера). Эта реакция на белки обусловлена образованием нитропроизводных ароматических и некоторых гетероциклических радикалов. При взаимодействии белка с азотной кислотой происходит нитрование ядра содержащихся в белке ароматических аминокислот с образованием окрашенных соединений. Таким образом, с помощью ксантопротеиновой реакции в составе белка можно обнаружить такие циклические аминокислоты, как фенилаланин, тирозин, триптофан н др.
Реакция протекает по схеме:
.
 −
NH
– CH
– CO
− ... ... – NH
– CH
– CO
− ... ... – NH
– CH
– CO
− ...
−
NH
– CH
– CO
− ... ... – NH
– CH
– CO
− ... ... – NH
– CH
– CO
− ...

 CH2
CH2
CH2
CH2
CH2
CH2
HNO3
NaOH






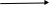
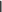
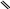
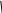
 NO2
N – O Na+
NO2
N – O Na+
OH OH O O
тирозин желтый цвет оранжевый цвет
Реактивы: 1) растворы белков;
2) раствор желатина;
3) HNO3, концентрированная;
4) 20%-ный раствор NаОН.
Ход определения. Реакцию следует проводить под тягой. В пробирки наливают по 1 мл растворов белков и желатина и в каждою добавляют по 5 капель азотной кислоты. В пробирках выпадает осадок. Содержимое пробирок осторожно нагревают при постоянном перемешивании. Если осадок содержит аминокислоты с ароматическим или гетероциклическим радикалом, при нагревании раствор и осадок окрашиваются в желтый цвет. Охладив смесь, осторожно, по каплям, добавляют избыток гидроксида аммония. При этом желтая окраска раствора переходит в оранжевую. При обработке белков корепкой азотной кислотой появляется желтое окрашивание (нитрование), которое после добавления основания переходит в оранжевое. Реакция указывает на присутствие фенилаланина, тирозина либо триптофана.
3. Реакция обнаружения серы в белке (Фоле)
Белок, содержащий в своем составе серу, при нагревании с раствором щелочи гидролизуется, сера отщепляется а виде сероводорода, который тут же превращается в сульфид натрия. Таким образом, для обнаружения серы в белках требуется разрушение белковой молекулы. Отщепляющуюся серу можно определить с помощью ацетата свинца, который реагирует с сульфидом натрия, образуя черный осадок сульфида свинца.
HS−CH2 – CH(NH2) – COOH + NaOH → − CH2 – CH (NH2) – COOH +H2S
H2S + NaOH → Na2S + H2O
(СН3СОО)2РЬ + Na2S → 2 CH3COONa + PbS↓
Если количество серы в белке незначительно, вместо осадка образуется раствор коричневого цвета.
Реакция обусловлена присутствием в белке серосодержащих аминокислот: цистина, цистеина и метионина.
Реактивы:
1) растворы белков;
2) 10%-ный раствор NaOH;
3) 10%-ный раствор (CH3COO)2Pb.
Ход определения. В пробирки наливают по 1 мл растворов белков. В каждую пробирку добавляют двойной объем 10%-ного раствора гидроксида натрия. Содержимое пробирок перемешивают и осторожно кипятят в течение 1-2 минут. Затем в каждую пробирку приливают но 1 мл раствора ацетата свинца и снова нагревают. Наблюдают за изменением окраски раствора в пробирках.
4. Реакция на триптофан (Адамкевнча). Триптофан, реагируя в кислой среде с альдегидами, образует окрашенные продукты конденсации. Так, с глиоксиловой кислотой (являющейся примесью в концентрированной уксусной кислоте) реакция протекает но уравнению:
о II С
–С =О
Н
ОН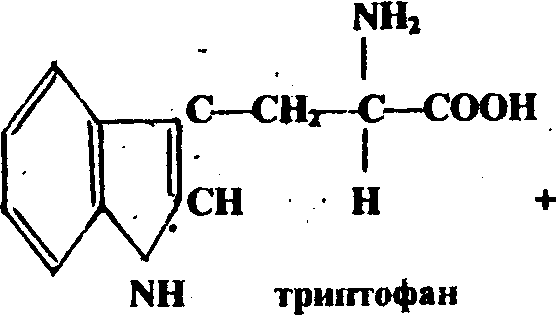

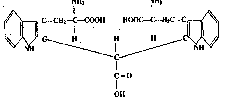
По аналогичной схеме протекает реакция триптофана с оксиметилфурфуролом или формальдегидом.
Реактивы:
1) растворы белков;
2) 1%-иый раствор желатина;
3) СН3СООН, концентрированная;
4) H2SO4, концентрированная.
Ход определения. В пробирку наливают несколько капель неразбавленного яичного белка, прибавляют 1-2 мл уксусной кислоты и осторожно нагревают до растворения выпавшего осадка, после чего охлаждают и осторожно но стенке пробирки, наклонив ее, наливают 1 мл серной кислоты, которую используют в качестве водоотнимающего средства. На границе двух несмешивающихся слоев жидкостей через некоторое время появляется красно-фиолетовое кольцо.
Эту же реакцию повторяют с раствором желатина. Окрашивание не происходит, т.к. триптофан не входит в состав желатина.
