
- •Глава 1. Первое начало термодинамики
- •1.1. Термодинамические состояния и термодинамические процессы
- •1.2. Внутренняя энергия и температура термодинамической системы
- •1.3. Методы измерения температуры
- •1.4. Адиабатически изолированная система
- •1.5. Первое начало термодинамики
- •Глава 2. Уравнения состояния термодинамических систем.
- •2.1. Уравнение состояния идеального газа
- •.2. Основные положения молекулярно-кинетической теории
- •2.3. Экспериментальные подтверждения молекулярно-кинетической теории
- •2.4. Теплоёмкость идеального газа
- •2.5. Адиабатический процесс
- •2.6. Политропический процесс
- •2.7. Газ Ван-дер-Ваальса
- •Глава 3. Второе и третье начала термодинамики.
- •3.1. Тепловые машины
- •3.2. Цикл Карно
- •3.3. Расчет цикла Карно для реального газа
- •3.4. Второе начало термодинамики
- •3.5. Теорема Карно
- •3.6. Термодинамическая шкала температур
- •3.7. Неравенство Клаузиуса
- •3.8. Термодинамическая энтропия
- •3.9. Закон возрастания энтропии
- •3.10. Третье начало термодинамики
- •Глава 4. Описание термодинамических процессов.
- •4.1. Основное неравенство и основное уравнение термодинамики
- •4.2. Термодинамические потенциалы
- •4.3. Применение термодинамических потенциалов для описания эффекта Джоуля-Томсона
- •4.4. Принцип Ле-Шателье - Брауна
- •4.5. Введение в термодинамику необратимых процессов
- •Глава 5. Статистическое описание равновесных состояний.
- •5.1. Функция распределения
- •5.2. Распределение Больцмана
- •5.3. Принцип детального равновесия
- •5.4. Распределение Максвелла
- •5.5. Экспериментальная проверка распределения Максвелла
- •5.6. Распределение Максвелла-Больцмана
- •5.7. Каноническое распределение Гиббса
- •5.8. Равновесные флуктуации
- •5.9. Статистическое обоснование второго начала термодинамики
- •Глава 6. Явление переноса.
- •6.1. Термодинамические потоки
- •6.2. Описание явлений переноса в газах
- •6.3. Эффузия в разреженном газе
- •6.4. Броуновское движение
- •6.5. Производство энтропии в необратимых процессах
- •Глава 7. Равновесие фаз и фазовые превращения.
- •7.1. Агрегатные состояния вещества
- •7.2. Условия равновесия фаз
- •7.3. Явления на границе раздела газа, жидкости и твердого тела
- •7.4. Фазовые переходы первого рода
- •7.5. Диаграммы состояния
- •7.6. Фазовые переходы второго рада
- •7.7. Критические явления при фазовых переходах
4.5. Введение в термодинамику необратимых процессов
Применение
законов равновесной термодинамики
ограничено случаем, когда температура
![]() ,
давление
,
давление![]() и
другие параметры состояния во всех
точках системы одинаковы. Если это не
так, то в термодинамической системе
возникают необратимые процессы.
и
другие параметры состояния во всех
точках системы одинаковы. Если это не
так, то в термодинамической системе
возникают необратимые процессы.
Для
описания необратимых процессов можно
воспользоваться гипотезой
локального равновесия,
заключающейся в предположении, что
внутри малого объема среды выполняется
основное уравнение термодинамики
равновесных процессов. Если в качестве
параметров состояния ввести локальную
плотность внутренней энергии
![]() ,
приходящуюся на единицу массы среды, и
удельный объем
,
приходящуюся на единицу массы среды, и
удельный объем ,
где
,
где![]() -
локальная плотность среды, то для точки
среды с координатами
-
локальная плотность среды, то для точки
среды с координатами![]() в
момент времени
в
момент времени![]() можно
записать уравнение
можно
записать уравнение
|
|
(4.82) |
Здесь
![]() -
удельная энтропия на единицу массы
среды.
-
удельная энтропия на единицу массы
среды.
Тогда
внутренняя энергия
![]() всей
системы определяется с помощью выражения
всей
системы определяется с помощью выражения
|
|
(4.83) |
а
ее энтропия
![]() соответственно
может быть найдена по формуле
соответственно
может быть найдена по формуле
|
|
(4.84) |
Совместное применение уравнения (4.82) с уравнениями баланса массы, внутренней энергии и других термодинамических величин, позволяет построить феноменологическую термодинамику необратимых процессов, опирающуюся на использование полученных из опыта соотношений между параметрами, описывающими термодинамические процессы.
Ключевое значение в термодинамике необратимых процессов имеет величина, численно равная скорости увеличения энтропии в единице объема:
|
|
(4.85) |
Эта
величина
![]() представляет
собой производство энтропии для
единичного объема адиабатически
изолированной системы.
Она описывает количество энтропии,
которая возникает в единичном объеме
термодинамической системы за единицу
времени при протекании в ней необратимых
термодинамических процессов.
представляет
собой производство энтропии для
единичного объема адиабатически
изолированной системы.
Она описывает количество энтропии,
которая возникает в единичном объеме
термодинамической системы за единицу
времени при протекании в ней необратимых
термодинамических процессов.
Если
в качестве термодинамических параметров
системы выступают
![]() величин
величин![]() ,
то формулу(4.85)
можно представить в виде:
,
то формулу(4.85)
можно представить в виде:
|
|
(4.86) |
Величины
 называютсятермодинамическими
силами,
а величины
называютсятермодинамическими
силами,
а величины
![]() -плотностями
термодинамических потоков.
Следовательно, производство энтропии
-плотностями
термодинамических потоков.
Следовательно, производство энтропии
![]() можно
рассчитывать по формуле:
можно
рассчитывать по формуле:
|
|
(4.87) |
В
случае небольших отклонений от
равновесного состояния между
термодинамическими потоками
![]() и
термодинамическими силами
и
термодинамическими силами![]() может
быть установлена линейная зависимость
может
быть установлена линейная зависимость
|
|
(4.88) |
Это соответствует наиболее простому случаю термодинамики линейных необратимых процессов.
Таким образом, для линейных необратимых процессов производство энтропии определяется выражением
|
|
(4.89) |
или
|
|
(4.90) |
Коэффициенты
![]() называются
кинетическими коэффициентами, и они
характеризуют интенсивность явлений
переноса.
В 1931 году американский физик и химик
Ларс
Онсагер (1903
- 1976) установил, что для кинетических
коэффициентов выполняется условие:
называются
кинетическими коэффициентами, и они
характеризуют интенсивность явлений
переноса.
В 1931 году американский физик и химик
Ларс
Онсагер (1903
- 1976) установил, что для кинетических
коэффициентов выполняется условие:
|
|
(4.91) |
указывающее на симметрию матрицы кинетических коэффициентов. Выражение (4.91) называется соотношением взаимности Онсагера.
Одним из принципов термодинамики линейных необратимых процессов является предложенный в 1947 году бельгийским физико-химиком Ильей Романовичем Пригожиным (р. 1917) принцип минимума производства энтропии:
Стационарные необратимые процессы протекают таким образом, чтобы производство энтропии было минимальным.
Принцип минимума производства энтропии позволяет установить критерий отбора реализующихся в природе необратимых процессов от реально не наблюдающихся, и, таким образом, выбрать из возможных процессов реально существующие.
Необходимость выполнения указанного принципа приводит к тому, что при протекании в среде необратимых стационарных процессов возникают динамические структуры, названные Пригожиным диссипативными структурами, что уменьшает производство энтропии. Примером таких структур могут служить ячейки Бенара - регулярные динамические структуры, возникающие в тонком слое нагреваемой снизу жидкости, и колебательные химические реакции Б.П. Белоусова, при которых происходят периодические изменения концентрации реагирующих веществ.

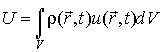 ,
, .
. .
. .
. .
.
 .
.