
- •Глава 1. Первое начало термодинамики
- •1.1. Термодинамические состояния и термодинамические процессы
- •1.2. Внутренняя энергия и температура термодинамической системы
- •1.3. Методы измерения температуры
- •1.4. Адиабатически изолированная система
- •1.5. Первое начало термодинамики
- •Глава 2. Уравнения состояния термодинамических систем.
- •2.1. Уравнение состояния идеального газа
- •.2. Основные положения молекулярно-кинетической теории
- •2.3. Экспериментальные подтверждения молекулярно-кинетической теории
- •2.4. Теплоёмкость идеального газа
- •2.5. Адиабатический процесс
- •2.6. Политропический процесс
- •2.7. Газ Ван-дер-Ваальса
- •Глава 3. Второе и третье начала термодинамики.
- •3.1. Тепловые машины
- •3.2. Цикл Карно
- •3.3. Расчет цикла Карно для реального газа
- •3.4. Второе начало термодинамики
- •3.5. Теорема Карно
- •3.6. Термодинамическая шкала температур
- •3.7. Неравенство Клаузиуса
- •3.8. Термодинамическая энтропия
- •3.9. Закон возрастания энтропии
- •3.10. Третье начало термодинамики
- •Глава 4. Описание термодинамических процессов.
- •4.1. Основное неравенство и основное уравнение термодинамики
- •4.2. Термодинамические потенциалы
- •4.3. Применение термодинамических потенциалов для описания эффекта Джоуля-Томсона
- •4.4. Принцип Ле-Шателье - Брауна
- •4.5. Введение в термодинамику необратимых процессов
- •Глава 5. Статистическое описание равновесных состояний.
- •5.1. Функция распределения
- •5.2. Распределение Больцмана
- •5.3. Принцип детального равновесия
- •5.4. Распределение Максвелла
- •5.5. Экспериментальная проверка распределения Максвелла
- •5.6. Распределение Максвелла-Больцмана
- •5.7. Каноническое распределение Гиббса
- •5.8. Равновесные флуктуации
- •5.9. Статистическое обоснование второго начала термодинамики
- •Глава 6. Явление переноса.
- •6.1. Термодинамические потоки
- •6.2. Описание явлений переноса в газах
- •6.3. Эффузия в разреженном газе
- •6.4. Броуновское движение
- •6.5. Производство энтропии в необратимых процессах
- •Глава 7. Равновесие фаз и фазовые превращения.
- •7.1. Агрегатные состояния вещества
- •7.2. Условия равновесия фаз
- •7.3. Явления на границе раздела газа, жидкости и твердого тела
- •7.4. Фазовые переходы первого рода
- •7.5. Диаграммы состояния
- •7.6. Фазовые переходы второго рада
- •7.7. Критические явления при фазовых переходах
4.4. Принцип Ле-Шателье - Брауна
Общее условие устойчивости равновесия изолированных систем может быть сформулировано на основе закона возрастания энтропии. Из этого закона следует, что возрастание энтропии изолированной системы происходит до тех пор, пока в ней не затухают все необратимые процессы. В этом случае энтропия достигает максимального значения. Следовательно, условие устойчивости состояния термодинамической системы можно сформулировать следующим образом:
Если энтропия адиабатически изолированной термодинамической системы принимает максимальное значение, то ее состояние термодинамически устойчиво.
Данное
условие означает, что при устойчивом
термодинамическом равновесии энтропия
![]() адиабатически
изолированной системы имеет экстремум:
адиабатически
изолированной системы имеет экстремум:![]() ,
где
,
где![]() -
энтропия системы в состоянии
термодинамического равновесия.
Следовательно, в состоянии устойчивого
равновесия первая вариация энтропии
-
энтропия системы в состоянии
термодинамического равновесия.
Следовательно, в состоянии устойчивого
равновесия первая вариация энтропии![]() изолированной
термодинамической системы равна нулю:
изолированной
термодинамической системы равна нулю:![]() ,
а вторая ее вариация
,
а вторая ее вариация![]() -
меньше нуля:
-
меньше нуля:![]() .
В данном случае под вариацией энтропии
понимается ее бесконечно малое изменение
при бесконечно малом изменении параметров
состояния, которые приводят к переводу
системы в неравновесное состояние.
Условие равенства нулю первой вариации
энтропии
.
В данном случае под вариацией энтропии
понимается ее бесконечно малое изменение
при бесконечно малом изменении параметров
состояния, которые приводят к переводу
системы в неравновесное состояние.
Условие равенства нулю первой вариации
энтропии![]() дает
необходимое условие равновесия
изолированной системы, а неравенство
дает
необходимое условие равновесия
изолированной системы, а неравенство![]() -
достаточное условие устойчивости
равновесного состояния.
-
достаточное условие устойчивости
равновесного состояния.
На термодинамическую систему, находящуюся в состоянии устойчивого равновесия, могут воздействовать внешние факторы, выводящие ее из этого состояния. Реакцию системы на эти воздействия можно качественно определить на основе принципа Ле-Шателье - Брауна, предложенного в 1884 году французским химиком Анри Луи Ле-Шателье (1850 - 1936) и обоснованного в 1887 году немецким физиком Карлом Фердинандом Брауном (1850 - 1918):
Внешние воздействия, выводящие термодинамическую систему из состояния устойчивого равновесия, вызывают в ней протекание процессов, которые уменьшают влияние этих внешних возмущений.
Противодействие внешним воздействиям протекающими в системе процессами напоминает известное в электродинамике правило Ленца, утверждающее, что индукционный ток в проводящем контуре всегда направлен так, что бы противодействовать изменению магнитного потока через поверхность, ограниченную этим контуром.
Сформулированный принцип позволяет предсказать направление протекания процессов в термодинамической системе, которая выводится из состояния устойчивого равновесия внешними воздействиями. Рассмотрим наглядный пример применения принципа Ле-Шателье-Брауна. Пусть имеется смесь льда и воды, находящаяся в состоянии устойчивого равновесия. Если этой смеси сообщить некоторое количество теплоты, то лед начнет таять, что будет препятствовать повышению температуры смеси. То есть, протекающий в системе процесс таяния льда будет ослаблять изменения, вызываемые подводом теплоты.
Примером использования в техническом устройстве процессов, следующих из принципа Ле-Шателье - Брауна, является поглощение газа в адсорбционных вакуумных насосах. Химическая адсорбция газа, как правило, происходит с выделением теплоты. Соответственно при охлаждении вещества (адсорбента), наблюдается резкое увеличение поглощения им газа, что позволяет уменьшить давление этого газа в вакуумируемом сосуде. При нагреве адсорбента газ из него выделяется, и система возвращается в исходное состояние.
Задача
4.6. Один моль идеального газа находится
в эластичной оболочке, с внешней стороны
которой действует постоянное давление.
Показать, что при подводе к этому газу
некоторого количества теплоты
![]() произойдет
его расширение, приводящее, в соответствии
с принципом Ле-Шателье - Брауна, к
уменьшению изменения его температуры
произойдет
его расширение, приводящее, в соответствии
с принципом Ле-Шателье - Брауна, к
уменьшению изменения его температуры
![]() по
сравнению с изменением температуры
по
сравнению с изменением температуры
![]() ,
которое имело бы место при неизменном
объеме газа:
,
которое имело бы место при неизменном
объеме газа:
![]() .
Проанализировать случай, когда в этой
оболочке находится фотонный газ.
.
Проанализировать случай, когда в этой
оболочке находится фотонный газ.
Решение: Для одного моля идеального газа в случае изобарического процесса изменение температуры может быть вычислено по формуле
 ,
,
а для изохорического - соответственно определяется выражением
 .
.
Из этих формул имеем:
 .
.
Так
как
![]() ,
то
,
то
![]() .
Из этого следует, что в рассматриваемой
термодинамической системе при внешнем
воздействии (подводе теплоты) возникает
процесс (расширение газа), приводящий
к уменьшению влияния внешнего возмущения:
изменение температуры газа меньше, чем,
если бы расширение не возникало.
.
Из этого следует, что в рассматриваемой
термодинамической системе при внешнем
воздействии (подводе теплоты) возникает
процесс (расширение газа), приводящий
к уменьшению влияния внешнего возмущения:
изменение температуры газа меньше, чем,
если бы расширение не возникало.
Если
в оболочке находится фотонный газ,
уравнение состояния которого имеет
вид:
![]() ,
то при подводе теплоты в изобарическом
процессе при
,
то при подводе теплоты в изобарическом
процессе при
![]() ,
изменение температуры не происходит:
,
изменение температуры не происходит:
![]() .
А для изохорического процесса, учитывая
выражение для внутренней энергии
фотонного газа:
.
А для изохорического процесса, учитывая
выражение для внутренней энергии
фотонного газа:
![]() ,
можно записать
,
можно записать
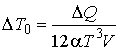 ,
,
где
изменение температуры
![]() считается
малым, по сравнению с температурой газа
считается
малым, по сравнению с температурой газа
![]() :
:
![]() .
.
Таким образом, происходящие в системе процессы могут не только уменьшить влияние внешнего воздействия, но и скомпенсировать его полностью. Из рассмотренного примера фотонного газа в эластичной оболочке следует, что для такой термодинамической системы подвод теплоты не приводит к увеличению её температуры.
