
- •Глава 1. Первое начало термодинамики
- •1.1. Термодинамические состояния и термодинамические процессы
- •1.2. Внутренняя энергия и температура термодинамической системы
- •1.3. Методы измерения температуры
- •1.4. Адиабатически изолированная система
- •1.5. Первое начало термодинамики
- •Глава 2. Уравнения состояния термодинамических систем.
- •2.1. Уравнение состояния идеального газа
- •.2. Основные положения молекулярно-кинетической теории
- •2.3. Экспериментальные подтверждения молекулярно-кинетической теории
- •2.4. Теплоёмкость идеального газа
- •2.5. Адиабатический процесс
- •2.6. Политропический процесс
- •2.7. Газ Ван-дер-Ваальса
- •Глава 3. Второе и третье начала термодинамики.
- •3.1. Тепловые машины
- •3.2. Цикл Карно
- •3.3. Расчет цикла Карно для реального газа
- •3.4. Второе начало термодинамики
- •3.5. Теорема Карно
- •3.6. Термодинамическая шкала температур
- •3.7. Неравенство Клаузиуса
- •3.8. Термодинамическая энтропия
- •3.9. Закон возрастания энтропии
- •3.10. Третье начало термодинамики
- •Глава 4. Описание термодинамических процессов.
- •4.1. Основное неравенство и основное уравнение термодинамики
- •4.2. Термодинамические потенциалы
- •4.3. Применение термодинамических потенциалов для описания эффекта Джоуля-Томсона
- •4.4. Принцип Ле-Шателье - Брауна
- •4.5. Введение в термодинамику необратимых процессов
- •Глава 5. Статистическое описание равновесных состояний.
- •5.1. Функция распределения
- •5.2. Распределение Больцмана
- •5.3. Принцип детального равновесия
- •5.4. Распределение Максвелла
- •5.5. Экспериментальная проверка распределения Максвелла
- •5.6. Распределение Максвелла-Больцмана
- •5.7. Каноническое распределение Гиббса
- •5.8. Равновесные флуктуации
- •5.9. Статистическое обоснование второго начала термодинамики
- •Глава 6. Явление переноса.
- •6.1. Термодинамические потоки
- •6.2. Описание явлений переноса в газах
- •6.3. Эффузия в разреженном газе
- •6.4. Броуновское движение
- •6.5. Производство энтропии в необратимых процессах
- •Глава 7. Равновесие фаз и фазовые превращения.
- •7.1. Агрегатные состояния вещества
- •7.2. Условия равновесия фаз
- •7.3. Явления на границе раздела газа, жидкости и твердого тела
- •7.4. Фазовые переходы первого рода
- •7.5. Диаграммы состояния
- •7.6. Фазовые переходы второго рада
- •7.7. Критические явления при фазовых переходах
2.6. Политропический процесс
В параграфе 2.4 отмечалось, что важным классом термодинамических процессов являются процессы, происходящие при постоянной теплоемкости, то есть политропические процессы. К таким процессам, в частности, относятся адиабатический, изотермический, изобарический и изохорический процессы.
Для
идеального газа нетрудно получить
уравнение политропического процесса
тем же способом, которым ранее было
выведено уравнение Пуассона. Пусть
молярная теплоёмкость идеального газа
в политропическом процессе равна
![]() .
Тогда в соответствии с первым началом
термодинамики(1.5)
имеем выражение:
.
Тогда в соответствии с первым началом
термодинамики(1.5)
имеем выражение:
|
|
(2.99) |
из которого следует:
|
|
(2.100) |
Подставляя это выражение в формулу (2.76) получим
|
|
(2.101) |
или с учетом соотношения Майера (2.70)
|
|
(2.102) |
Сравнение
формул (2.100)
и (2.102)
при условии, что
![]() ,
позволяет записать уравнение
,
позволяет записать уравнение
|
|
(2.103) |
аналогичное уравнению (2.79). Здесь введен параметр
|
|
(2.104) |
который называется показателем политропы.
Из
этой формулы можно также получить
зависимость молярной теплоемкости
![]() от
показателя политропы
от
показателя политропы![]() :
:
|
|
(2.105) |
Преобразование формулы (2.103) к виду:
|
|
(2.106) |
и интегрирование полученного уравнения дает
|
|
(2.107) |
Уравнение
(2.107)
называется уравнением
политропического процесса
или политропы
– кривой, описываемой таким уравнением
в переменных
![]() и
и![]() .
.
Аналогично уравнениям адиабаты (2.86) и (2.87) уравнение политропы может быть переписано в других термодинамических координатах:
|
|
(2.108) |
|
|
(2.109) |
При
адиабатическом процессе
![]() ,
что соответствует нулевой теплоемкости.
Подставив
,
что соответствует нулевой теплоемкости.
Подставив![]() в
формулу(2.104)
и сравнив получившееся выражение с
(2.80),
имеем
в
формулу(2.104)
и сравнив получившееся выражение с
(2.80),
имеем
![]() ,
и уравнение политропы(2.107)
становится уравнением адиабаты:
,
и уравнение политропы(2.107)
становится уравнением адиабаты:
![]() .
.
Если
процесс изотермический, то
![]() ,
так как при этом
,
так как при этом![]() .
В этом случае показатель политропы
.
В этом случае показатель политропы![]() в
пределе равен единице, и уравнение
политропы(2.107)
преобразуется в уравнение Бойля-Мариотта
(2.11):
в
пределе равен единице, и уравнение
политропы(2.107)
преобразуется в уравнение Бойля-Мариотта
(2.11):
![]() .
Обратим внимание на то, что поскольку
при выводе уравнения политропы мы
исключали величину
.
Обратим внимание на то, что поскольку
при выводе уравнения политропы мы
исключали величину![]() ,
то этот вывод не может считаться полностью
корректным для изотермического процесса.
,
то этот вывод не может считаться полностью
корректным для изотермического процесса.
Для
изобарического процесса при
![]() показатель
политропы
показатель
политропы![]() ,
и уравнение(2.107)
принимает форму:
,
и уравнение(2.107)
принимает форму:
![]() .
.
При
изохорическом процессе
![]() должно
стать равным
должно
стать равным![]() ,
что соответствует случаю, когда показатель
,
что соответствует случаю, когда показатель![]() .
Очевидно, переход в формуле(2.107)
к указанному пределу некорректен. Это
связано с тем, что при выводе уравнения
политропы предполагалось, что
.
Очевидно, переход в формуле(2.107)
к указанному пределу некорректен. Это
связано с тем, что при выводе уравнения
политропы предполагалось, что
![]() (см.
переход к формуле(2.103)).
(см.
переход к формуле(2.103)).
Если
умножить уравнение (2.100)
на величину
![]() и
сложить его с уравнением(2.102),
предварительно умноженным на величину
и
сложить его с уравнением(2.102),
предварительно умноженным на величину
![]() ,
то получим уравнение политропы в
дифференциальном виде
,
то получим уравнение политропы в
дифференциальном виде
|
|
(2.110) |
При
![]() это
уравнение приобретает форме:
это
уравнение приобретает форме:
|
|
(2.111) |
Отсюда
имеем
![]() или
или![]() .
Из уравнения(2.110)
также следует, что в процессе, при котором
.
Из уравнения(2.110)
также следует, что в процессе, при котором
![]() ,
давление постоянно:
,
давление постоянно:![]() .
.
Для
политропических процессов значение
теплоёмкости и, соответственно, показателя
политропы могут принимать любые величины.
Отрицательные значения теплоёмкости,
когда показатель политропы
![]() принимает
значения от единицы до величины g (см.
формулу(2.105)),
соответствуют таким условиям, при
которых внутренняя энергия термодинамической
системы убывает при передаче ей
положительного количества теплоты. Это
может быть осуществлено при принудительном
расширении газа.
принимает
значения от единицы до величины g (см.
формулу(2.105)),
соответствуют таким условиям, при
которых внутренняя энергия термодинамической
системы убывает при передаче ей
положительного количества теплоты. Это
может быть осуществлено при принудительном
расширении газа.
В
соответствии с формулой (2.100)
при
![]() величины
величины![]() и
и![]() имеют
различные знаки, и с ростом объёма газа
его температура, а, следовательно, и
внутренняя энергия, уменьшаются. С этим,
в частности, связано понижение температуры
идеального газа при его адиабатическом
расширении, так как в этом процессе
имеют
различные знаки, и с ростом объёма газа
его температура, а, следовательно, и
внутренняя энергия, уменьшаются. С этим,
в частности, связано понижение температуры
идеального газа при его адиабатическом
расширении, так как в этом процессе![]() .
Наоборот, при
.
Наоборот, при![]() с
ростом объёма газа его температура
растёт. В соответствии с первым началом
термодинамики этот рост должен быть
обеспечен подводом к системе дополнительного
количества теплоты.
с
ростом объёма газа его температура
растёт. В соответствии с первым началом
термодинамики этот рост должен быть
обеспечен подводом к системе дополнительного
количества теплоты.
Рассуждая
аналогичным образом, можно на основании
формулы (2.102)
установить связь между приращениями
давления и температуры. При
![]() с
ростом давления температура газа будет
возрастать, а при
с
ростом давления температура газа будет
возрастать, а при![]() -
уменьшаться.
-
уменьшаться.
Работа газа в политропическом процессе может быть определена с помощью интеграла (1.13) при подстановке в него уравнения политропы (2.107), аналогично тому, как это сделано в формуле (2.97):
|
|
(2.112) |
Интегрирование в выражении (2.112) дает формулу для определения работы в политропическом процессе
|
|
(2.113) |
где:
![]() и
и![]() -
начальные давление и объём газа,
-
начальные давление и объём газа,![]() -
его конечный объём.
-
его конечный объём.
Из этой формулы, в частности, следует, что работа при расширении газа всегда остаётся положительной, независимо от того, какое значение принимает показатель политропы, больше или меньше единицы.
Нетрудно
видеть, что для адиабатического процесса
при
![]() выражение(2.113)
переходит в формулу (2.95).
Для изобарического процесса, при
выражение(2.113)
переходит в формулу (2.95).
Для изобарического процесса, при
![]() ,
выражение(2.113)
дает
,
выражение(2.113)
дает
|
|
(2.114) |
где
учтено, что при этом процессе
![]() .
.
Формула
(2.113)
неприменима для описания изохорического
процесса, так как при выводе уравнения
политропы (2.103)
исключался случай
![]() .
Но из формулы(2.100)
очевидно, что работа газа в изохорическом
процессе равна нулю.
.
Но из формулы(2.100)
очевидно, что работа газа в изохорическом
процессе равна нулю.
Другим
процессом, не описывающимся соотношением
(2.113),
является изотермический процесс. Как
было сказано выше, он является предельным
случаем политропического процесса при
![]() .
Работу в изотермическом процессе можно
найти, если в формулу(2.112)
в соответствии с законом Бойля-Мариотта
подставить
.
Работу в изотермическом процессе можно
найти, если в формулу(2.112)
в соответствии с законом Бойля-Мариотта
подставить
![]() ,
а затем выполнить интегрирование. Тогда
имеем
,
а затем выполнить интегрирование. Тогда
имеем
|
|
(2.115) |
или
|
|
(2.116) |
где
учтено постоянство температуры в этом
процессе:
![]() .
.
Поскольку
внутренняя энергия идеального газа не
изменяется в изотермическом процессе,
количество теплоты, полученное газом,
также может быть рассчитано по этой
формуле, то есть в этом процессе
![]() .
При изотермическом расширении идеального
газа работа совершается только за счёт
теплоты, подведённой из окружающей
среды.
.
При изотермическом расширении идеального
газа работа совершается только за счёт
теплоты, подведённой из окружающей
среды.
В заключение параграфа запишем все полученные формулы в единую таблицу 2.1.
|
Термодинамический процесс |
Показательполитропы |
Теплоемкость |
Работа |
|
Изотермический |
1 |
|
|
|
Изобарический |
0 |
|
|
|
Изохорический |
|
|
0 |
|
Адиабатический |
|
0 |
|
Задача
2.4. Какова молярная теплоёмкость
![]() одноатомного
газа и показатель политропы
одноатомного
газа и показатель политропы
![]() для
процесса, в котором работа, совершаемая
газом, в два раза превосходит количество
теплоты, передаваемое ему?
для
процесса, в котором работа, совершаемая
газом, в два раза превосходит количество
теплоты, передаваемое ему?
Решение:
Так как по условию задачи
![]() ,
то в соответствии с первым началом
термодинамики имеем:
,
то в соответствии с первым началом
термодинамики имеем:
![]()
или
![]() .
.
Тогда,
с учетом одноатомности газа (число
степеней свободы
![]() ),
молярную теплоемкость можно определить
по формуле:
),
молярную теплоемкость можно определить
по формуле:
![]() ,
,
а показатель политропы соответственно будет равен:

Задача
2.5. Какая работа совершается одним молем
идеального газа в политропическом
процессе с показателем политропы
![]() при
изменении температуры газа на
при
изменении температуры газа на
![]() ?
?
Решение:
Используя уравнение политропы (2.108):
![]() и
уравнение Клапейрона-Менделеева для
одного моля
и
уравнение Клапейрона-Менделеева для
одного моля
![]() ,
перепишем (2.113)
в виде:
,
перепишем (2.113)
в виде:
 .
.
Отсюда имеем:
![]() .
.
Следовательно, работа, совершаемая одном молем идеального газа в процессе с постоянной теплоёмкостью, определяется только разностью температур конечного и начального состояний газа.
Таким образом, для идеального газа работа, а, следовательно, и количество теплоты, в политропических процессах определяются только конечным и начальным состояниями системы, так как путь перехода из одного состояния в другое определён теплоёмкостью газа (показателем политропы). Однако даже при рассмотрении только политропических процессов, работу и количество теплоты нельзя считать функцией состояния системы, так как переход из одного состояния в другое может быть осуществлен последовательностью различных политропических процессов.
Задача 2.6. Какое количество теплоты передано одноатомному газу в процессе, описанному в условии задачи 2.5?
Решение: В соответствии с формулой (2.105) имеем:
 .
.
Тогда количество теплоты будет равно:
 .
.
Отсюда,
в частности, следует, что при равенстве
показателя политропы показателю адиабаты
для одноатомного газа:
![]() ,
количество теплоты
,
количество теплоты
![]() .
.

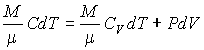 ,
, .
.
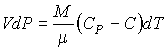 .
. ,
, .
. ,
,
 ,
,
