
- •I біля від’ємного(якщо вважати, що рухаються по провіднику по-
- •1. Для абсолютно однорідного ел. Поля.
- •2. Для реального поля двох заряджених пластин.П оле біля пластин - сильнійше
- •3. Для поля точкового заряду (неоднорідне поле )
- •X з кінців r , позначимо вертикальну і горизонтальну проек-
- •X Тепер спроектуємо на вісь х вектор f2 .
- •2. Конденсатор зарядили до визначеної напруги u і, не від’єднуючи від джерела живлення, роздви-
- •Значення сил струму.
- •96,66 Ом.Як ми бачимо – значення спів-
- •48. Знайти різницю потенціалів на конденсаторі. 49. Знайти різницю потенціалів на конденсаторі
- •І ( напрямок сили струму )
- •Види розрядів.
- •А Цей закон отримується шляхом підстанови першого закону Фарадея у другий.
І ( напрямок сили струму )
Електрони вилітають з від’ємно зарядженого катода і , розганяючись електричним полем, прямують до позитивно зарядженого анода. Математичний вираз закону, який описує електричний струм у вакуумі , ми вже зустрічали в параграфі 6” Напруга” (розділ 1).
2 Ця формула – є одним з виражень закону збереження енергії.
m v Тобто, потенціальна енергія заряду q E d = e U – переходить у
e U = -------- кінетичну енергію заряду ( у вакуумі, на відміну від провідника
2 з опором, електронам ніщо не заважає розганятися) .Ще раз
нагадаємо, що робота електричного поля іде на зміну кінетич-
ної та потенціальної енргії заряду. Електрони можуть покидати катод завдяки багатьом причинам. Напрклад, термоелектронна емісія( нагрівання катоду, яке збільшує тепловий рух молекул, при зіштовхуванні електрони вибиваються з верхніх орбіт та під дією напруги вилітають з катоду), вибивання електронів іншими частинками з катоду, наприклад – фотонами (явище фотоефекту).
Якщо між катодом і анодом міститься газ (діелектрик), то електричний струм в такому газі називається газовий розряд. Під час проходження електронів через газ, електрони зіштовхуються з молекулами газу, гальмуються, розганяються, знову гальмуються і від цього прискоренного руху виникає електромагнітна хвиля видимого діапазону, яку ми бачимо у виглядщі блискавки або світіння у газопроменевій розрядній трубці.
Види розрядів.
Іскровий (критичний) : при великих напругах електрони пробивають дієлектрик у вигляді дуже швидкого лавиноподібного потоку. Приклади: блискавка під час грози, іскра у закороченій розетці, фотоспалах у фотоапараті.
Тліючий розряд : пролітання електронів через дуже розряджений газ, при цьому виникає світіння газу. Приклад : світіння неонових рекламних ламп, в таких лампах містяться інертні гази, кожен з яких світиться своїм кольором (неон – блакитним, ксенон – салатовим тощо).
Коронний розряд : світіння газу біля кінцівок загострених предметів. Наприклад, під час грози електрони шукають найближчий шлях для розраду, тому блискавка б’є у найвищий об’єкт. Але, при великих напругах і при недостатній кількості електричних зарядів, ці заряди прагнуть до загострених. кінцівок предметів. Перед грозою можна спостерігати, як світиться кінчик голки, якщо вийти на балкон на верхньому поверсі (вночі). Або, здавна моряки спостерігали світіння на кінцівках мачт перед штормом, вони називали їх вогнями святого Ельма і вважали, що святий Ельм попереджає їх про загрозу загибелі.
Північне та південне сяйво : світіння верхніх шарів атмосфери Землі при проходженні через них космічних потоків заряджених частинок. Це – один з видів тліючого розряду. Магнітне поле Землі відхиляє від’ємно заряджені частинки (електрони) до північного полюсу, а позитивно заряджені ( α-частинки, ядра легких елементів) до південного. Південне сяйво – більш насичене кольорами, але спостерігається дуже рідко.
Електрична дуга : на відміну від іскрового розряду – триває достатньо довгий час. Для отримання тіскрового розряду необхідно мати потужне і непреривне джерело живлення, яке б поновлювало кожну мить напругу між електродами. Використовується при електрозварці.
Є ще один вид електричного струму у газі : електричний струм у плазмі. Закони цього струму вже не підлягають законам електродинаміки. Але скажемо, що у плазмі, розміщеній в магнітному полі виникають спіралевидні потоки заряджених частинок, при чому від’ємно заряджені – рухаються в одну сторону, а позитивно – в іншу. Плазма – це четвертий стан речовини, в якому електрони і ядра не зв’язані.
Параграф 2. Електричний струм в електролітах.
Електричний струм проводять середовища, в яких є внаявності вільні заряджені частинки. До таких речовин відносяться не тільки метали, а і електроліти – це речовина у стані рідини, в якій містяться заряджені іони. Іонна провідність – це провідність, в якій електричний заряд переносять іони. До електролітів відносять розплавлені метали, розчини кислот, солей і лугів. При розчині,наприклад, солі у воді NaCl – утворюються позитивно заряджені іони натрію та від’ємно заряджені іони хлору. Якщо опустити в такий розчин два електроди, то виникне спрямований рух заряджених іонів, які будуть осідати на електродах (позитивні іони – на від’ємних, а від’ємні – на позитивних).Після того, як всі іони осядуть, електричний струм припиниться.
лампа
Роздивимось малюнок. Якби
у сосуді була чиста 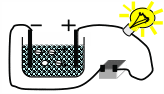
вода, то коло було б просто розімкнуте і електрич-
ного струму не було. Але, якщо налити в сосуд роз-
чин солі або мідного купоросу, то лампа буде горіти.
(Коло буде замкнено). При чому на одному з елект-
родів буде осідати, наприклад чиста мідь. Завдяки
електролізу, можна отримати абсолютно чисті хіміч-
ні елементи. Самий дешевий спосіб отримання літію -
це електроліз.За допомогою електроліза вчений Фа-
акумулятор радей вперше визначив заряд електрона.
Як відбувається перенос електричних зарядів? Від’ємно заряджені іони, тобто атоми в яких є надлишок електронів, притягуються позитивним анодом і при зіштовхуванні з ним віддають йому зайві електрони, а самі – осідають у вигляді нейтральних атомів чистої речовини. Електрони через анод і з’єднювальні дроти прямують до амперметра, який показує силу струму, або до лампи (як на малюнку). Так само позитивно заряджені іони при зіштовхуванні з від’ємним катодом Забирають з катоду електрони і осідають на катоді у вигляді нейтральних атомів.
Перший закон Фарадея.
Маса речовини m , що осідає на електроді , пропорційна електричному заряду q , що пройшов через електроліт.
m = kq m – маса речовини , що виділилася на електроді, вимірюється в кілограмах [кг].
q – електричний заряд, що пойшов через електроліт, вимірюється в Кулонах [Кл].
k – електрохімічний еквівалент речовини, вимірюється в кілограм, розділений на
Кулон [кг/Кл]. Це – власна характеристика електроліту, її дивляться для кожної
речовини в таблиці.
Другий закон Фарадея.
Електрохімічний еквівалент речовини прямопропорційний відношенню атомної (молекулярної) маси речовини А до валентності n .
A
k = ---- ----- q q – електричний заряд, що пойшов через електроліт, вимірюється в Кулонах [Кл].
F n k – електрохімічний еквівалент речовини [кг/Кл].
А – атомна (молекулярна) маса речовини, вимірюється в кг/моль, її дивляться в
таблиці Менделєєва для кожного елемента.
n – валентність хімічного елемента, це число, яке вказує кількість зайвих або недостатніх електронів.
А
--- Це відношення - називається хімічним еквівалентом.
n 4
F – стала
Фарадея .
F
= 9,648
10 Кл / моль
– стала
Фарадея .
F
= 9,648
10 Кл / моль
Об’єднаний закон електролізу Фарадея.
