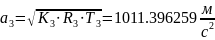- •Определение соотношений компонентов в топливе
- •Расчет параметров, характеризующих интегральные свойства системы в сечении 2-2 камеры сгорания жрд
- •Расчет параметров, характеризующих дифференциальный свойства системы в сечении 2-2 камеры сгорания жрд
- •Расчет параметров химически реагирующей смеси газов в сечении 3-3 камеры сгорания жрд
- •Система уравнений химического равновесия и её решение
- •Определение параметров в сечении 3-3
- •Расчет параметров в выходном сечении сопла 4-4.
- •Графическое изображение разомкнутого цикла жрд
- •Расчет скорости истечения продуктов сгорания из сопла жрд, числа маха и тяги двигателя:
Система уравнений химического равновесия и её решение
Система уравнений химического равновесия состоит в случае одной химической реакции из аппроксимации закона действующих масс в виде уравнения:
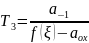
и уравнения баланса
энтальпии
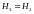 в виде:
в виде:
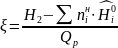
Эта система уравнений решается графоаналитическим способом.
где
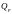 -
изобарный тепловой эффект химической
реакции, определяемый по формуле:
-
изобарный тепловой эффект химической
реакции, определяемый по формуле:
 .
.
5.1. определяются значения величины пробега химической реакции при T=2000;4000;5000
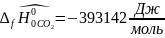
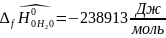
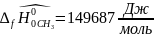
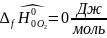

При T=2000К
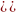
Тогда:
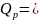
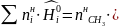
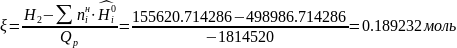
При T=4000К
Тогда:

При T=5000К
Тогда:

5..2 Строится график
зависимости
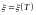 ,
который при пересечении с прямой
,
который при пересечении с прямой
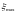 определяет максимальное значение
температуры
определяет максимальное значение
температуры
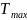 =2767.7
=2767.7
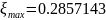 моль
моль
Для определения
коэффициентов аппроксимации
 и
и
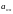 используется аппроксимация константы
равновесия, выраженной через парциальные
давления:
используется аппроксимация константы
равновесия, выраженной через парциальные
давления:

Где

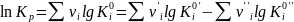
(константа равновесия
химической реакции распада i-го
вещества на газообразные атомы;
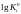 определяется из таблиц индивидуальных
веществ)
определяется из таблиц индивидуальных
веществ)
5.2 Определяются
коэффициенты
и
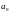 определяются из решения системы из двух
уравнений для двух значений температуры.
определяются из решения системы из двух
уравнений для двух значений температуры.
При температуре T=1000K
 ,
,
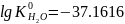 ,
,
 ,
,
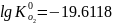

 203.413626
203.413626
При температуре T=3000K
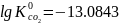 ,
,
 ,
,
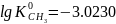 ,
,
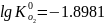

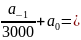 58.069339
58.069339

Коэффициент аппроксимации
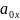 определяется
по формуле:
определяется
по формуле:
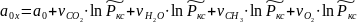
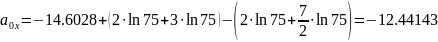
5.3. Задаваясь рядом
значений пробега химической реакции
 определяется значение функции
определяется значение функции
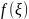 :
:



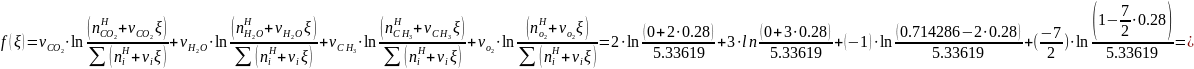 16.584538
16.584538

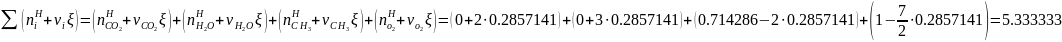
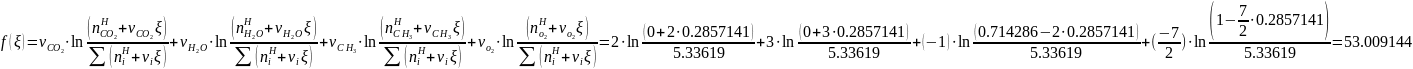
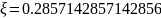
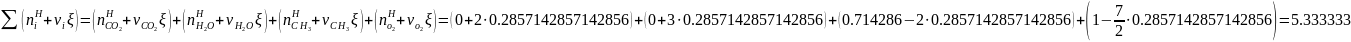

Подставляя в уравнение
аппроксимации закона действующих масс
полученные значения функции
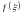 и коэффициентов
и
,
определяется температура смеси газов
при заданных значениях пробега химической
реакции:
и коэффициентов
и
,
определяется температура смеси газов
при заданных значениях пробега химической
реакции:
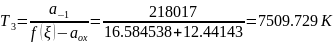
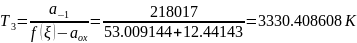
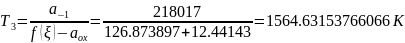
Строится график
зависимости
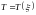 .
Пересечение этой зависимости с
зависимостью
.
Пересечение этой зависимости с
зависимостью
 ,
полученной ранее, дает искомые:
,
полученной ранее, дает искомые:
=2767.422K
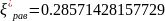
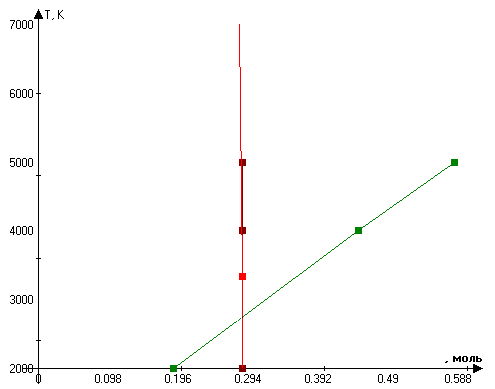
В увеличенном масштабе

что является решением системы уравнений химического равновесия в сечении 3-3 для случая протекания в камере сгорания ЖРД одной химической реакции.
Определяется погрешность определения пробега химической реакции
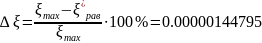
А=
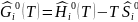


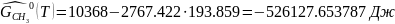

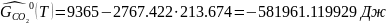
Следовательно:
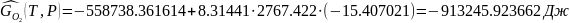
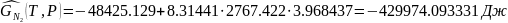

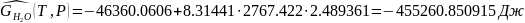
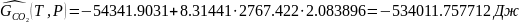
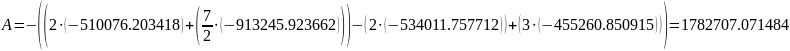
Реакция идет до конца
Определение состава реагентов в сечении 3-3 камеры сгорания ЖРД
Определение числа молей каждого из компонентов смеси
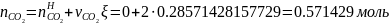
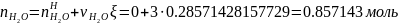

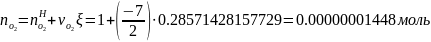

Определяется число молей смеси газов:
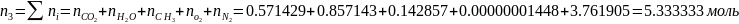
Определяются мольные доли смеси:
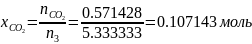

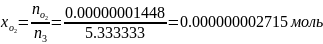
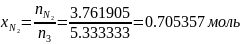

Проверка:
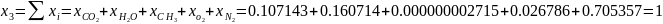
Определяются молярные массы компонентов смеси
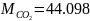 ,
,
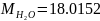 ,
,
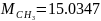 ,
,
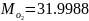 ,
,
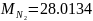
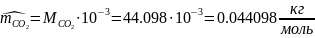
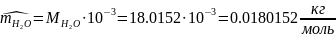
Определяются массы компонентов смеси
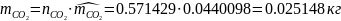
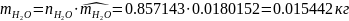

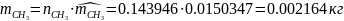
Определяем массу смеси газов:
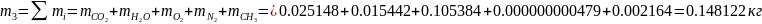
Определяются массовые доли смеси газов

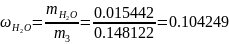



Определение параметров в сечении 3-3
7.1. Определяется молярная масса смеси

7.2. Определяется объем смеси газов:

7.3 Определяется плотность смеси газов:
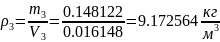
7.4 Определение удельной газовой постоянной смеси газов:
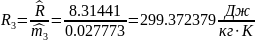
7.5 Определяются молярные энтальпии компонентов смеси:
Интерполируя:
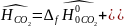
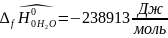
Интерполируя:
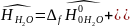
Интерполируя:

Интерполируя:
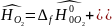
Интерполируя:
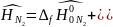
7.5.1. Определяется энтальпия смеси газов:
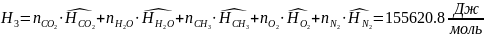
Определяются молярные энтропии компонентов смеси
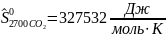
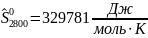
Интерполируя:

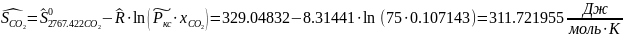
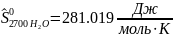
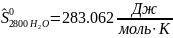
Интерполируя:
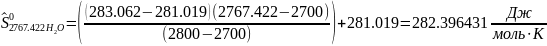
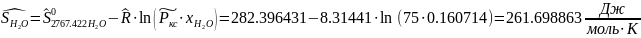


Интерполируя:
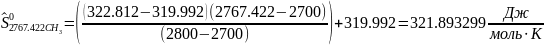
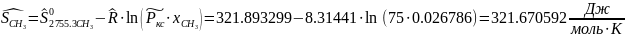
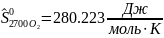
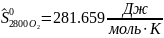
Интерполируя:

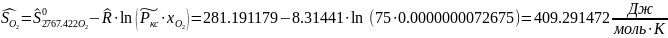
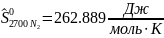
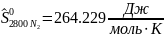
Интерполируя:
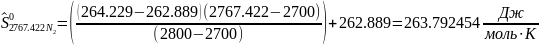
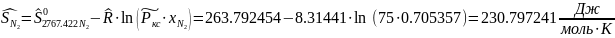
Определяется энтропия смеси веществ

Определяется изобарная теплоемкость смеси газов:

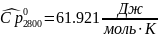
Интерполируя:

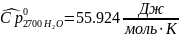

Интерполируя:


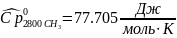
Интерполируя:
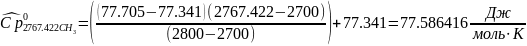
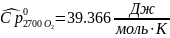

Интерполируя:
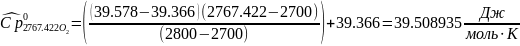

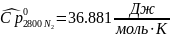
Интерполируя:

Определяется изобарная теплоемкость смеси газов:
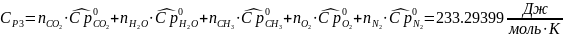
По уравнению Маера определяется изохорная теплоемкость смеси газов
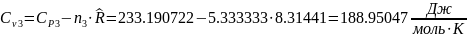
Определяется показатель адиабатного процесса

Определяется скорость звука: