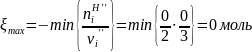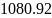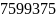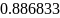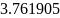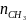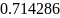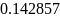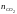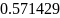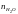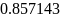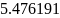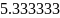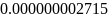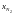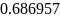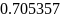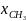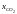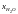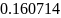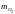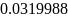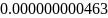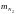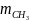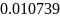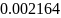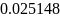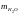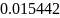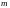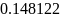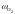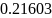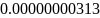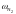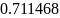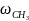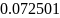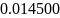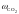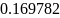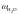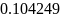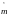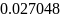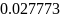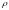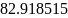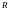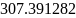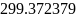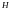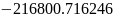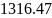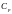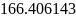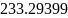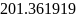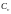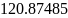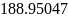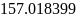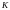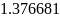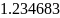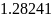- •Определение соотношений компонентов в топливе
- •Расчет параметров, характеризующих интегральные свойства системы в сечении 2-2 камеры сгорания жрд
- •Расчет параметров, характеризующих дифференциальный свойства системы в сечении 2-2 камеры сгорания жрд
- •Расчет параметров химически реагирующей смеси газов в сечении 3-3 камеры сгорания жрд
- •Система уравнений химического равновесия и её решение
- •Определение параметров в сечении 3-3
- •Расчет параметров в выходном сечении сопла 4-4.
- •Графическое изображение разомкнутого цикла жрд
- •Расчет скорости истечения продуктов сгорания из сопла жрд, числа маха и тяги двигателя:
Московский Авиационный Институт
(Государственный технический университет)
Кафедра 204
Курсовая работа
По дисциплине: «Термодинамика энергосистем»
На тему: «Термодинамический расчет ракетного двигателя с учетом одной химической реакции»
Работу выполнила:
Студент Гр. 02-316
Бурова Мария Геннадьевна
Работу принял:
Доцент каф. 204
Меснянкин Сергей Юрьевич
Москва
2011г
Сводная таблица
результатов термодинамического расчета ракетного двигателя.
обозначение |
Ед. измерения |
Сечение 2-2 |
Сечение 3-3 |
Сечение 4-4 |
|
К |
298.15 |
2767.422 |
|
|
Па |
|
|
54048,3 |
|
м3 |
|
|
|
|
Моль |
1 |
|
|
|
Моль |
|
|
|
|
Моль |
|
|
|
|
Моль |
0 |
|
|
|
Моль |
0 |
|
|
|
моль |
|
|
|
|
- |
|
|
|
|
- |
|
|
|
|
- |
|
|
|
|
- |
|
|
|
|
- |
|
|
|
|
Кг |
|
|
|
|
Кг |
|
|
|
|
Кг |
|
|
|
|
Кг |
0 |
|
|
|
Кг |
0 |
|
|
|
Кг |
|
|
|
|
- |
|
|
|
|
- |
|
|
|
|
- |
|
|
|
|
- |
0 |
|
|
|
- |
0 |
|
|
|
Кг/моль |
|
|
|
|
кг/м3 |
|
|
|
|
Дж/кг·К |
|
|
|
|
Дж |
|
|
|
|
Дж/К |
|
|
|
|
Дж/К |
|
|
|
|
Дж/К |
|
|
|
|
- |
|
|
|
Теоретические сведения.
ЖРД – ракетный двигатель, который создает силу тяги за счет вытекания из его сопла газообразных продуктов сгорания топлива. Он состоит из камеры сгорания (I), сопла Лаваля (II) и турбонасосного агрегата – ТНА (III), который подает горючее и окислитель из баков (IV) и (V) к форсункам (VI).
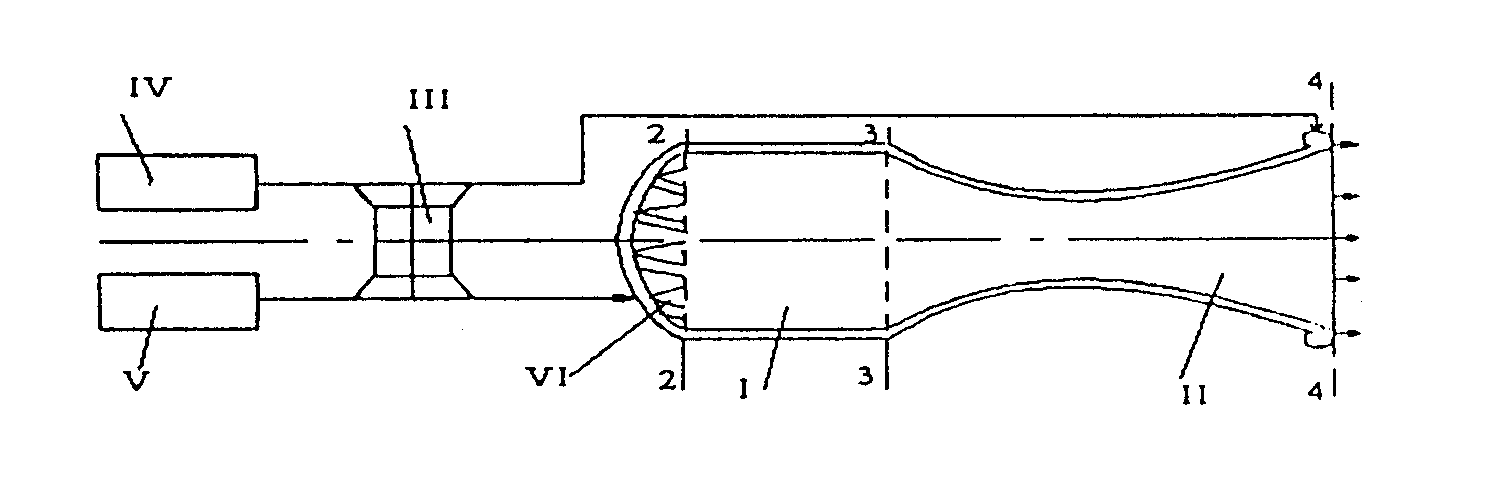
На рисунке: сечение 2-2 - вход в камеру сгорания, 3-3 - конец камеры сгорания, 4-4 - срез сопла.
Задачей настоящей работы является термодинамический расчет ракетного двигателя в условиях термодинамического равновесия реагирующих систем в характерных сечениях двигателя, в результате которого определяется химический состав продуктов сгорания, интегральные и дифференциальные свойства системы в этих сечениях ЖДД.
Целью термодинамического расчета ракетного двигателя в общем случае является определение параметров потока: температуры, давления, скорости, термодинамических и теплофизических свойств рабочего тела и его химического состава, необходимых для определения секундного массового расхода топлива и характерных размеров камеры сгорания, сопла и других агрегатов двигателя, а также для расчета газодинамических процессов и процессов теплообмена.
Дана химическая
реакция
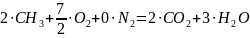
Определение соотношений компонентов в топливе
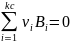
Где
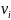 =-
’
и
=
’’-
стихеометрические коэффициенты
компонентов реакции. Для левой части
уравнения (исходные вещества) они
отрицательны, а для правой (продуктов
реакции)- положительны
=-
’
и
=
’’-
стихеометрические коэффициенты
компонентов реакции. Для левой части
уравнения (исходные вещества) они
отрицательны, а для правой (продуктов
реакции)- положительны
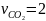 ,
,
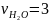 ,
,
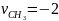 ,
,
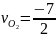 ,
,
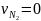
Задаем
число молей кислорода, например
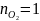 моль.
моль.
Определим число молей азота, который впрыскивается через форсунку в камеру сгорания ЖРД в смеси с кислородом.
Азот не участвует в реакции, но его присутствие влияет на ход реакции . он включен в уравнение химической реакции формально, полагая, что стехиометрический коэффициент
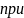
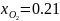 ,
,
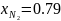 ,
моль
,
моль
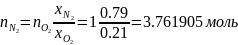
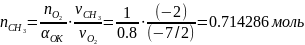
Где
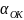 =0.8,
- коэффициент избытка окислителя
=0.8,
- коэффициент избытка окислителя
Определяем число молей смеси газов исходного состава, которое впрыскивается в камеру сгорания через форсунки:
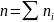
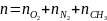
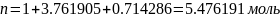
1.2 Определяем мольные доли смеси:
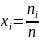
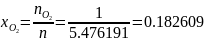
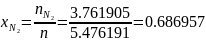
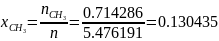
Проверка:
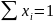
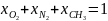
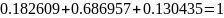
1.3 Определяем массу смеси:
1.3.1 находим молярную массу компонентов смеси:
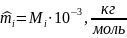
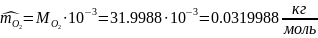
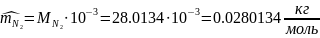
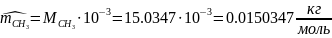
1.3.2 находим массу каждого компонента смеси:
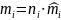 ,
кг
,
кг
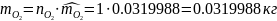
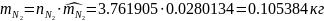
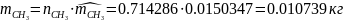
1.3.3 определяем массу всей смеси:
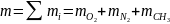
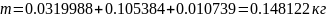
1.4 определяем массовые доли смеси газов:
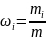
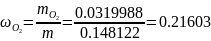
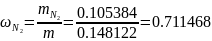
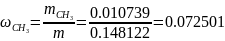
Проверка:
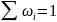
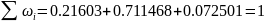
Расчет параметров, характеризующих интегральные свойства системы в сечении 2-2 камеры сгорания жрд
Определяем молярную массу смеси
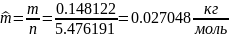
Определяется объем смеси газов:
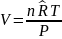
Где:
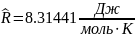 - молярная газовая постоянная
- молярная газовая постоянная
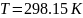 -температура
в сечении 2-2
-температура
в сечении 2-2
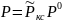 Па- давление в камере сгорания,
Па- давление в камере сгорания,
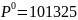 Па,
Па,
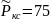 Па
Па
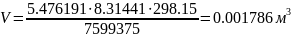
определяется плотность смеси газов:
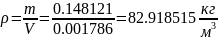
определяется удельная газовая постоянная смеси газов:
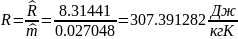
определяем энтальпию смеси индивидуальных веществ
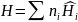
Где
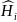 -
молярная энтальпия i-го
вещества
-
молярная энтальпия i-го
вещества
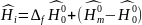
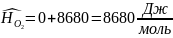
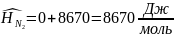
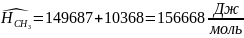
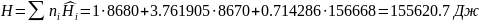
Определяется энтропия смеси газов:
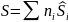
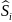 -молярная
энтропия, которая зависит от температуры
и давления
-молярная
энтропия, которая зависит от температуры
и давления
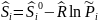
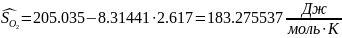
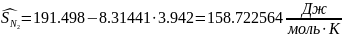
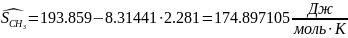
Следовательно:
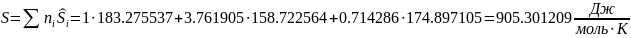
Расчет параметров, характеризующих дифференциальный свойства системы в сечении 2-2 камеры сгорания жрд
Определяется изобарная теплоемкость смеси газа
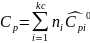
Где
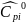 -
молярная изобарная теплоемкость i-го
компонента смеси, берется из таблиц
справочника.
-
молярная изобарная теплоемкость i-го
компонента смеси, берется из таблиц
справочника.
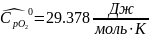
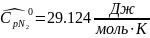
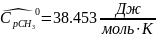
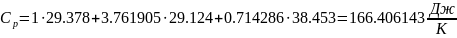
определяется изохорная теплоемкость смеси газов:
По уравнению Майера:
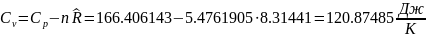
Определяется показатель адиабаты смеси газов
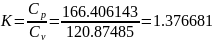
Определяется скорость звука
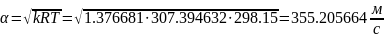
Расчет параметров химически реагирующей смеси газов в сечении 3-3 камеры сгорания жрд
Процесс сгорания топлива в камере
сгорания ЖРД является
изобарно-адиабатно-изоэнтальпийный,
так как теплота извне к системе не
подводится и согласно уравнению первого
закону термодинамики для просто закрытой
системы
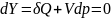 т.е энтальпия в сечении 3-3 камеры сгорания
должна быть равной энтальпии в сечении
2-2
т.е энтальпия в сечении 3-3 камеры сгорания
должна быть равной энтальпии в сечении
2-2
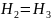 увеличение температуры рабочего тепла
в камере сгорания двигателя происходит
за счет выделения тепловой энергии при
протекании химической реакции сгорания
топлива. При этом задача определения
температуры на выходе из камеры сгорания
увеличение температуры рабочего тепла
в камере сгорания двигателя происходит
за счет выделения тепловой энергии при
протекании химической реакции сгорания
топлива. При этом задача определения
температуры на выходе из камеры сгорания
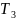 и химического состава продуктов сгорания
сводится к расчету равновесного состояния
системы в сечении 3-3 при двух фиксированных
параметрах: (
и химического состава продуктов сгорания
сводится к расчету равновесного состояния
системы в сечении 3-3 при двух фиксированных
параметрах: (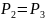 )
и энтальпии
)
и энтальпии
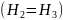 .
.
В соответствии со вторым законом
термодинамики энтропия системы будет
возрастать из-за необратимого протекания
процесса сгорания топлива и при достижении
состояния равновесия примет
экспериментальной значение, соответствующий
максимуму энтропии. Таким образом,
процесс сгорания в камере сгорания ЖРД
соответствует переходу системы из
химически неравновесного в равновесное
состояние, который полностью определяется
заданием двух независимых термодинамических
параметров (в данном сучае p-const,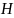 -const)
-const)
Состав реагирующей смеси газов в
начальный момент химической реакции
определяется числами молей вещества,
впрыскиваемых в камеру сгорания через
форсунки
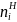 ,
моль. Для нашей реакции:
,
моль. Для нашей реакции:
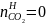 ,
,
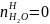 ,
,
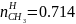 моль,
моль,
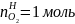 ,
,
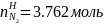
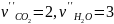 ,
,
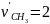 ,
,
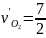 ,
,
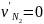
, , , ,
Текущее значение количеств веществ для термодинамической системы с учетом одной химической реакции определяется соотношением
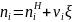
Где - количество i-ой компоненты смеси в начальный момент реакции
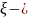 величина пробега химической реакции,
которая полностью характеризует в этом
случае степень изменения состава системы
при химической реакции. Она показывает
на сколько сдвинулась реакция по
отношению к начальному состоянию
термодинамической системы.
величина пробега химической реакции,
которая полностью характеризует в этом
случае степень изменения состава системы
при химической реакции. Она показывает
на сколько сдвинулась реакция по
отношению к начальному состоянию
термодинамической системы.
Неизвестная величина
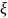 при переходе системы в равновесное
состояние определяется из условия
равенства нулю сродства химической
реакции А , которое при сопряжении
термодинамической системы с окружающей
средой Р,Т-const
имеет вид:
при переходе системы в равновесное
состояние определяется из условия
равенства нулю сродства химической
реакции А , которое при сопряжении
термодинамической системы с окружающей
средой Р,Т-const
имеет вид:
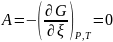
При
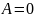 достигается состояние равновесие
системы. При этом сводная энергия Гиббса
достигается состояние равновесие
системы. При этом сводная энергия Гиббса
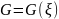 принимает минимальное значение, а пробег
химической реакции
принимает минимальное значение, а пробег
химической реакции
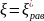 .
Для системы состоящей из смеси идеальных
газов
.
Для системы состоящей из смеси идеальных
газов
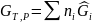
Где
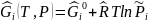
Тогда А=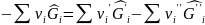
При
отклонении от состояния равновесия
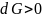 если
если
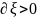 ,
то А<0 и если
,
то А<0 и если
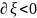 ,
то А>0
,
то А>0
(рис.2)
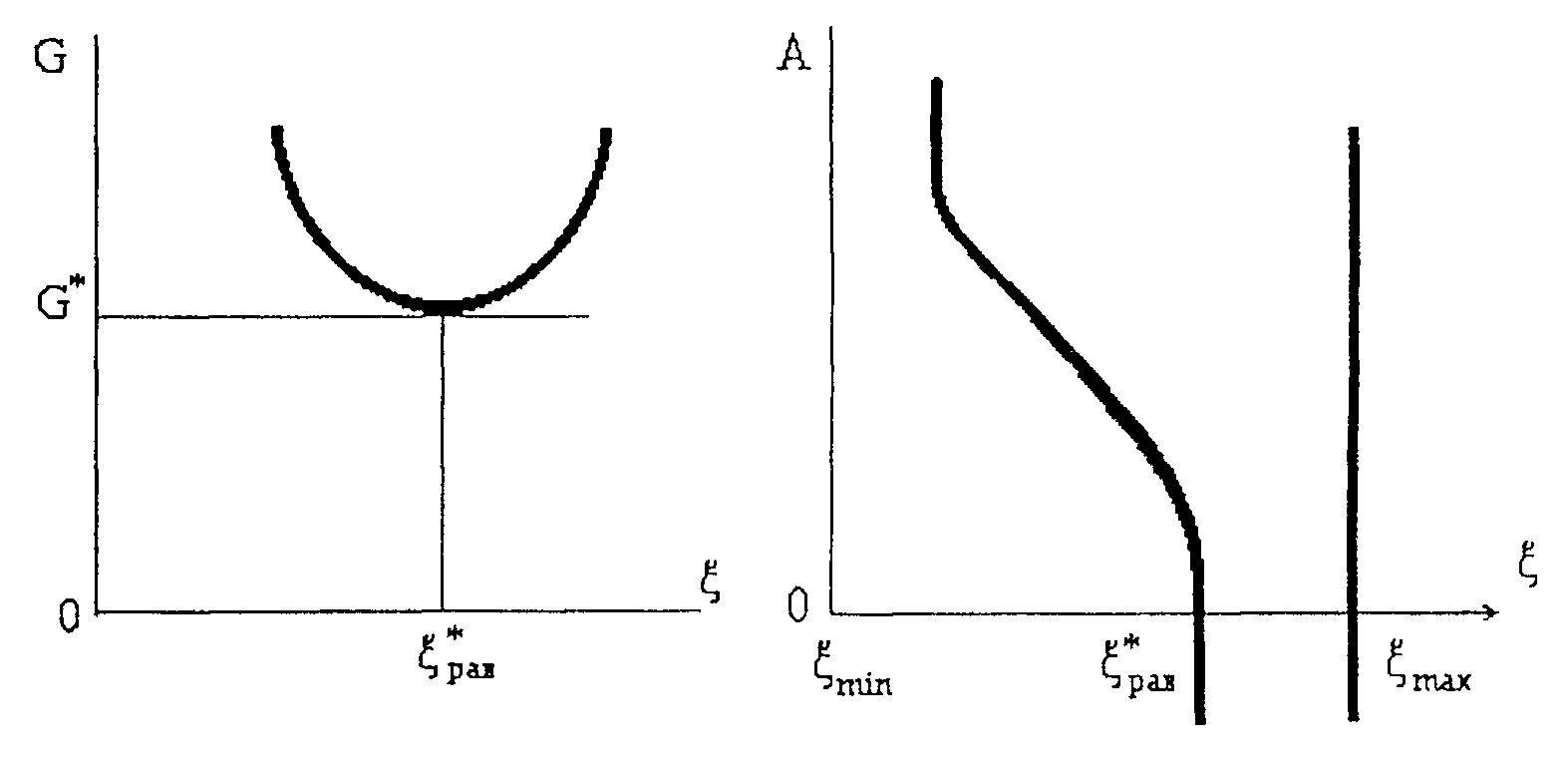
Рис. 1 Рис.2
Реакция слева направо может идти до тех пор, пока в системе присутствуют все реагенты, имеющиеся в левой части уравнения химической реакции, т.е.
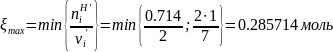
Для химической реакции, протекающей справа налево, имеем: